М.Ю. Просянников, О.В. Константинова, Н.В. Анохин, Д.А. Войтко
- Просянников М.Ю. – к.м.н., зав. отделом мочекаменной болезни НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России, prosyannikov@gmail.com. AuthorID 791050
- Константинова О.В. – д.м.н., главный научный сотрудник отдела мочекаменной болезни НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России. konstant-ov@yandex.ru, AuthorID 679965
- Анохин Н.В. – к.м.н., научный сотрудник отдела мочекаменной болезни НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России. anokhinnikolay@yandex.ru, AuthorID 880749
- Войтко Д.А. – к.м.н., научный сотрудник отдела мочекаменной болезни НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России. 1987vda@mail.ru, AuthorID 942353
Кальциевый уролитиаз – наиболее распространенная форма мочекаменной болезни (МКБ). Одной из характерных особенностей уролитиаза являются частые рецидивы процессов камнеобразования. При этом многие аспекты патогенеза МКБ до конца не изучены.
По одной из самых распространенных теорий патогенеза МКБ считается, что в основе процессов литогенеза лежат два механизма: наличие бляшки Рэндалла в паренхиме почки и наличие перенасыщенной камнеобразующими веществами мочи. Бляшка Рэндалла всегда состоит из солей кальция фосфата, а ее дальнейший рост происходит за счет отложения кристаллов кальциевых солей на уже имеющуюся кальций-фосфатную основу [1].
При этом обязательным условием роста кальций-оксалатного конкремента является перенасыщенность мочи камнеобразующими веществами [2,3]. К ним относят кальций, мочевую кислоту, оксалат (кальциевая соль щавелевой кислоты) [4,5]. Повышенная концентрация указанных веществ приводит к их осаждению, что инициирует литогенез. Кристаллы постепенно адгезируются к бляшке Рэндалла, состоящей из кальций-фосфата и происходит рост мочевого камня (рис. 1).
Препятствовать процессу камнеобразования специалисты могут, влияя на основные этапы патогенеза МКБ. Одним из направлений метафилактики уролитиаза является воздействие на перекисное окисление липидов, как на одну из причин образования бляшек Рэндалла. В данном случае антиоксиданты являются препаратами выбора [7].
Кроме оказания влияния на процессы образования бляшек Рэндалла, профилактика повторного камнеобразования при МКБ возможна путем снижения концентрации в моче основных камнеобразующих веществ – кальция, оксалатов, мочевой кислоты. Известно, что гиперкальциурия, гипероксалурия, гиперурикурия способны инициировать образование кальций-оксалатных камней [8,9].
Гипероксалурия – одно из наиболее часто встречаемых метаболических литогенных нарушений, выявляемых при кальциевом уролитиазе. Оксалат представляет собой органическую соль щавелевой кислоты. При физиологических уровнях pH мочи оксалат образует растворимую соль с натрием и калием. Однако при соединении с кальцием щавеливая кислота образует нерастворимое в воде соединение – кальций оксалат [10].
Выделяют 2 основных пути появления оксалата в организме человека: экзогенный и эндогенный. 85-90% оксалата в организме человека синтезируются эндогенно. Пути метаболизма оксалатов в гепатоцитах представлены на рисунке 2. Часть представленных процессов протекает в пероксисомах, часть – цитоплазме клеток. Эндогенный оксалат синтезируется из 2-х основных источников: аскорбиновой кислоты и глиоксилата [11]. Основной путь синтеза оксалата – окисление глиоксилата, основным источником которого является гликолат. Эти метаболические реакции катализируются несколькими ключевыми ферментами, включая алкогольдегидрогеназу 1 (ADH-1), лактатдегидрогеназу (LDH), гидроксикислотную оксидазу 1 (HAO-1), ксантиноксидазу (XO), аланинглиоксилат аминотрансферазу (AGAT) и глиоксилатредуктазу (GRHPR) [11]. Помимо аскорбиновой кислоты и глиоксилата другие соединения, такие как различные аминокислоты (триптофан, фенилаланин, тирозин), креатинин, пурины и даже глюкоза и другие углеводы могут служить предшественником оксалата [12,13]. Различные условия способны влиять на синтез оксалатов. Одним из важнейших параметров является рН внутриклеточной жидкости. Изменения данного параметра способны влиять на активность ферментов [14].
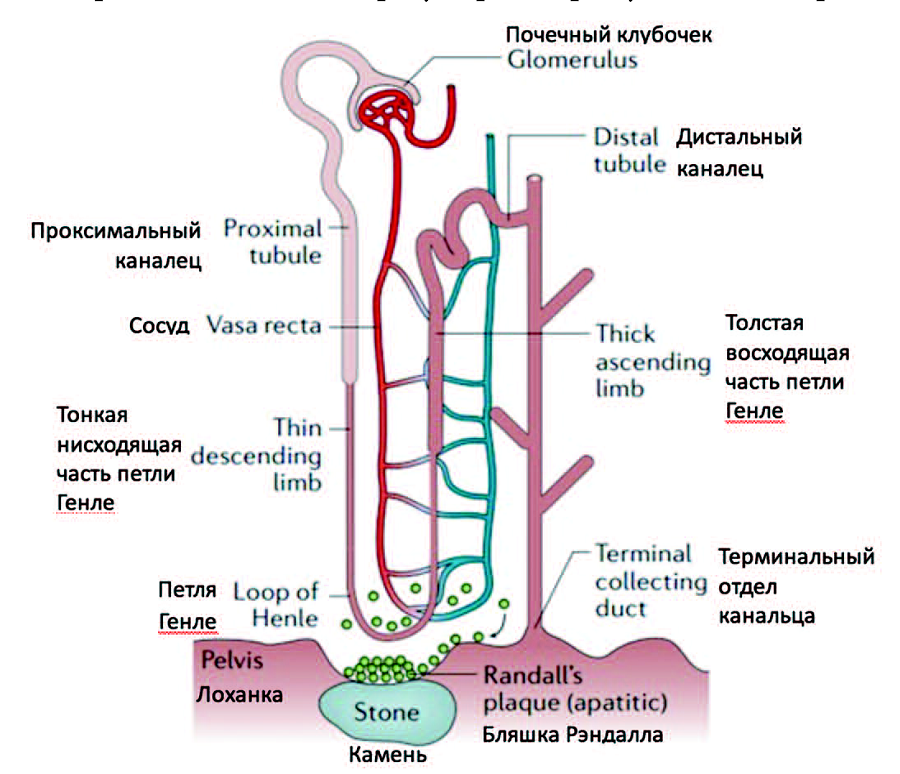
Рис.1. Современные представления о патогенезе камнеобразования при МКБ, образование бляшки Рэндалла [6]
Fig.1. Modern views on the pathogenesis of stone formation in the ICD, the formation of Randall plaque [6]
Экзогенный оксалат поступает с пищей и абсорбируется главным образом в толстом кишечнике. Экзогенный оксалат попадает в организм человека в основном при потреблении листьев, орехов, плодов и коры растительных продуктов. В современном рацион основным источником оксалата является картофель, шоколад, чай. Пищевые продукты животного происхождения практически не содержат оксалатов [11]. Необходимо подчеркнуть, что из пищи абсорбируется только 2-10% потребляемого оксалата, тогда как большая часть оксалата (90-98%) служит источником питания для бактерий, находящихся в кишечнике или экскретируется с калом [15].
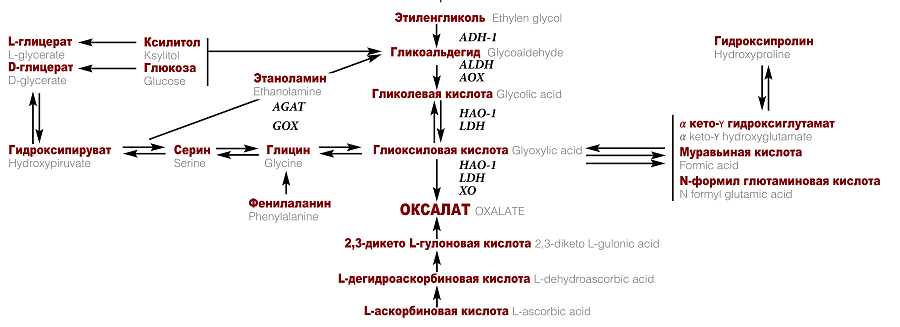
Рис. 2. Пути синтеза эндогенного оксалата в организме [14]
Fig. 2. The synthesis of endogenous oxalate in the body [14]
Соотношение эндогенного и экзогенного оксалата в организме зависит главным образом от диеты пациента, от количества оксалата в потребляемой пище. Как поступление экзогенного оксалата, так и синтез эндогенного способствуют поддержанию уровня оксалата в крови. Большая часть оксалата крови (90-95%) выводится из организма почками, тогда как только 5-10% оксалата экскретируется кишечником (рис. 3). Определенное количество эндогенного оксалата экскретируется из организма вместе с желчью. Небольшая часть оксалата возвращается в гепатоциты, и таким образом, постоянно циркулирует в организме [16,17].
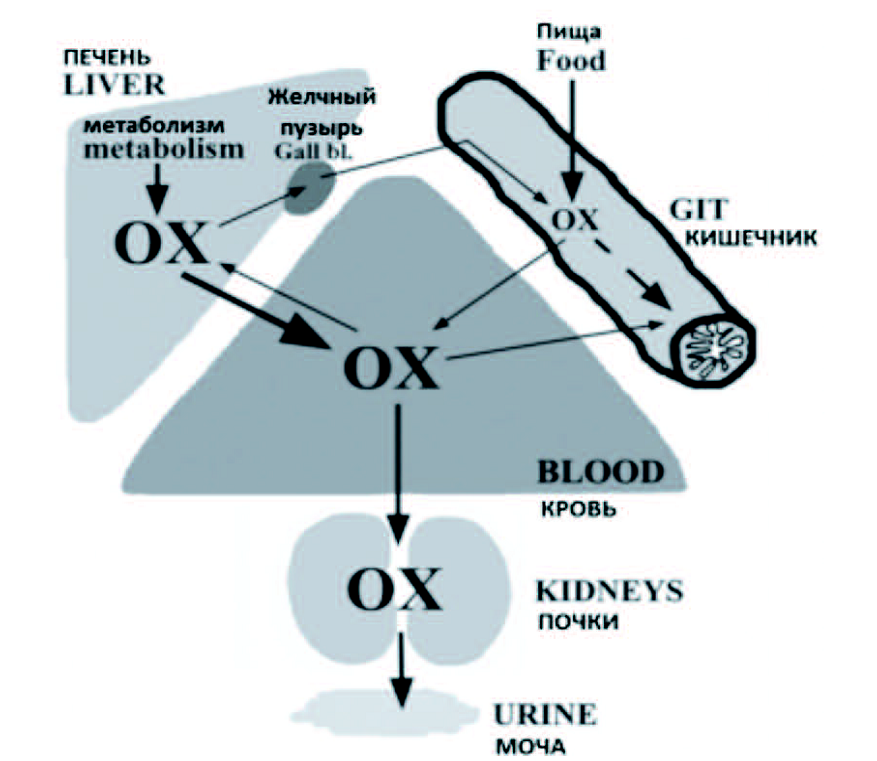
Рис. 3. Метаболизм оксалата в организме человека [14]
Fig. 3. Oxalate metabolism in the human body [14]
Полагают, что в метаболизме человека оксалат не играет какой-либо существенной роли и является конечным продуктом обмена веществ, как и мочевая кислота. Если бы не высокое сродство оксалата к кальцию и низкая растворимость соли оксалата кальция, метаболизм оксалата не представлял бы особого интереса. В то же время оксалат мочи является одним из значимых литогенных факторов при МКБ.
В почках происходит фильтрация, реабсорбция и секреция оксалата [18]. Гломерулярная фильтрация оксалатов зависит от уровня оксалатов в плазме крови. В то же время канальциевый транспорт (реабсорбция и секреция) оксалатов происходит под влиянием транспортного белка SLC26A1, который обеспечивает поглощение оксалата в клетку через базолатеральную мембрану в обмен на сульфат [19]. Было доказано, что этот белок также влияет на секрецию оксалата в кишечнике, дефект SLC26A1 способствует увеличению кишечной абсорбции оксалата в тонкой кишке [20]. Доказано, что решающее значение в регуляции уровня оксалатов в плазме крови имеет канальцевая секреция и клубочковая фильтрация, поскольку была продемонстрирована сильная корреляция между высокими уровнями оксалатов в плазме и секрецией оксалатов [21].
Таким образом, снижение уровня экскреции оксалатов в моче имеет одно из ведущих значений в метафилактике кальциевого уролитиаза.
Уменьшить концентрацию в моче основных камнеобразующих веществ у пациентов с МКБ возможно путем назначения медикаментозных препаратов, например, цитратных смесей, тиазидных диуретиков и др. [22]. Однако синтетические вещества химического происхождения, применяемые при метафилактике МКБ, всегда будут иметь широкий спектр побочных эффектов. Особенно заметно побочное действие подобных средств при их длительном приеме, который необходим именно при метафилактике уролитиаза. К тому же, многие пациенты достаточно негативно относятся к потребности принимать нерастительные лекарственные средства в течение длительного времени.
В данной ситуации назначение фитопрепаратов весьма оправдано и является вариантом выбора. К тому же положительное влияние многих трав на процессы литогенеза хорошо изучено, эффективность их применения научно доказана.
При метафилактике кальций-оксалатного и кальцийфосфатного уролитиаза достаточно давно и с успехом применяются экстракты трав Филлантуса Нирури (Phyllanthus niruri), Фукуса Везикулозуса (Fucus vesiculosus), Десмодиума стираксолистного [23,24].
Филлантус Нирури (Phyllanthus niruri, рис. 4) – тропическое однолетнее растение, относящееся к семейству молочайных, которое встречается в дикой природе. Проведенное N.D. Pucci и соавт. в 2018 году исследование, в котором были проанализированы данные 56 пациентов с диагнозом МКБ, показало, что прием P. niruri в течение 12 недель статистически достоверно снижает концентрацию оксалатов в моче на 48,81%, снижает уровень мочевой кислоты в моче на 70% [25].
M.E. Barros и соавт в своей работе, заключающейся в моделировании кальций-оксалатной формы уролитиаза у крыс, показали, что применение экстракта P. niruri в течение 40 дней, уменьшает массу и число кальций-оксалатных камней у крыс в 3,8 раза. К тому же потребление P. niruri делает более гладкими по форме и менее твердыми формирующиеся конкременты, что существенно облегчает их отхождение из мочевых путей [23].
Исследователи из Бразилии J.L. Nishiura и соавт. после изучения влияния приема P. niruri на биохимические параметры суточной мочи у пациентов с кальций-оксалатным уролитиазом пришли к выводу, что экстракт растения нормализует метаболизм кальция у пациентов с гиперкальциурией, уменьшая его экскрецию на 41,2% [26].
Большое влияние на процессы литогенеза оказывают ингибиторы камнеобразования: цитраты, магний, гликозамингликаны. Пониженный уровень экскреции этих веществ является одним из основных метаболических факторов риска развития МКБ [27]. A.M. Freitas и соавт. в эксперименте на крысах изучили уровень цитратов, магния и гликозамингликанов в моче после введения опытным животным экстракта P. niruri. Ученые обнаружили, что на фоне приема P. niruri уровень цитратов и магния в моче не увеличивался. Тем не менее, статистически значимо возрастал уровень экскреции гликозамингликонов, что подтверждает способность P. niruri препятствовать развитию МКБ [28].
Назначение P. niruri оказывает положительной влияние на отхождение мочевых камней в раннем послеоперационном периоде после выполнения литотрипсии. Согласно данным исследования, проведенного S. Micali и соавт., регулярный прием P. niruri после дистанционной литотрипсии нижней чашечки почки статистически значимо увеличивает частоту самостоятельного отхождения фрагментов мочевых камней по сравнению с аналогичными показателями у пациентов из контрольной группы (p=0,01) [29].
Таким образом, доказана эффективность применения P. niruri, как при метафилактике кальций-оксалатного и кальций-фосфатного уролитиаза вне зависимости от выявленных метаболических литогенных нарушений, так и в раннем послеоперационном периоде после дробления мочевых камней для повышения эффективности литокинетической терапии.
Экстракт травы Fucus vesiculosus (рис. 5) с успехом применяется для лечения больных не только уролитиазом, но и многих других заболеваний. Fucus vesiculosus – бурая водоросль – многоклеточное растение более метра в длину, разрастающееся в виде куста. Произрастает на каменистом морском грунте. В Российской Федерации встречается на побережье северных морей (Балтийского, Баренцева, Белого и др.).
По данным Н.А. Боева Fucus vesiculosus в диапазоне концентраций от 40 до 1000 мг/мл проявляет антимикробную активность, как в отношении грамположительных кокков, так и грамотрицательных энтеробактерий [30]. Антимикробная активность Fucus vesiculosus связана с наличием в составе водоросли флавоноидов и других соединений [31].

Рис. 4. Phyllanthus niruri

Рис. 5. Fucus vesiculosus

Рис. 6. Desmodium styracifolium
Данные Н.А. Боева подтверждают результаты исследования А.П. Годовалова и соавт. В своей работе авторы также пришли к выводу, что настой Fucus vesiculosus обладает антистафилококковой активностью, антибактериальным действием в отношении представителей кишечной микрофлоры [32].
Более того, российские ученые Е.В. Журишкина и соавт. показали, что воздействие фукоидана, который содержится в клеточных стенках бурых водорослей, на малигнизированные клетки приводит к индукции апоптоза и нарушению клеточного цикла опухолевых клеток [33].
Таким образом, Fucus vesiculosus является растением, проявляющим разнообразную биологическую активность: противоопухолевую, антибактериальную, антивирусную, антикоагулянтную, иммуномодулирующую и противовоспалительную [34].
Применение Fucus vesiculosus при МКБ обусловлено его влиянием на метаболические литогенные процессы. Доказано, что фукоидан способствует снижению концентрации оксалата в моче в 3,72 раза, уменьшает выделение кальция с мочой на 83%, снижает экскрецию фосфатов на 34,2%, повышает уровень экскреции с мочой цитратов на 25,4% и гликозамингликонов в 3,17 раза [35].
Более того, доказано, что Fucus vesiculosus снижает концентрацию одного из маркеров перекисного окисления липидов и оксидативного стресса – малонового диальдегида у крыс при моделированном кальций-оксалатном уролитиазе по сравнению с контрольной группой [36].
Десмодиум стираксолистный (Desmodium styracifolium, рис. 6) – средство растительного происхождения, традиционно использовавшееся в китайской медицине для лечения МКБ и официально зарегистрированное в китайской фармакопее [37]. Исследования in vitro подтвердили, что D. styracifolium снижает риск рецидива кальций-оксалатного уролитиаза посредством торможения процессов роста и агрегации кристаллов кальций-оксалата [38].
Исследователи из Китая Jun Mi и соавт. изучили влияние D. styracifolium на крыс при имитации этиленгликолевой модели уролитиаза. Авторы установили, что применение экстракта D. styracifolium в средних и высоких дозах повышает уровень экскреции цитрата с мочой, снижает содержание общего кальция в моче, стимулирует увеличение диуреза. Необходимо подчеркнуть, что на фоне приема D. styracifolium в крови подопытных мышей было замечено снижение уровня малонового диальдегида – вторичного продукта липидной пероксидации [39]. Таким образом, экстракт D. styracifolium замедляет процессы перекисного окисления липидов и тормозит инициацию процессов камнеобразования.
Одним из фитопрепаратов, сочетающих в себе экстракты вышеописанных растений, является биологически активная добавка к пище «Оксалит» (далее Препарат), производство «SH PHARMA», Россия. В составе Препарата содержатся экстракты трав Фукуса Везикулозуса, Филлантуса Нирури и Десмодиума стираксолистного.
Применение Препарата обоснованно у пациентов с МКБ при выявлении в биохимическом анализе мочи гипероксалурии, гиперкальциурии. Кроме того, доказанные антиоксидантные свойства экстракта D. styracifolium, выявленная ингибиторная активность P. niruri, антибактериальное действие Fucus vesiculosus позволяют назначать препарат при метафилактике МКБ, в том числе, при идиопатической форме кальций-оксалатного и кальций-фосфатного уролитиаза.
Одним из вариантов применения Препарата является его использование для улучшения литокинетической терапии после проведенного сеанса дистанционной литотрипсии.
Как было отмечено, экстракт P. niruri стимулирует отхождение фрагментов мочевых камней после сеансов литотрипсии.
Вышеописанные эффекты действующих веществ позволяют говорить о возможности их применения при противорецидивном лечении больных уролитиазом. Применение препаратов, содержащих экстракты Phyllanthus niruri, Fucus vesiculosus и Desmodium styracifolium, может стать дополнением к описанной в различных национальных рекомендациях традиционной консервативной терапии, одобренной к назначению при кальций-оксалатном уролитиазе. Для оценки комплексного влияния всех описанных компонентов на метаболизм пациента, страдающего МКБ, а также для определения их роли в метафилактике уролитиаза, необходимо проведение дальнейших клинических исследований.
ЛИТЕРАТУРА
- Taylor ER, Stoller ML. Vascular theory of the formation of Randall plaques. Urolithiasis 2015;43(Suppl 1):41-5. doi: 10.1007/s00240-014-0718-4.
- Pak CY, Sakhaee K, Moe OW, Poindexter J, Adams-Huet B, Pearle MS,et al. Defining hypercalciuria in nephrolithiasis. Kidney Int 2011;80(7):777-82. doi: 10.1038/ki.2011.227. Epub 2011 Jul 20.
- Pearle MS, Lotan Y. Urinary lithiasis: etiology, epidemiology and pathogenesis. Campbell-Walsh Urology, ninth edition. [Edit. Alan J. Wein]. Philadelphia, PA, 2007 2: 1363-1392.
- Петров С.Б., Левковский С.Н., Левковский Н.С. Насыщение мочи малорастворимыми камнеобразующими соединениями у здоровых и больных уролитиазом. Клиническая патофизиология 2004;(2):28-33. [Petrov S.B., Levkovskiy S.N., Levkovskiy N.S. Saturation of urine with slightly soluble stone-forming compounds in healthy and urolithiasis patients. Klinicheskaya patofiziologiya=Clinical pathophysiology 2004 2: 28-33. (In Russian)].
- Türk C, Petřík A, Sarica K, Seitz C, Skolarikos A, Straub M, Knoll T. Guidelines on Diagnosis and Conservative Managementof Urolithiasis. Eur Urol 2016;69(3):468-74. doi: 10.1016/j.eururo.2015.07.040
- Bird VY, Khan SR . How do stones form? Is unification of theories on stone formation possible? Arch Esp Urol 2017;70(1):12–2
- Kizivat T, Smolić M, Marić I, Tolušić Levak M, Smolić R, Bilić Čurčić I et al. Antioxidant Pre-Treatment Reduces the Toxic Effects of Oxalate on Renal Epithelial Cells in a Cell Culture Model of Urolithiasis. Int J Environ Res Public Health. 2017;14(1):E109. doi: 10.3390/ijerph14010109
- Константинова О.В. Прогнозирование и принципы профилактики МКБ. Дис. … д.м.н. М.: 1999 г. [Konstantinova O.V. Prediction and principles of prevention of urolithiasis. Dr. Med.Sci [dissertation]. M., 2000, 234 p. (In Russian)].
- Pearle MS, Goldfarb DS, Assimos DG, Curhan G, Denu-Ciocca CJ, Matlaga BR et al. Medical management of kidney stones: AUA guideline. J Urol 2014;192(2):316-24. doi: 10.1016/j.juro.2014.05.0062015
- Bhasin B, Urekli HM, Atta MG. Primary and secondary hyperoxaluria: understanding the enigma. World J Nephrol. 2015;4(2):235-44. doi: 10.5527/wjn.v4.i2.235..
- Shekarriz B, Schwartz BF, Stoller ML, Terries MK, Talavera F. Hyperoxaluria [Электронный ресурс]. Jun, 2019. Режим доступа: Emedicine.medscape.com
- Hagler L, Herman RH. Oxalate metabolism. Am J Clin Nutr 1973;26:758-65.
- Yanagawa M, Maeda-Nakai E, Yamakawa K, Yamamoto I, Kawamura J, Tada S, Ichiyama A. The formation of oxalate from glycolate in rat and human liver. Biochim Biophys Acta 1990;1036:24-33.
- Brzica H, Breljak D, Burckhardt BC, Burckhardt G, Sabolić I. Oxalate: from the environment to kidney stones. Arh Hig Rada Toksikol 2013;64(4):609-30. doi: 10.2478/10004-1254-64-2013-2428
- Chen Z, Ye Z, Zeng L, Yang W. Clinical investigation on gastric oxalate absorption. Chin Med J 2003; 116:1749-51.
- Williams AW, Wilson DM. Dietary intake, absorption, metabolism and excretion of oxalate. Semin Nephrol 1990;10:2-8.
- Hautman RE. The stomach: a new and powerful oxalate absorption site in man. J Urol 1993;149:1401-4.
- Knight TF, Sansom SC, Senekjian HO, Weinman EJ. Oxalate secretion in the rat proximal tubule. Am J Physiol 1981;240:295–298
- Mount DB, Romero MF. The SLC26 gene family of multifunctional anion exchangers. Pflugers Arch 2004;447:710–721
- Jiang Z, Asplin JR, Evan AP, Rajendran VM, Velazquez H, Nottoli TP et al. Calcium oxalate urolithiasis in mice lacking anion transporter Slc26a6. Nat Genet 2006;38(4):474
- Bergsland KJ, Zisman AL, Asplin JR, Worcester EM, Coe FL. Evidence for net renal tubule oxalate secretion in patients with calcium kidney stones. Am J Physiol Renal Physiol 2011;300: 311–318
- Jung H, Andonian S, Assimos D, Averch T, Geavlete P, Kohjimoto Y, et al. Urolithiasis: evaluation, dietary factors, and medical management: an update of the 2014 SIU-ICUD international consultation on stone disease. World J Urol 2017;35(9):1331-1340. Doi: 10.1007/s00345-017-2000-1
- Barros ME, Lima R, Mercuri LP, Matos JR, Schor N, Boim MA Effect of extract of Phyllanthus niruri on crystal deposition in experimental urolithiasis. Urol Res 2006;34(6):351-7
- Coothan KV, Anthony J, Sreenivasan PP, Palaninathan V. Physico-chemical alterations of urine in experimental hyperoxaluria: a biochemical approach with fucoidan J Pharm Pharmacol 2007;59(3):419-27
- Pucci ND, Marchini GS, Mazzucchi E, Reis ST, Srougi M, Evazian D, et al. Effect of phyllanthus niruri on metabolic parameters of patients with kidney stone: a perspective for disease prevention. Int Braz J Urol 2018;44(4):758-764. doi: 10.1590/S1677-5538.IBJU.2017.0521
- Nishiura JL, Campos AH, Boim MA, Heilberg IP, Schor N. Phyllanthus niruri normalizes elevated urinary calcium levels in calcium stone forming (CSF) patients. Urol Res 2004;32:362–366. doi: 10.1007/s00240-004-0432-8
- Robertson WG. Do "inhibitors of crystallisation" play any role in the prevention of kidney stones? A critique. Urolithiasis 2017;45(1):43-56. doi: 10.1007/s00240-016-0953-y.
- Freitas AM, Schor N, Boim MA. The effect of Phyllanthus niruri on urinary inhibitors of calcium oxalate crystallization and other factors associated with renal stone formation. BJU In. 2002;89(9):829-34
- Micali S, Sighinolfi MC, Celia A, De Stefani S, Grande M, Cicero AF, Bianchi G. Can Phyllanthus niruri affect the efficacy of extracorporeal shock wave lithotripsy for renal stones? A randomized, prospective, longterm study. J Urol 2006;176(3):1020-2
- Боев И.А. Антимикробная активность морских бурых водорослей. Наука и инновации XXI века. Материалы III Всероссийской конференции молодых ученых. 2016 Издательство: Сургутский государственный университет (Сургут). C. 105-107. [Boev I.A. Antimicrobial activity of marine brown algae. Science and innovation of the XXI century. Materials of the III All-Russian Conference of Young Scientists. 2016 Publisher: Surgut State University (Surgut). P. 105-107. (In Russian)].
- Cushnie TP, Lamb AJ. Recent advances in understanding the antibacterial properties of flavonoids Int. Antimicrob Agents. 2011. Vol. 38. P. 99 107
- Годовалов А.П., Быкова Л.П. Антимикробная активность производных некоторых растений. Современные научные исследования и разработки 2017;2(1):58-61 [Godovalov A.P., Bykova L.P. Antimicrobial activity of derivatives of some plants. Sovremennyye nauchnyye issledovaniya i razrabotki=Modern scientific research and development 2017;2(1);58-61] (In Russian)].
- Журишкина Е.В., Степанов С.И., Швецова С.В., Кульминская А.А., Лапина И.М. Сравнительный анализ влияния фукоидана из водорослей Fucus vesiculosis и фракций, полученных из него с помощью анионообменной хроматографии, на клетки HeLa G-63, Hep G2 и Chang liver. Цитология 2017;59(2): 148-155 [Zhurishkina Ye.V., Stepanov S.I., Shvetsova S.V., Kul'minskaya A.A., Lapina I.M. Comparative effect of fucoidan from alga fucus vesiculosus and its fractions, obtained by anion-exchange chromatography, on cell lines hela g-63, hep g2 and chang liver. Tsitologiya=Cytology 2017; 59(2):148-155 (In Russian)].
- Cumashi A, Ushakova NA, Preobrazhenskaya ME, D’Incecco A, Piccoli A, et al. A comparative study of the anti-inflammatory, anticoagulant, antiangiogenic and antiadhesive activities of nine different fucoidans from brown seaweeds. Glycobiology 2007;17(5):541-52.
- Coothan KV, Anthony J, Sreenivasan PP, Palaninathan V. Physico-chemical alterations of urine in experimental hyperoxaluria: a biochemical approach with fucoidan J Pharm Pharmacol 2007;59(3):419-27
- Veena CK, Josephine A, Preetha SP, Varalakshmi P, Sundarapandiyan R. Renal peroxidative changes mediated by oxalate: the protective role of fucoidan. Life Sci 2006;79(19):1789-95.
- The State Pharmacopoeia Committee of China Pharmacopoeia Commission of the People’s Republic of China, 2005, vol.1. Chemical Industry Press, Beijing
- Gohel MD, Wong SP. Chinese herbal medicines and their efficacy in treating renal stones. Urol Res 2006;34(6):365–372. doi: 10.1007/s00240-006-0068-y
- Jun Mi, Jianmin Duan, Jun Zhang, Jianzhong Lu, Hanzhang Wang и соавт. Evaluation of antiurolithic effect and the possible mechanisms of Desmodium styracifolium and Pyrrosiae petiolosa in rats. Urol Res 2012;40(2):151-61. doi: 10.1007/s00240-011-0401-y
Статья опубликована в журнале "Экспериментальная и клиническая урология" №3 2019, стр. 104-108













Комментарии