На сайте используются файлы cookie для анализа поведения пользователей и повышения качества работы ресурса. Продолжая использование сайта, вы подтверждаете своё согласие на применение cookie в соответствии с нашей политикой.
Согласен- ВКонтакте
- Telegram
- РћРТвЂВВВВВВВВнокласснРСвЂВВВВВВВВРєРСвЂВВВВВВВВ
53-летнему мужчине с жалобами на лихорадку, потерю веса до 15 кг, общим состоянием по ECOG 0, с опухолью почки 12 ˟ 9,5 см и опухолевым тромбом II (почти III) уровня в нижней полой вене для уменьшения массы тромба, первичной опухоли и операционного риска была предложена предоперационная таргетная терапия. Пациент дал согласие на назначение сорафениба, что привело к заметному уменьшению первичной опухоли почки и регрессии опухолевого тромба на 43%. Уменьшение размеров опухоли и регрессия тромба позволили выполнить резекцию левой почки. Патогистологические результаты показали, что часть опухоли была некротизирована. Через два года после начала предоперационной терапии сорафенибом пациент остается жив без признаков прогрессирования заболевания.
Введение
Циторедуктивная нефрэктомия (ЦН) с последующей терапией цитокинами доказано улучшает выживаемость пациентов с метастатическим почечно-клеточным раком (мПКР) . Однако некоторые пациенты не подходят для ЦН, метастаз- или тромбэктомии в связи с выраженностью заболевания. В последнее время ингибиторы тирозинкиназы (ИТК) использовались предоперационно у пациентов с первичным труднорезецируемым ПКР для облегчения выполнения операции за счет уменьшения размера опухоли . Таргетная терапия, в том числе сорафенибом, доказано уменьшает размер опухоли у пациентов с метастатическим раком почки по сравнению с цитокиновой терапией. На втором этапе исследования, сорафениб продемонстрировал скорейшее уменьшение размеров опухоли и улучшение качества жизни по сравнению с терапией цитокинами . Целью описания этого случая было изучение клинических результатов предоперационной таргетной терапии сорафенибом у пациентов с неоперабельным мПКР. Кроме того, мы проанализировали патогистологические изменения для определения влияния сорафениба на ткань опухоли.
История болезни
53-летний мужчина поступил с 6-месячной историей постепенного повышения температуры тела и потерей веса в 15 кг. С-реактивный белок сыворотки (СРБ) повышен до 17,2 мг/дл. История болезни без особенностей. Компьютерная томография (КТ) брюшной полости показала распространенную опухоль (12 ˟ 9,5 см), которая была клинически диагностирована как ПКР слева с опухолевым тромбом II (почти III) уровня в нижней полой вене, cT4N2M1 в соответствии с системой стадирования TNM .
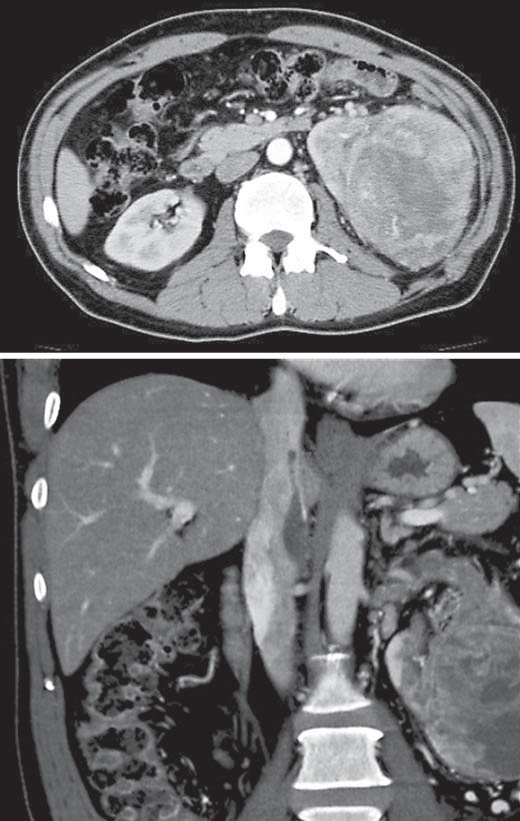
Рисунок 1: Компьютерная томограмма пациента до предоперационной терапии сорафенибом: 1 – первичная опухоль левой почки размером 12 ˟ 9,5 см; 2 – опухолевый тромб, простирающийся в нижнюю полую вену.
Общее состояние по European Cooperative Oncology Group (ECOG) и категория риска MSKCC были ECOG 1 и промежуточная, соответственно, кроме того в легких были обнаружены метастазы. Варианты лечения были обсуждены с пациентом, в частности, применение таргетной терапии для уменьшения опухоли и облегчения открытой левосторонней радикальной нефрэктомии. Была предложена возможность циторедукции тромба сорафенибом в рамках предоперационной терапии. Начиная с декабря 2008 года, сорафениб вводился в дозе 400 мг в день в течение 2 недель со снижением дозировки с учетом повышенного уровня СРБ и длительной лихорадки и с увеличением дозы до 400 мг дважды в день в течение 10 недель. Доза была уменьшена до 400 мг в день на 1 неделю из-за ладонно-подошвенного синдрома 2-й степени. Через тринадцать недель после начала предоперационной терапии сорафенибом компьютерная томография показала регрессию тромба нижней полой вены (НПВ) на 43%, а также уменьшение размера (11,4%) первичной опухоли . Ожидаемое снижение хирургической травмы из-за частичного ответа по результатам КТ и выраженное снижение уровня СРБ (1,7 мг/дл) позволили провести пациенту хирургическое лечение. Сорафениб был отменен на 2 недели, затем была проведена открытая радикальная нефрэктомия слева и тромбэктомия. Патогистологическое исследование: pT4N2Mx, атипия по Фурману 2-й степени, светлоклеточный ПКР с обширными некрозами. Интра- или послеоперационных осложнений, в том числе осложнений заживления ран или кровотечений, не наблюдалось. Через две недели после операции сорафениб был назначен в дозе 400 мг два раза в день в течение 6 месяцев. Сывороточный уровень СРБ был нормализован (0,20 мг / дл) через 9 недель после операции. КТ показала исчезновение примерно 20% легочных метастазов. В последующем пациент получал комбинированную терапию сорафенибом (400 мг в день) и ИФН - α (3 млн. МЕ 3 раза в неделю) в течение года. Через два года после начала предоперационной терапии сорафенибом пациент остается жив без признаков прогрессирования заболевания.
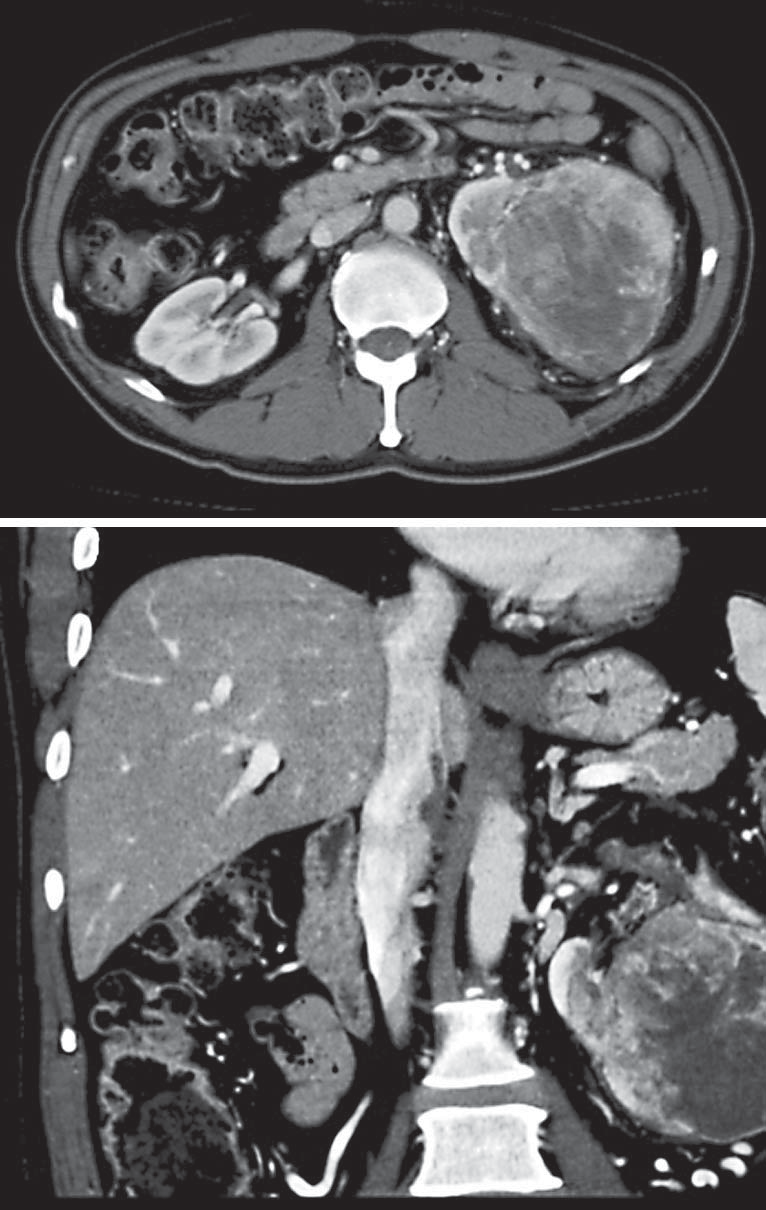
Рисунок 2: Компьютерная томограмма пациента после предоперационной терапии сорафенибом: 1 – на КТ заметно уменьшение размеров опухоли приблизительно на 11,4%; 2 – значительное уменьшение размеров опухолевого тромба, сократившегося до почечной вены.
Обсуждение
До утверждения таргетных агентов, включая сорафениб, большинство пациентов с поздними стадиями ПКР получали лечение цитокинами, такими как интерферон-α и ИЛ-2. Было доказано, что ЦН после терапии цитокинами улучшает выживаемость пациентов с метастатическим раком почки в эпоху цитокиновой терапии. Цитокиновая терапия, скорее всего, будет ограничена ввиду скромной общей частоты ответов и коротких интервалов до прогрессии. Кроме того, некоторые пациенты не могут перенести ЦН, метастаз- или тромбэктомии в связи с выраженным бременем болезни. Лишь один отчет показал противоопухолевый эффект неоадъювантной терапии цитокинами, включая IFNα-2b, но выживаемость была ограничена . В эпоху ИТК в качестве варианта лечения было предложено использование таргетной терапии до операции, в том числе неоадъювантной терапии, индукционной терапии и предоперационной терапии нерезектабельных/резектабельных первичных ПКР на основании имеющихся результатов клинических испытаний ИТК: два доклада показали уменьшение размеров опухоли в среднем на 14 и 24%, соответственно . Тем не менее, есть опасения, что минимальное сокращение не сможет увеличить резектабельность первичной опухоли. В недавнем докладе было показано значительное снижение размеров тромба в нижней полой вене после предоперационной терапии сунитинибом . Эти данные предполагают, что сокращение первичной опухоли при помощи ИТК может быть еще одним вариантом увеличения хирургической резектабельности. Кроме того, в нашем случае, после предоперационного назначения сорафениба заметно уменьшился тромб в НПВ, в силу чего сложность открытой радикальной нефрэктомии с тромбэктомией была снижена. Не отмечено послеоперационных осложнений, в том числе задержки заживления раны или кровотечения. Существует возможность того, что обширный некроз в первичной опухоли был вызван сорафенибом. В заключение, это исследование показывает, что регресс тромба в НПВ после предоперационной таргетной терапии сорафенибом дает несколько потенциальных преимуществ пациентам с неоперабельным первичным ПКР. Сорафениб в предоперационном режиме может сделать трудновыполнимую резекцию возможной.
Список литературы:
- Leibovich BC, Blute ML: Surgical management of renal cell carcinoma. Semin Oncol 2006; 33: 552-562.
- Wood CG: The role of cytoreductive nephrectomy in the management of metastatic renal cell carcinoma. Urol Clin North Am 2003; 30: 581–588.
- Cowey CL, Amin C, Pruthi RS, et al: Neoadjuvant clinical trial with sorafenib for patients with stage II or higher renal cell carcinoma. J Clin Oncol 2010; 28: 1502–1507.
- Shuch B, Riggs SB, LaRochelle JC, et al: Neoadjuvant targeted therapy and advanced kidney cancer: observations and implications for a new treatment paradigm. BJU Int 2008; 102: 692–696.
- Harshman LC, Srinivas S, Kamaya A, Chung BI: Laparoscopic radical nephrectomy after shrinkage of a caval tumor thrombus with sunitinib. Nat Rev Urol 2009; 6: 338–343.
- Bex A, van der Veldt AA, Blank C, et al: Neoadjuvant sunitinib for surgically complex advanced renal cell cancer of doubtful resectability: initial experience with downsizing to reconsider cytoreductive surgery. World J Urol 2009; 27: 533–539.
- Thomas AA, Rini BI, Lane BR, et al: Response of the primary tumor to neoadjuvant sunitinib in patients with advanced renal cell carcinoma. J Urol 2009; 181: 518–523.
- Escudier B, Szczylik C, Hutson TE, Demkow T, Staehler M, Rolland F, Negrier S, Laferriere N, Scheuring UJ, Cella D, Shah S, Bukowski RM. Randomized phase II trial of first-line treatment with sorafenib versus interferon Alfa-2a in patients with metastatic renal cell carcinoma. J Clin Oncol 2009; 27: 1280–1289.
- Sobin LH: TNM Classification of Malignant Tumors. Oxford, Wiley-Blackwell, 2009.
- Bex A, Horenblas S, de Gast GC: The timing of immunotherapy and nephrectomy in multimodality treatment of metastatic renal cell carcinoma. Technol Cancer Res Treat 2003; 2: 205–210.
- ВКонтакте
- Telegram
- РћРТвЂВВВВВВВВнокласснРСвЂВВВВВВВВРєРСвЂВВВВВВВВ






Комментарии