- ВКонтакте
- Telegram
- РћРТвЂВВВВВВВВнокласснРСвЂВВВВВВВВРєРСвЂВВВВВВВВ
С.Н. Калинина 1 , В.Н. Фесенко 1 , А.В. Никольский 2 , О.О. Бурлака 2 , Н.В. Марченко 2
1ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, Санкт-Петербург;
2СПб ГБУ
З «Александровская больница», Санкт-Петербург
Введение
Болезнь Пейрони, или фибропластическая индурация полового члена, в последние десятилетия вошла в число значимых проблем мужского здоровья. Болезнь Пейрони не представляет опасности для жизни пациента, но затрудняет ведение половой жизни, приводит к сексуальной несостоятельности мужчин, распаду семьи, выраженной депрессии.
Впервые болезнь Пейрони описана в 1743 г. Франсуа де ла Пейрони (1678–1747), придворным хирургом французского короля Людовика ХV. Несмотря на то что с этого времени прошло 275 лет, к настоящему времени нет консенсуса относительно причин развития болезни Пейрони, по-прежнему не до конца ясны ее этиология и патогенез [1, 2]. Остаются также спорными вопросы относительно используемой терминологии. В ряде случаев под фибропластической индурацией понимают заболевание с преимущественной локализацией патологического процесса в пещеристых телах полового члена, приводящее к его деформации во время эрекции. В других работах под этим подразумевают постепенное и малоболезненное уплотнение нескольких участков пещеристых тел, появление в них плотных соединительнотканных включений, приводящих к нарушению функции полового члена. Иногда болезнь Пейрони определяют как доброкачественное, медленно прогрессирующее заболевание неясной этиологии, характеризующееся образованием фиброзных экстракавернозных бляшек на белочной оболочке полового члена, приводящих к искривлению эрегированного полового члена и нарушению эректильной функции. В ряде исследований указывается, что болезнь Пейрони — это очаговый фиброз (рубцевание) белочной оболочки полового члена, приводящий к нарушению соотношения коллагеновых и эластических волокон, нарушению эластичности белочной оболочки и искривлению полового члена во время эрекции в том направлении, в котором белочная оболочка не нарушена. При последнем пересмотре МКБ-10 (2005) болезнь Пейрони и фиброз кавернозных тел полового члена объединены в одну нозологическую группу, относящуюся к пластической индурации полового члена.
На сегодняшний день распространенность болезни Пейрони оценивают среди всех взрослых мужчин в диапазоне от 3 до 8 % [3–5]. При этом отмечается, что заболевание может не всегда сопровождаться клинической симптоматикой, которая требует лечения. Частота возникновения фибропластической индурации полового члена увеличивается с возрастом пациентов [1]. Возможно, это связано с тем, что у пожилых мужчин эластичность тканей полового члена снижается, повышая риск микротравмирования тканей.
К наиболее распространенным теориям развития болезни Пейрони относятся следующие [6, 7].
- Теория микротравмы белочной оболочки полового члена: незначительный надрыв белочной оболочки с образованием небольшой гематомы, фибрина активизирует фибробласты и медиаторы воспаления. Заболевание начинается с острого воспалительного процесса между слоями белочной оболочки. Полный процесс замещения фибрина в белочной оболочке занимает 12–18 месяцев, когда полностью может сформироваться искривление.
- Эндокринная теория: развитие заболевания на фоне гормонального дисбаланса.
- Теория патологии соединительной ткани: отмечена связь с другими заболеваниями, характеризующимися патологией соединительной ткани (контрактура Дюпюитрена, склеродермия, плечелопаточный периартрит, дермомиозит, склероз ушных раковин). Хромосомные аномалии клеток, полученных из бляшек при болезни Пейрони, аналогичны таковым при контрактуре Дюпюитрена.
- Химическая теория: наличие связи между развитием болезни Пейрони и длительным приемом барбитуратов.
- Генетическая теория: частая выявляемость при болезни Пейрони антигенов II класса системы HLA: HLA-DR3 и HLA-DQW2, сопутствующих органоспецифическим аутоиммунным нарушениям и напоминающим ревматический процесс.
- Вирусная теория: фактор трансформации TGF-В1 (цитокин) усиливает синтез и накопление коллагена в кавернозной ткани полового члена и стимуляцию роста фибробластов, что ведет к снижению содержания оксида азота, гипоксии и повреждению эндотелия.
- Вегетативная теория: поражение вегетативной кавернозной иннервации в зоне дорсального сосудисто-нервного пучка.
Кроме того, в патогенезе болезни Пейрони имеет значение развитие фиброза белочной оболочки или кавернозной ткани, который может быть одной из причин эректильной дисфункции. Врожденные анатомические особенности полового члена (наличие тяжей соединительной ткани — хорд), заболевания уретры (гипоспадия, стриктура) могут повышать риск болезни Пейрони.
Вовлечение в процесс фасции Бука, перфорантных сосудов и дорсальных артерий полового члена приводит к нарушению механизма веноокклюзии и артериальной недостаточности полового члена, тогда необходимо выполнение динамической кавернозографии. В рубец чаще вовлекается дорсальная часть полового члена, а также латеральная и вентральная. В связи с отложением в уплотненных участках солей кальция они приобретают хрящевую консистенцию. Соединительнотканные бляшки появляются на тыльной поверхности одного или обоих кавернозных тел как плоское полигональное образование, которое растет вниз, вглубь, их может быть одно или несколько.
В диагностике болезни Пейрони применяют магнитно-резонансную или компьютерную томографию. Ультразвуковая доплерография полового члена может помочь оценить размеры и локализацию бляшек, кровоток в сосудах полового члена. Консервативное лечение показано на ранних стадиях заболевания и при отказе пациента от оперативного лечения [8–10]. Консервативное лечение обычно проводят в первый год от начала заболевания до наступления кальцификации бляшки и при искривлении полового члена менее 30–45 градусов. Используют гормональные препараты, биогенные стимуляторы, физиотерапевтические методы, ударно-волновую терапию, близкофокусную рентгенотерапию, верапамил, интерфероны, ингибиторы ФДЭ 5-го типа [11–13].
Целью настоящего исследования была оценка эффективности консервативного лечения болезни Пейрони.
Материалы и методы
Под наблюдением в Александровской больнице, являющейся базой кафедры урологии Северо-Западного государственного медицинского университета им. И.И. Мечникова, находились 27 мужчин в возрасте от 25 до 66 лет (средний возраст — 45,5 года), получавших консервативное лечение по поводу болезни Пейрони. Длительность заболевания составляла от 3 месяцев до 5 лет. Все пациенты были женаты. У 4 пациентов в анамнезе — контрактура Дюпюитрена, у 2 — компенсированный сахарный диабет. Пациенты предъявляли жалобы на умеренные боли в области полового члена, снижение адекватных, спонтанных эрекций, незначительные уплотнение в области тела, корня полового члена, небольшое искривление полового члена, что ухудшало качество их жизни.
Всем пациентам проводили общеурологическое обследование, выполняли общий анализ мочи, клинические и биохимические анализы крови, определяли уровень половых и гонадотропных гормонов, уровень простатспецифического антигена (ПСА) в сыворотке крови. Уровни половых и гонадотропных гормонов, глюкоза в сыворотке крови у наблюдаемых больных были в пределах нормы, уровень ПСА ниже 2 нг/мл. Также у всех пациентов исключены инфекции, передаваемые половым путем.
В комплексное обследование входило выполнение ультразвуковой доплерографии полового члена, при которой определяли скорость кровотока в кавернозных и дорсальных артериях и размеры бляшки. У наблюдаемых нами больных размеры бляшек полового члена не превышали 1,5 см в диаметре, а угол искривления полового члена был менее 45 градусов, что являлось критериями включения в исследование.
Всем больным назначали комбинированную терапию — симптоматическое, иммунологическое и физиотерапевтическое лечение. К последнему относились магнитолазерная терапия на область бляшек полового члена и ЛОД-терапия. При этом 15 пациентов (1-я группа) дополнительно получали препарат лонгидазу (внутримышечно по 3000 МЕ 1 раз в 3 дня, на курс 10 инъекций, с одновременным введением ректально свечей с лонгидазой в той же дозе, на курс 10 свечей). Локально этим пациентам наряду с магнитолазерной терапией назначали фонофорез с лонгидазой на область бляшек (10 сеансов). Остальные 12 больных (2-я группа) препарат лонгидазу не получали.
Пациентам обеих групп одновременно с магнитолазерной терапией проводили лечение на аппарате АМВЛ-01, создающем локальное отрицательное давление (ЛОД) при 2 атм в колбе, вызывая эрекцию с длительностью воздействия на половой член в течение 10–20 минут (рис. 1), количество ЛОД-терапии составляет 10 процедур. При выраженной эректильной дисфункции пациентам назначали ингибиторы ФДЭ 5-го типа в индивидуально подобранных дозах. Результаты лечения оценивали через 6 и 12 месяцев от его начала.
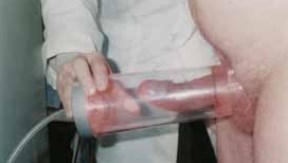
Рис. 1. Диагностика искривления полового члена на аппарате АМВЛ-01 (аппарат вакуумно-лазерный терапевтический урологический) у больного А., 54 года, с болезнью Пейрони. Локальное отрицательное давление с максимальным разряжением в колбе воздействует на баро- и терморецепторы кожи полового члена, усиливает микроциркуляцию в его сосудах. Выявлено незначительное искривление (угол искривления — 30 градусов) полового члена
Результаты исследований были обработаны общепринятыми статистическими методами с вычислением среднего значения, доверительного интервала при доверительной вероятности α = 0,95 (вероятность ошибки p < 0,05). Статистическую обработку материала осуществляли с использованием пакета программ прикладной статистики SPSS12.0.
Результаты
При выполнении ультразвуковой доплерографии полового члена у 16 из 27 обследованных пациентов были выявлены сосудистые изменения, у 8 (50 %) из них проявляющиеся веногенными компенсированными и субкомпенсированными эректильными дисфункциями (рис. 2, 3). У остальных 11 больных этой группы признаков сосудистых изменений не обнаружено (табл. 1).
Таблица 1. Сосудистые нарушения у больных с болезнью Пейрони по данным ультразвуковой доплерографии полового члена
| Группа больных | Сосудистые нарушения по данным ультразвуковой доплерографии полового члена | |
| выявлены | не выявлены | |
| 1-я (n = 15) | 9 | 6 |
| 2-я (n = 12) | 7 | 5 |
| Всего (n = 27) | 16 (59,3 %) | 11 (40,3 %) |
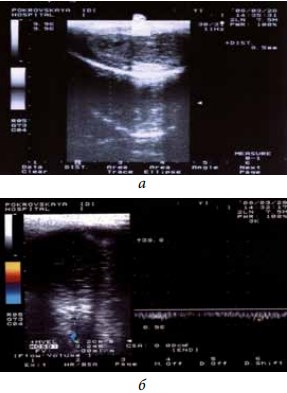
Рис. 2. Ультразвуковая доплерография полового члена больного Д., 36 лет, с болезнью Пейрони и веногенной эректильной дисфункцией: а — в дистальной части полового члена бляшки от 1–2 до 8,5 мм; б — дорсальная вена не спалась, кровоток по ней определяется в течение всего исследования до 30 мл/мин. Проба Вальсальвы положительная
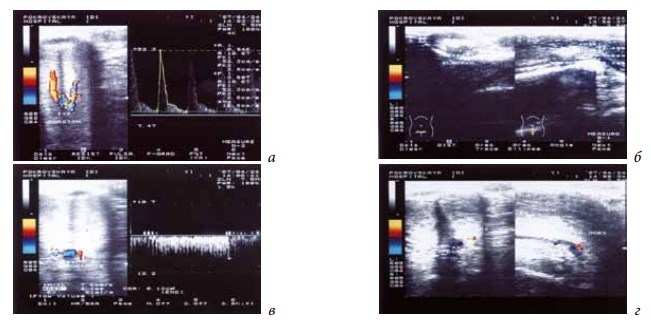
Рис. 3. Ультразвуковая доплерография полового члена больного Т., 55 лет, с болезнью Пейрони и веногенной эректильной дисфункцией. У больного выявлена контрактура Дюпюитрена: а — аномалия строения кавернозных артерий: в ножке полового члена кавернозные артерии имеют анастомоз; б — бляшки в кавернозных телах (выделена бляшка размером 11,4 × 4,6 × 9,2 мм), деформирующие половой член; в и г — неспадение дорсальной вены — признак веногенной эректильной дисфункции
У всех 27 больных до начала лечения максимальные размеры бляшек были менее 1,5 см. При этом у 13 (48,1 %) из них размеры бляшек были более 0,5 см в диаметре, у 6 (22,2 %) — более 1 см, у остальных 8 (29,6 %) пациентов размеры бляшек были менее 0,5 см в диаметре (табл. 2). У больных 1-й группы максимальные размеры бляшек менее 0,5 см, более 0,5 см и более 1 см были у 5, 7 и 3 больных соответственно, во 2-й группе — у 3, 6 и 3 больных. Через 6 месяцев после начала комплексного комбинированного лечения с лонгидазой почти в 2 раза уменьшилось число больных, у которых бляшки были более 0,5 см (до лечения — у 13 больных, после лечения — у 7 пациентов). В 4 раза уменьшилось число пациентов с бляшками размером менее 0,5 см. Отсутствие бляшек через 6 месяцев после начала лечения зафиксировано у 8 (53,3 %) больных 1-й группы и 4 (33,3 %) больных 2-й группы, а через 12 месяцев — соответственно у 11 (73,3 %) и 6 (41,6 %) пациентов (см. табл. 2).
Таблица 2. Результаты лечения пациентов с болезнью Пейрони (n = 27)
| Группа больных |
Максимальные размеры бляшек по данным ультразвуковой доплерографии, см | Отсутствие бляшек через 6 и 12 месяцев, п (%) | ||||||||
| до лечения | через 6 месяцев после лечения | через 12 месяцев после лечения | ||||||||
| < 0,5 | > 0,5 | > 1 | < 0,5 | > 0.5 | > 1 | < 0.5 | > 0,5 | > 1см | ||
| 1-я (и = 15) | 5 | 7 | 3 | 1 | 4 | 2 | - | 3 | 1 | 8 (66,6 %)/ 11 (73,3 %) |
| 2-я (я = 12) | 3 | 6 | 3 | 2 | 4 | 2 | 1 | 3 | 2 | 4 (33,3 %)/ 6 (50 %) |
| Всего (и = 27) | 8 | 13 | 6 | 2 | 7 | 4 | 1 | 6 | 3 | 14 (51,8 %)/ 17 (63 %) |
Результаты исследования показали высокую эффективность консервативной комбинированной терапии на ранней стадии заболевания, патогенетическую обоснованность лечения и его хорошую переносимость. При этом в группе больных, получавших лонгидазу, эффективность лечения оказалась выше.
Выводы
Таким образом, консервативная терапия при болезни Пейрони эффективна у пациентов на ранних стадиях заболевания, при умеренной девиации полового члена и размерах бляшек до 1,5 см. Включение в комплексную терапию препарата лонгидаза повышает эффективность проводимого лечения.
Литература
- Щеплев П.А., Гарин Н.Н., Данилов И.А., и др. Болезнь Пейрони. – М.: ИД «АБВ-пресс», 2012. [Shheplev PA, Garin NN, Danilov IA, et al. Bolezn’ Pejroni. Moscow: ABV-press; 2012. (In Russ.)]
- Урология. Российские клинические рекомендации / Под ред. Ю.Г. Аляева, П.В. Глыбочко, Д.Ю. Пушкаря. – М.: ГЭОТАРМедиа, 2015. [Urologija. Rossijskie klinicheskie rekomendacii. Ed. by Yu.G. Aljaev, P.V. Glybochko, D.Yu. Pushkar. Moscow: GEOTAR-Media; 2015. (In Russ.)]
- Sommer F, Schwarzer U, Wassmer G, et al. Epidemiology of Peyronie’s disease. International Journal of Impotence Research. 2002;14(5):379-383. doi: 10.1038/sj.ijir.3900863.
- La Pera G, Pescatori ES, Calabrese M, et al. Peyronie’s disease: prevalence and association with cigarette smoking: a multicenter population-based study in men aged 50-69 years. European Urology. 2001;40(5):525-530. doi: 10.1159/000049830.
- Щеплев П.А., Данилов И.А., Колотинский А.Б., и др. Клинические рекомендации. Болезнь Пейрони // Андрология и генитальная хирургия. – 2007. – № 1. – С. 55–58. [Shheplev PA, Danilov IA, Kolotinskij AB,etal. Klinicheskierekomendacii. Bolezn’ Pejroni. Andrologija i genital’naja hirurgija. 2007;(1):55-58 (In Russ.)]
- Калинина С.Н., Тиктинский О.Л., Новиков И.Ф. Фибропластическая индурация полового члена(болезнь Пейрони): Пособие для врачей-урологов. – СПб.: Изд-во СПбМАПО, 2009. [Kalinina SN, Tiktinskij OL, NovikovIF. Fibroplasticheskajainduracija polovogo chlena (bolezn’ Pejroni). Posobie dlja vrachej-urologov. Saint Petersburg: SPbMAPO; 2009. (In Russ.)]
- Тиктинский О.Л., Калинина С.Н., Михайличенко В.В. Андрология. – М.: МИА, 2010 [Tiktinskij OL, Kalinina SN, Mihajlichenko VV. Andrologija. Moscow: MIA; 2010. (In Russ.)]
- Мазо Е.Б., Муфагед М.Л., Иванченко Л.П., и др. Консервативное лечение болезни Пейрони в свете новых патогенетических данных // Урология. – 2006. – № 2. – С. 31–37 [Mazo EB, Mufaged ML, Ivanchenko LP, et al. Konservativnoe lechenie bolezni Pejroni v svete novyh patogeneticheskih dannyh. Urologiia. 2006;(2):31-37. (In Russ.)]
- Adeniyi AA, Goorney SR, Pryor JP, Ralph DJ. The Lue procedure: an analysis of the outcome of Peyronie’s disease. BJU Int. 2002;89(4):404-408. doi: 10.1046/j.1464-4096.2001.01896.x.
- Levine LA, Goldman KE, Greenfild JM. Experience with intraplaque injection of Verapamil for Peyronie’s disease. J Urol. 2002;168(2):621-625. doi: 10.1097/00005392-200208000-00045.
- Москалева Ю.С., Остапченко А.Ю., Корнеев И.А. Болезнь Пейрони // Урологические ведомости. – 2015. – Т. 5. – № 4. – С. 30–35 [Moskaleva YuS, Ostapchenko AYu, Korneev IA. Peyronie’s disease. Urologicheskie vedomosti. 2015;5(4):30-35. (In Russ.)]
- Сокольщик М.М., Гагарина С.В., Петрович Р.Ю., и др. Лечение эректильной дисфункции у пациентов с пластической индурацией полового члена // Урология. – 2008. – № 1. – С. 41–44. [Sokol’shhik MM, Gagarina SV, Petrovich RJu, et al. Lechenie jerektil’noj disfunkcii u pacientov s plasticheskoj induraciej polovogo chlena. Urologiia. 2008(1):41-44. (In Russ.)]
- Lebret T, Loison G, Herve JM, et al. Extracorporeal shock wave therapyin thetreatment of Peyronie’s disease:experience with standard lithotripter (Siemens-Multiline). Urology. 2002;59(5):657-661. doi: 10.1016/s0090-4295(02)01527-3.
Статья опубликована в журнале "Урологические ведомости" 2018 №1, стр. 5-10
Тематики и теги
- ВКонтакте
- Telegram
- РћРТвЂВВВВВВВВнокласснРСвЂВВВВВВВВРєРСвЂВВВВВВВВ











Комментарии