А.Г. Мартов, Д.В. Ергаков, А.Б. Новиков, А.Б. Манцаев
Кафедра урологии и андрологии ФМБЦ им. А. И. Бурназяна ФМБА РФ, Москва, Россия ГКБ им. Д. Д. Плетнёва, Москва, Россия
Методика внутреннего дренирования верхних мочевыводящих путей (ВМП) с помощью подвесных мочеточниковых катетеров типа «стент» была впервые описана и применена более 30 лет назад и в настоящее время широко используется при различных урологических заболеваниях. Преимуществами данной методики дренирования ВМП, которые позволили широко использовать ее как для профилактики, так и для ликвидации суправезикальной обструкции, являются относительная простота установки внутреннего стента и возможность длительного поддержания адекватного пассажа мочи по ВМП без контакта катетера с внешней средой.
Основными показаниями к применению внутреннего дренирования ВМП являются: 1) внутрипросветное отведение мочи при обструкции ВМП, обусловленной камнем мочеточника или почки, опухолью (мочеточника, забрюшинного пространства, прилежащих органов), стриктурой ВМП, ретроперитонеальным фиброзом; 2) визуализация мочеточника при открытых оперативных и видеоэндоскопических (лапароскопия, ретроперитонеоскопия) вмешательствах путем предоперационного стентирования; 3) шинирование и дренирование мочеточника и лоханочно-мочеточникового сегмента (ЛМС) после эндотомий, реканализации и наложения анастомозов; 4) достижение пассивной дилатации мочеточника перед уретеропиелоскопией и с целью профилактики образования «каменной дорожки» и обструкции после дистанционного ударно-волнового дробления камней и др. [1, 2].
Различные авторы описали осложнения внутреннего дренирования ВМП, которые помимо инфекционно-воспалительных и обструктивных, включают в себя т.н. «стент- зависимые симтомы», часть из которых, помимо болей в области почки, проявляется типичными симптомами нарушения функции нижних мочевыводящих путей (СНМП) – дизурией, странгурией, поллакиурией, болями в надлобковой области и др. [1, 3–6]. Достаточно широко освещены причины и характер осложнений применения внутренних мочеточниковых стентов и, тем не менее, большинство авторов, сообщая об осложнениях, требующих смены, коррек-ции положения или удаления катетера, уделяют недостаточное внимание субъективным симптомам, характеризующим индивидуальную переносимость стентов. Не существует также общепринятых установленных и утвержденных критериев объективной оценки данных симптомов с учетом их влияния на «качество жизни» и социальную адаптацию пациентов. В то же время имеется много публикаций об успешном применении α1-адреноблокаторов в терапии пациентов с СНМП, обусловленных различными урологическими заболева- ниями [7, 8].
Целью данной работы являлось изучение влияния терапии тамсулозином (Омник, капсулы) на качество жизни и «стент-зависимые симптомы» у пациентов с внутренними стентами.
Нами были проспективно отобраны 135 пациентов (66 мужчин, 69 женщин в возрасте от 19 до 74 лет (в среднем 47,3 года), которым по тем или иным причинам (МКБ, стриктура ЛМС и мочеточника и др.) было произведено стентирование мочеточника. Всем пациентам были установлены одинаковые внутренние стенты типа «pig tail» (с полным проксимальным и дистальным завитком) из полиуретана, размером №6F (по шкале Шарьера), произведенные одной и той же компанией. Длина стента определялась в зависимости от роста пациента и на основании экскреторных урограмм. Правильность стояния стента определялась на основании рентгенологического и ультразвукового обследований. Длительность стентирования у всех пациентов была более месяца и составила от 32 до 47 дней (в среднем 38 дней).
Критериями исключения из исследования являлись: неправильный выбор длины стента (слишком короткий, слишком длинный), неправильная его установка (отсутствие полностью сформированного дистального или проксимального завитка), неадекватное его функционирование (пиелоэктазия), выраженная мочевая инфекция (бактериурия выше 105 КОЕ в мл), необходимость кратковременного или слишком длительного стентирования мочеточника, длительное и систематическое использование α-адреноблокаторов или анальгетиков, наличие симптоматической доброкачественной гиперплазии простаты (ДГПЖ) с показателем IPSS более 8 или хронического простатита (у мужчин), хронического цистита (у женщин).
Все пациенты подписали информированное согласие для участия в исследовании. Исследование носило односторонний слепой характер, т.е. лечащие врачи и пациенты знали о приеме α-адреноблокатора, а исследователи, которые получали и интерпретировали полученные данные, не были информированы о том, получает ли конкретный пациент α-адреноблокатор.
Случайным образом пациенты были рандомизированы в 2 группы. Первая группа больных (n=65) принимала после установки стента тамсулозин (Омник) в дозе 0,4 мг однократно в сутки в сочетании с курсом противовоспалительной терапии, включавшим в себя прием фторхинолона (норфлоксацин 400 мг дважды в сутки) в течение 7 дней с последующим переходом на уроантисептики, и спазмолитической терапии по потребности. Средняя длительность приема тамсулозина на данном этапе исследования составила 38 дней. Вторая группа пациентов (n=70) не получала α-адреноблокатора. Терапия пациентов с симптомами, связанными с наличием стента, заключалась в проведении аналогичной с первой группой противовоспалительной и спазмолитической терапии.
Спустя две недели (в среднем 15 дней) после установки стента пациенты проходили первый контрольный осмотр в амбулаторном порядке, который включал в себя ультразвуковое исследование, контроль лабораторных данных и, по показаниям, обзорную урографию (при подозрении на миграцию стента), а также заполнение специального опросника и визуальной аналоговой шкалы симптомов. В данные сроки удалось обследовать 81 (60%) пациента (группа 1 – 47 пациентов, группа 2 – 34 пациента), остальные по различным причинам не смогли явиться на это промежуточное обследование, однако не были исключены из окончательного анализа, т.к. прошли обследование при удалении стента.
Через 32–47 (в среднем 38) дней от момента установки стента всем 135 пациентам проведена цистоскопия и удаление стента. Перед манипуляцией пациенты также заполняли опросник и визуальную аналоговую шкалу симптомов.
В последующем через 1–1,5 месяца (в среднем 34 дня) после удаления внутреннего стента больным назначалось контрольное обследование и заполнение опросников для оценки эффективности лечения. При этом больные 1-й группы продолжали принимать тамсулозин в той же дозировке. На данном этапе обследованы 64 пациента, остальные на контрольный осмотр без стента не явились и были исключены из окончательного анализа. Данные 64 пациентов включали в себя 28 больных из 1-й группы и 36 пациентов из 2-й группы.
Дизайн исследования был спланирован таким образом, чтобы максимально объективизировать субъективную оценку пациентами своих СНМП, связанных с наличием стента, а также проследить зависимость выраженности этих симптомов от терапии тамсулозином.
На протяжении всего исследования проводилась регистрация побочных эффектов, связанных с приемом препарата.
С целью объективизации степени выраженности симптомов, возникающих у пациентов при наличии внутреннего мочеточникового стента, мы произвели анкетирование 135 пациентов с помощью специальной анкеты –опросника. Больным предлагалось ответить на ряд вопросов, характеризующих интенсивность симптоматики, обусловленной наличием стента в различные сроки внутреннего дренирования ВМП. Симптоматика оценивалась с 5–7-х суток дренирования почки, что позволило исключить ее связь с перенесенной операцией и дренированием мочевого пузыря уретральным катетером. Выраженность симп-томатики оценивалась самими пациентами по 3-балльной шкале и фиксировалась ими в специальной анкете на 5–14-е и 15–30-е сутки после установки стента. Оценивали наличие и степень выраженности следующих симптомов: боли в области мочевого пузыря, боли в области почки в покое и после мочеиспускания, гематурия, дневная и ночная поллакиурия. Кроме того, больным предлагалось оценить степень выраженности затруднений в быту, на работе и в половой жизни, обусловленных наличием стента (см. таблицу).
Таблица. Анкета для оценки степени выраженности стент-зависимых симптомов
|
№№ Вопросов |
Ответы на 5–14 день |
Ответы на 15–30 день |
|---|---|---|
|
№1 . Боли в области мочевого пузыря ? |
0 1 2 3 |
0 1 2 3 |
|
№2 . Боли в области почки в покое ? |
0 1 2 3 |
0 1 2 3 |
|
№3. Боли в области почки после мочеиспускания ? |
0 1 2 3 |
0 1 2 3 |
|
№4 . Учащение мочеиспускания ? |
0 1 2 3 |
0 1 2 3 |
|
№5 . Примесь крови в моче ? |
0 1 2 3 |
0 1 2 3 |
|
№6 . Ночные позывы на мочеиспускание ? |
0 1 2 3 |
0 1 2 3 |
|
№7 . Затруднения в быту или на работе ? |
0 1 2 3 |
0 1 2 3 |
|
№8 . Затруднения в половой жизни ? |
0 1 2 3 |
0 1 2 3 |
Ответы: 0 – нет, 1 – незначительные, 2 – умеренные, 3 – выраженные.
Таким образом, максимально выраженная симптоматика позволяла набрать пациенту максимальную сумму в 24 балла, отсутствие симптоматики – 0 баллов.
Для субъективной оценки состояния своего организма пациенты во время лечения заполняли визуальную аналоговую шкалу, которая представляет собой 20 см вертикальную шкалу от 0 (плохое состояние) до 100 (хорошее состояние). Визуальная аналоговая шкала заполнялась через 2 недели после установки стента, перед удалением стента и через 1 месяц после удаления стента.
Все 135 пациентов закончили основную часть исследования, обе группы были разделены случайным образом, так что не было существенных межгрупповых различий по возрастно-половым и клиническим характеристикам пациентов. В послеоперационном периоде наиболее частым осложнением являлся острый пиелонефрит, который отмечен у больных из 1-й группы в 8 (12%) случаях и у 9 (13%) пациентов из 2-й группы. Коррекции положения стента не потребовалось ни в одном из случаев. Контрольное обследование перед удалением внутреннего стента не выявило бактериурии при микробиологическом исследовании мочи.
Оценка «стент-зависимых симптомов» производилась нами к концу 2-й недели после установки стента, перед удалением стента и через 1 месяц после удаления стента. Результаты оценки представлены на рис. 1. При проведении сравнительного анализа было отмечено, что к концу 2-й недели перед удалением стента и через 1 месяц после его удаления выраженность «стент-зависимых симптомов» была статистически достоверно больше у пациентов 2-й группы по сравнению с 1-й группой. При детализации ответов на вопросы было выявлено, что основные межгрупповые различия связаны с ответами на вопросы № 1, 3, 4, 6, 7 и 8 (рис. 2), т.е. без вопросов №7–8, это в основном вопросы, отражающие СНМП.
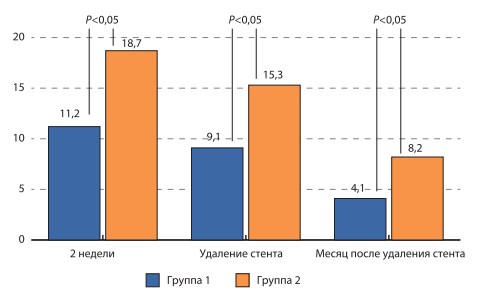
Рис. 1. Диаграмма оценки «стент-зависимых симптомов» в баллах (шкала ординат) в зависимости от терапии и дизайна исследования (объяснения в тексте)
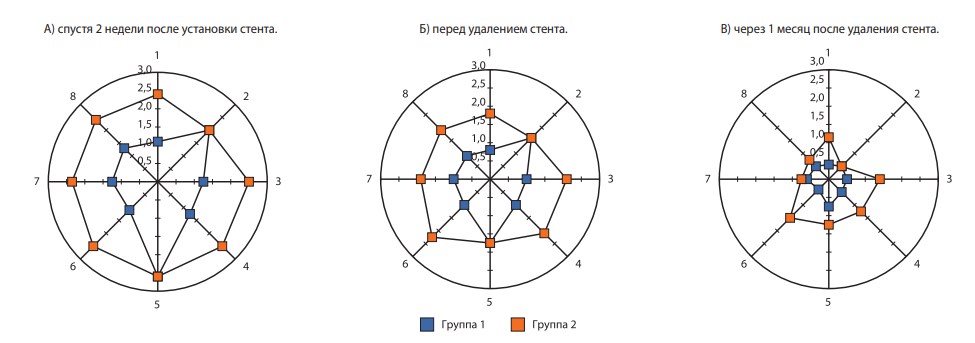
Рис. 2. Диаграммы детализации ответов на вопросы анкеты по оценке «стент-зависимых симптомов». По оси ординат цифровое обозначение выраженности симптоматики (ответы 0, 1, 2, 3), по кругу – номера вопросов (№1–№8)
Несмотря на то что вопросы № 7 и 8 в основной анкете направлены на изучение оценки качества жизни пациентов, нами была проведена оценка самочувствия пациента по визуальной аналоговой шкале. Данные представлены на рис. 3. По данным сравнительной оценки показателей визуальной аналоговой шкалы статистическая достоверность межгрупповых отличий была отмечена через 2 недели после установки стента и перед его удалением. Через 1 месяц после удаления стента показатели визуальной аналоговой шкалы статистически не отличались друг от друга.
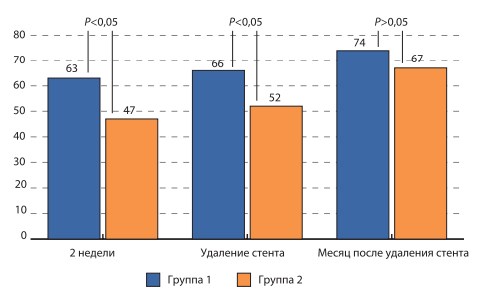
Рис. 3. Диаграмма визуальной аналоговой шкалы субъективной оценки симптоматики у пациентов с внутренними стентами в баллах (по оси ординат) в зависимости от терапии и дизайна исследования (объяснения в тексте)
За время исследования нами не было отмечено побочных эффектов, связанных с приемом тамсулозина, которые бы послужили причиной отмены препарата и выхода больного из исследования.
Симптомы, связанные с наличием стента включают в себя ирритативную симптоматику со стороны нижних мочевыводящих путей (боли в надлобковой области, позывы на мочеиспускание, учащенное моче-испускание, ночная поллакиурия), боли в поясничной области и другие симптомы, включающие в себя пузырно-мочеточниковый рефлюкс, обострение инфекционно- воспалительных заболеваний мочеполовой системы (пиелонефрит, цистит, простатит, орхоэпидидимит), гематурию. Помимо вышеперечисленных состояний, многие пациенты отмечали невозможность осуществлять обычную социальную и бытовую активность, испытывали депрессию и тревогу [9–12]. Традиционно для терапии пациентов со «стент-зависимыми симптомами» применяется противовоспалительная, спазмолитическая и анальгетическая терапия. Удачный и длительный опыт применения α-адреноблокаторов в терапии пациентов с расстройствами мочеиспускания, вызванных ДГПЖ, хроническим простатитом и камнями терминального отдела мочеточника явился предпосылкой для данного исследования, направленного на изучение эффективности тамсулозина в терапии пациентов с ирритативными симптомами, вызванными наличием внутреннего стента.
Патофизиология стент-зависимой и, в частности ирритативной симптоматики, остается до конца не изученной. R. Thomas считает, что часть симптомов связана с развитием пузырно-лоханочного рефлюкса, когда при мочеиспускании повышается внутрипузырное давление и в результате градиента давления между полостью мочевого пузыря и лоханкой моча забрасывается в почку [13]. Однако многие пациенты испытывают данные симптомы и при наличии специальных антирефлюксных стентов.
Ряд урологов считают, что ирритативная симптоматика может быть связана с формой пузырного завитка стента и материалом, из которого он изготовлен (твердый-мягкий). За последнее время проделана большая работа по улучшению дизайна дистального завитка стента для облегчения СНМП . Большое внимание уделяется также усовершенствованию материалов, из которых изготовлен стент. Однако исследование H.B. Joshi и соавт. [14] не выявило влиянияматериала из которого он сделан на качество жизни пациентов. Продолжаются исследованиястентов из биологически инертного рассасывающегося материала с тем,чтобы избежать необходимость выполнения в последующем цистоскопии для его удаления. К сожалению, на сегодняшний день «идеальный стент» не изготовлен. Такой стент должен полностью самостоятельно рассасываться, не покрываться биопленками микроорганизмов, не инкрустироваться и не вызывать симптомов раздражения со сторо- ны мочевого пузыря и, в то же время быть удобным для его установки в ВМП (быть достаточно твердым) [13, 14].
A. Rаne и соавт. [15] в своей работе доказывают отсутствие влияния техники установки внутреннего стента в ВМП на развитие «стент-зависимых ирритативных симптомов» и предполагают, что решающим фактором в их возникновении может являться длина пузырного конца стента. Чем он более длинный, тем сильнее выраженность симптомов раздражения. Тем не менее авторы не приводят статистически подкрепленных доказательств своих выводов. Дальнейшие детальные исследования должны уточнить, влияет ли длина пузырного конца стента на выраженность «стент-зависимой симпто- матики». Учитывая вышеприведенные данные, мы в своей работе у всех пациентов использовали стенты, состоящие из одного материала – полиуретана, и имеющие один размер – 6F. Длина стента определялась нами индивидуально с учетом роста пациента и для исключения влияния на ирритативную симптоматику неправильно расположенного стента (когда имелся большой пузырный завиток), мы исключали подобных больных из исследования, также как и пациентов с выяв-ленной в процессе лечения миграцией стента.Весьма показательной для оценки выраженности «стент-зависимой симптоматики» является работа D.T. Beiko и соавт. [16], которые для облегчения страданий пациентов вводили им внутрипузырно такие препараты, как кетопрофен, оксибутинин, лидокаиновые гели. На наш взгляд, терапевтическое значение такого лечения с позиции благоприятного соотношения польза/риск весьма спорно, однако данная работа наглядно показывает возможную степень выраженности «стент-зависимых симптомов». По данным авторов, инстилляции с кетопрофеном наиболее эффективны в терапии пациентов с данными расстройствами.
Влияние инфекции при внутреннем дренировании мочевыводящих путей на выраженность «стент-зависимой симптоматики» изучено довольно хорошо [1, 2, 9]. Для исключения влияния мочевой инфекции мы проводили бактериологический контроль мочи на протяжении всего исследования и пациенты со значимой бактериурией исключались из дальнейшего анализа.
Выбор анкеты – опросника для оценки пациентами своих жалоб был затруднен в связи с необходимостью адаптации к русскому языку вопросов из таких известных анкет, как USSQ (Ureteric stent symptom questionnaire) [10] и EQ-5D (European quality of life 5-dimension questionnaire) [12]. Кроме того, данные анкеты являются чрезмерно громоздкими и сложными для применения в повседневной практике. В связи с этим мы разработали адаптированную анкету,приспособленную для более удобной работы и лучшего восприятия на русском языке [1]. Достоинствами анкеты является ее простота, доступность для восприятия пациентами и легкость оценки полученных данных. Помимо данной анкеты пациенты заполняли визуальную аналоговую шкалу для интегральной субъективной оценки своего самочувствия, что в ряде наблюдений позволяло нам более объективно судить о достоверности оценки пациентами своих жалоб.
Обоснованием для назначения α-адреноблокаторов для терапии «стент- зависимых» симптомов является их доказанная эффективность в терапии ирритативных симптомов, вызванных другими урологическими заболеваниями [7, 17]. Несмотря на то что эффективность современных α-адреноблокаторов приблизительно одинакова, тамсулозин является одним из самых безопасных и комплаэнтных препаратов, поэтому он и был выбран для исследования. Тамсулозин является суперселективным антагонистом α-адренорецепторов, расположенных в простатическом отделе уретры, шейке мочевого пузыря, дистальной части мочеточников. Механизм влияния тамсулозина на «стент-зависимые симптомы» связан, по нашему мнению, с реализацией эффектов блокирования α-адренорецепторов в данных зонах, что позволяет снизить сопротивление шейки мочевого пузыря при мочеиспускании, понизить внутрипузырное давление, улучшить кровообращение в стенке мочевого пузыря и расширить дистальную треть мочеточника. Таким образом удается существенным образом снизить выраженность учащенного мочеис-пускания, ночную поллакиурию, позывы на мочеиспускание, боли над лоном, что приводит в конечном итоге к суммарному улучшению самочувствия пациентов при оценке «стент-зависимых симптомов» по визуальной аналоговой шкале. Так, по нашим данным, добавление тамсулозина к проводимой стандартной противовоспалительной и спазмолитической терапии уже ко второй неделе после стентирования привело к снижению суммарной симптоматики на 33% (11,2 против 18,7 баллов) по сравнению с группой больных, получавших только стандартное лечение. Схожие данные, свидетельствующие об объективности оценки пациентами своих жалоб, были получены по данным сравнения визуальной аналоговой шкалы (63% против 47%). Выраженность данных различий несколько снижается к моменту удаления стента и составляет соответственно 9,1 балла в 1-й и 15,3 балла во 2-й группе как по данным анкетирования, так и по данным визуальной аналоговой шкалы (66% против 52%), т.е. на протяжении всего срока стентирования применение тамсулозина позволяет статистически достоверно улучшить СНМП, связанные с наличием стента. После удаления стента применение тамсулозина также позволяет улучшить самочувствие больных за счет более быстрого и более полного устранения данных симптомов. Через 1 месяц после удаления стента межгрупповые различия не были статистически достоверными как при оценке данных анкет, так и по данным визуальной аналоговой шкалы, однако пациенты из 1-й группы в целом имели лучшие показатели (4,1 против 8,2 балла и 74% против 67% соответственно). Безопасность приема тамсулозина подтверждена в нашем исследовании отсутствием побочных эффектов, связанных с его приемом и тем, что ни один пациент не выбыл из исследования в связи с отказом от приема препарата.
ЛИТЕРАТУРА
- Зенков С.С. Внутреннее дренирование верхних мочевых путей. Дисс. к.м.н., 1998.
- Мартов А.Г., Долгушин Б.И., Меринов Д.В. и др. Стентирование для восстановления проходимости верхних мочевыводящих путей. В книге: Сосудистое и внутриорганное стентирование. Руководство. М., 2004. Глава 15. с. 326–43.
- Ringel A., Richter S., Shalev M., Nissenkom I. Late complications of urereral stents. Eur. Urol. 2000;38:41–4.
- Damiano R., Oliva A., Esposito C., De Sio I., Autorino R., D'Armiento M. Early and late complications of double pigtail uteteral stent. Urol. Tnt. 2002;69:136–40.
- Lee C., Kuskowski M., Premoli J., Skemp M. Monga M. Randomized evaluation of ureteral stents using validated symptom questionnaire. J. Endourol. 2005;19:990–3.
- Deliveliotis C., Chrisofos M., Gougousis E., Papatsoris A., Dellis A., Varkamkis I.M. Is there a role for alpha-blockers in treating double-J related symptoms? Urology. 2006;67:35–9.
- Michel M.C., de la Rosette J.J. Efficacy and safety of tamsulosin in the treatment of urological diseases. Expert. Opin Pharmacother. 2004;5:151–60.
- Autorino R., De Sio M., Damiano R., et al. The use of tamsulosin in the medical treatment of ureteral calculi: Where do we stand? Urol. Res. 2005;33:460–4.
- Paz A., Amiel G.D., Pick N., et al. Febrile complications following insertion of 100 double J-ureteral stents. J. Endourol. 2005;19:147–50.
- Joshi H.B., Newns N., Stainhorpe A., et al. Ureteral stent symptom questionnaire:development and validation of multidimensional quality of life measure. J. Urol. 2003;169:1060–4.
- Nabi G., Cook J., N’Dow J., et al. Outcomes of stenting after uncomplicated ureteroscopy: systematic review and meta-analysis. BMJ. 2007;334–572.
- Damiano R., Autorino R., De Sio M., et al. Effect of Tamsulosin in Preventing Ureteral Stent-Related Morbidity: A Prospective Study. J. Endourol. 2008;22(4):651–5.
- Thomas R. Indwelling ureteral stents: Impact of material and shape on patient comfort. J. Endourol. 1993;7:137–40.
- Joshi H.B., Chitale S.V., Nagarajan M., et al. A prospective randomized single-blind comparison of ureteral stent composed of firm and soft polymer. J. Urol. 2005;174:2303–6.
- Rane A., Saleemi A., Cahill D., et al. Have stent-related symptoms anything to do with placement technique? J. Endourol. 2001;15:741–5.
- Beiko D.T., Watterson J.D., Knudsen B.E., et al. Double-blind randomized controlled trial assessing the safety and efficacy of intravesical agents for ureteral stents symptoms after extracorporeal shockwave lithotripsy. J. Endourol. 2004;18:723–30.
- Мартов А.Г., Гущин Б.Л., Ощепков В.Н., Ергаков Д.В. Применение α1-адрено-блокаторов для лечения нарушений мочеиспускания у больных после трансуретральной резекции предстательной железы. Урология. 2002;5 (Прил.):23–37.












Комментарии