Красный С.А., Суконко О.Г., Ролевич А.И.
ГУ «НИИ онкологии и медицинской радиологии им. Н.Н. Александрова» Минск, Беларусь
Основным методом лечения инвазивного рака мочевого пузыря является радикальная цистэктомия [1, 2, 7, 8, 15, 27, 29]. Такой подход связан с поражением мышечного слоя стенки мочевого пузыря, невозможностью выполнения трансуретральной резекции из-за большого объема опухолевой массы и высокой вероятностью регионарного метастазирования.
Данная операция включает в себя удаление единым блоком вместе с мочевым пузырем и перивезикальной клетчаткой у мужчин – предстательной железы и семенных пузырьков с прилегающей брюшиной, проксимальных частей семевыносящих протоков и 1-2 см проксимальной уретры; у женщин – матки с придатками и уретры с передней стенкой влагалища и сочетается с тазовой лимфодиссекцией [8, 11, 29, 32]. Стандартная лимфодиссекция включает удаление лимфатических тканей вокруг наружных и внутренних подвздошных сосудов и вокруг запирательного нерва с обеих сторон [8, 32].
Дооперационная диагностика метастазов в регионарных лимфоузлах является неудовлетворительной [12]. Компьютерная томография позволяет выявить только 35-40% метастатически пораженных лимфатических узлов, а тонкоигольная аспирационная биопсия лишь незначительно улучшает диагностику, так как ее чувствительность не превышает 60%, а выполняется эта процедура лишь при увеличенных лимфоузлах [12]. Позитронно-эмиссионная томография позволяет выявить метастазы в лимфатических узлах только у 67% больных [26]. При поражении регионарных лимфоузлов pN1 результаты дооперационной диагностики еще более удручающие. Все это делает обязательным выполнение в ходе цистэктомии регионарной лимфодиссекции, являющейся одновременно диагностической и лечебной операцией. В исследовании Madersbacher S. с соавторами (2003), включавшем 507 больных инвазивным раком мочевого пузыря без регионарных метастазов по данным дооперационного обследования, тазовая лимфодиссекция выявила регионарные метастазы у 24% пациентов [22].
Поражение регионарных лимфатических узлов при инвазивном раке мочевого пузыря является крайне неблагоприятным прогностическим фактором. Суммируя данные литературы, общая 5-летняя выживаемость этих больных не превышает 25% [21, 22, 31].
В данной статье мы проанализировали результаты лечения больных раком мочевого пузыря с метастазами в регионарных лимфатических узлах и оценили влияние объема лимфодиссекции на частоту выявления метастазов и выживаемость больных.
Материалы и методы
Изучены результаты 668 радикальных цистэктомий, произведенных в 1995-2005 гг. в онкоурологическом отделении ГУ «НИИ онкологии и медицинской радиологии им. Н.Н. Александрова». Характеристика пациентов представлена в таблице 1.
Возраст больных колебался от 29 до 84 лет. Средний возраст составил 62,8 ± 8,1 года. У всех больных выполнена радикальная цистэктомия по поводу рака мочевого пузыря.
Впервые установленный диагноз рака мочевого пузыря был у 476 (71,3%) больных, в 192 (28,7%) случаях операция выполнялась по поводу рецидива заболевания после ранее проведенного лечения. При этом у 117 (17,5%) больных ранее проводилась лучевая терапия на область мочевого пузыря, а у 31 (4,6%) – системная полихимиотерапия.
До 1998 года в ходе цистэктомии выполнялась лимфодиссекция, ограниченная запирательной ямкой, а также удалялись визуально измененные лимфоузлы. С 1999 года всем больным производилась стандартная лимфодиссекция, включавшая удаление лимфатических тканей вокруг наружных и внутренних подвздошных сосудов медиальнее бедренно-полового нерва и вокруг запирательного нерва с обеих сторон, а при визуальных изменениях и лимфоузлы до уровня середины общей подвздошной артерии.
Метод деривации мочи выбирался у каждого больного индивидуально. В 320 (48,1%) случаях выполнялся уретеросигмоанастомоз (основной метод отведения мочи с 1995 по 1998 годы), у 120 (18,0%) больных – уретерокутанеостомия, операция Бриккера выполнена 35 (5,2%) больным, ректосигмопластика (Майнц-II) – 27 (4,0%) пациентам, в 157 (23,5%) случаях выполнялась операция по ортотопической реконструкции мочевого пузыря из подвздошной или сигмовидной кишки. В 5 (0,7%) случаях произведена операция по созданию континентного гетеротопического резервуара и в 4 (0,5%) случаях ректального мочевого пузыря и сигмостомы. Из методик илеоцистопластики применяли методики Штудера (U. Studer) – в 15 случаях и W-образную илеоцистопластику (E. Hautmann) – в 141 случае. Обязательными условиями проведения ортотопического отведения мочи являлись: удовлетворительная функция почек (креатинин < 150 ммоль/л), отрицательный результат биопсии простатического отдела уретры, нормальные интеллектуальные способности пациента, возможность последующего регулярного контроля.
Расчет выживаемости проводился с использованием метода Каплана-Мейера. Для сравнения выживаемости больных в различных группах применялся непараметрический log-rank тест. При оценке достоверности различий номинальных данных использовался критерий Фишера (χ2–тест). Для определения прогностической значимости различных факторов проводился мультивариантный анализ с использованием регрессионной модели Кокса. Статистически достоверными различия считались при уровне р<0,05.
Результаты
Опухоль, ограниченная мочевым пузырем (pT1-2, pN0М0), была выявлена в 269 (40,4%) случаях. У 399 (59,6%) пациентов опухоль выходила за пределы органа (прорастание опухоли в жировую клетчатку или соседние органы, либо метастазы в регионарных лимфатических узлах или отдаленные метастазы). Метастатическое поражение регионарных лимфоузлов (N+) выявлено у 151 (22,6%) больного.
В ближайшем послеоперационном периоде (30 суток) умерло 34 больных, послеоперационная летальность составила 5,1%. При этом из 151 больного с метастазами в регионарных лимфоузлах в ближайшем послеоперационном периоде умерло 4 (2,6%) пациента. Таким образом, наличие метастазов в регионарных лимфатических узлах не повлияло на количество послеоперационных осложнений и послеоперационную летальность.
При анализе частоты выявления метастазов в регионарных лимфоузлах в зависимости от объема лимфодиссекции (табл. 2) отмечено, что при выполнении стандартной лимфодиссекции выявляется значительно большее количество метастатически пораженных лимфатических узлов, чем при ограниченной лимфодиссекции: 24,8% и 17,8%, соответственно (р χ2 = 0,04).
Основные различия получены за счет пациентов с инвазией опухоли в жировую клетчатку (рТ3), поэтому данная группа больных проанализирована более детально (табл. 3). Обращает на себя внимание, что при выполнении стандартной лимфодиссекции значительно увеличилось количество пациентов с множественными метастазами в регионарных лимфоузлах (N2), которые не выявлялись при ограниченной лимфодиссекции: 27,6% и 8,6%, соответственно (р χ2 = 0,04).
Общая пятилетняя выживаемость для всей группы больных, включенных в исследование, составила 27,8 ± 2,3%, десятилетняя – 20,1 ± 3,2%. Пятилетняя выживаемость больных с интактными лимфоузлами была достоверно выше, чем у больных с метастазами в регионарных лимфоузлах – 33,3 ± 2,7% и 8,9 ± 3,4%, соответственно (р = 0,000001).
В таблице 4 представлена зависимость общей пятилетней выживаемости от местной распространенности опухоли. При инвазивном раке мочевого пузыря наиболее высокая выживаемость отмечена у больных с опухолями, ограниченными мышечной оболочкой мочевого пузыря. При прорастании опухоли в поверхностную мышцу пятилетняя выживаемость после цистэктомии составила 39,7 ± 5,9%, а при инвазии глубокой мышцы - 31,9 ± 7,4% (р > 0,05). В случае выхода опухоли за пределы мочевого пузыря с прорастанием в паравезикальную клетчатку или соседние органы (рТ3-4) общая пятилетняя выживаемость значительно снижалась и составляла 18,0 ± 2,9% (р = 0,000001).
Подобная закономерность отмечена и при изучении зависимости отдаленных результатов от степени поражения регионарных лимфоузлов (табл. 4, рис. 1).
Пятилетняя выживаемость больных с одиночным регионарным метастазом до 2 см в диаметре (рN1) достоверно не отличалась от выживаемости пациентов с интактными регионарными лимфатическими узлами и составила 28,1 ± 8,9% и 33,3 ± 2,7%, соответственно. При множественном поражении регионарных лимфоузлов данный показатель достоверно снижался.
Увеличение объема оперативного вмешательства позволило сократить у больных раком мочевого пузыря с регионарными метастазами количество нерадикально выполненных операций (R1-2) с 34,2% до 19,5%. При этом значительно увеличилась общая выживаемость пациентов (рис. 2). После цистэктомии с ограниченной лимфодиссекцией все больные с метастазами в регионарных лимфоузлах умерли в течение 30 месяцев после операции, а после стандартной лимфодиссекции пятилетняя общая выживаемость больных с регионарными метастазами составила 23,8 ± 6,7% (р = 0,006).
В качестве метода деривации мочи у больных раком мочевого пузыря с метастазами в регионарных лимфоузлах в 71 (47,0%) случае применялся уретеросигмоанастомоз, у 40 (26,5%) больных – уретерокутанеостомия, операция Бриккера выполнена 10 (6,6%) больным, ректосигмопластика (Майнц-II) – 5 (3,3%) пациентам, в 25 (16,6%) случаях выполнялась операция по созданию искусственного мочевого пузыря из подвздошной кишки.
При анализе зависимости отдаленных результатов от метода отведения мочи (рис. 3) выявлены значительные преимущества современных методик операции, к которым мы отнесли ортотопическую реконструкцию мочевого пузыря, операцию Бриккера и ректосигмопластику Майнц-2. Общая пятилетняя выживаемость больных при использовании современных методов отведения мочи увеличилась с 7,7 ± 3,7% до 41,5 ± 11,6% (р = 0,002).
При моновариантном анализе такие факторы, как возраст, пол, глубина инвазии и степень дифференцировки опухоли у больных раком мочевого пузыря с регионарными метастазами не оказали влияния на выживаемость. Мультивариантный анализ с использованием регрессионной модели Кокса с включением прогностически значимых факторов, полученных при моновариантном анализе, показал, что независимое прогностическое значение имеют степень поражения регионарных лимфоузлов (р=0,04) и объем лимфодиссекции (р=0,02).
Обсуждение
Частота поражения регионарных лимфоузлов при раке мочевого пузыря колеблется от 14 до 38% [21, 22, 30, 31]. Для того чтобы выявить 60% пораженных лимфатических узлов, необходимо удалить 15 лимфоузлов и более, а при удалении 20-23 лимфоузлов и более выявляется 80% метастазов [13]. При этом стандартная лимфодиссекция позволяет удалить 5-30 лимфоузлов, а расширенная от 9 до 67 [30]. Поэтому некоторые авторы рекомендуют расширить объем лимфаденэктомии, включая дистальную часть общей подвздошной артерии [5], всю общую подвздошную артерию [4] и даже бифуркацию аорты и пресакральную зону [3, 20, 30]. Продолжительность расширенной лимфодиссекции увеличивается на 1 час по сравнению со стандартной, при этом количество осложнений не меняется [6]. Однако консенсуса в отношении объема лимфодиссекции сегодня нет, и в подавляющем большинстве случаев производится стандартная лимфодиссекция.
В нашем исследовании увеличение объема лимфодиссекции привело к достоверному увеличению выявленных регионарных метастазов с 17,8% до 24,8%, в основном это увеличение произошло за счет выявления множественных метастазов в лимфоузлах у пациентов с инвазией опухоли в паравезикальную клетчатку (рТ3).
В ряде исследований было показано, что выживаемость больных напрямую зависит от количества пораженных лимфоузлов [10, 17, 28], поэтому была разработана концепция удельного веса метастатически пораженных лимфоузлов среди общего числа удаленных, согласно которой пациенты с процентом метастатически пораженных лимфоузлов 20% и более имеют значительно более неблагоприятный прогноз, чем больные, у которых поражено менее 20% удаленных лимфоузлов [13, 28]. Прорастание опухоли за пределы капсулы лимфоузла еще более ухудшает прогноз заболевания [9].
Каким образом объем лимфодиссекции влияет на выживаемость больных инвазивным раком мочевого пузыря до конца не ясно, так как не было проведено рандомизированных исследований по этому поводу и, вероятно, они не могут быть проведены вообще. Однако в ряде исследований было показано, что увеличения выживаемости можно добиться при удалении 14 и более лимфоузлов [21, 24]. Подобные результаты были получены и в других исследованиях [14, 18]. Данную операцию рекомендуется выполнять даже в случае полной регрессии опухоли в результате неоадъювантной терапии [12].
В 2004 году Herr H.W. с соавторами проанализировали результаты цистэктомий, выполненных 106 хирургами в 109 различных центрах США [16]. Было выявлено, что пятилетняя выживаемость больных инвазивным раком мочевого пузыря после цистэктомии без лимфодиссекции, с ограниченной лимфаденэктомией и со стандартной тазовой лимфодиссекцией составляет 33%, 46% и 60%, соответственно. Удаление 10 и более регионарных лимфоузлов позволяет увеличить 5-летнюю выживаемость с 44% до 61% и снизить частоту местных рецидивов с 25% до 6%. При этом 62% общих урологов по сравнению с 23% онкоурологов в ходе цистэктомии выполняют ограниченную лимфаденэктомию, либо не выполняют ее вообще (р<0,001). Отсюда делается вывод, что хирургические факторы влияют на выживаемость больных после цистэктомии не меньше, чем распространенность процесса и дополнительное лечение.
Полученные нами результаты также показывают важность тщательного выполнения в ходе радикальной цистэктомии регионарной лимфодиссекции, позволяющей при регионарных метастазах рN1 добиться пятилетней выживаемости, сравнимой с выживаемостью пациентов с интактными лимфоузлами, а при множественных метастазах (рN2) данный показатель достигает 6,9 ± 3,4%. При метастазах в регионарных лимфоузлах более 5 см в диаметре, когда опухоль невозможно удалить радикально, общая однолетняя выживаемость составила 23,1 ± 11,7%, а двухлетний период не пережил ни один больной. Подобные результаты со столь низкой продолжительностью жизни следует ожидать при выполнении цистэктомии без регионарной лимфодиссекции у больных раком мочевого пузыря с регионарными метастазами рN1 и рN2.
Несмотря на рутинное выполнение тазовой лимфаденэктомии при радикальной цистэктомии, обоснованность выполнения илеоцистопластики при наличии метастазов в тазовых лимфоузлах остается предметом споров. C одной стороны, в недавних исследованиях получен ответ на вопрос о терапевтической роли тщательной тазовой лимфодиссекции при раке мочевого пузыря. Было продемонстрировано увеличение выживаемости при тщательном удалении лимфатических узлов. С другой стороны, частота местных рецидивов после радикальной цистэктомии по поводу инвазивного рака мочевого пузыря остается достаточно высокой. Однако оказалось, что только половина этих больных испытывает проблемы с ортотопическим резервуаром в течение последних 6 месяцев жизни. Продолжительность жизни после развития местного рецидива весьма ограничена, но большинство пациентов могут рассчитывать на нормальную функцию кишечного “мочевого пузыря”, несмотря на наличие местного рецидива. Поэтому сегодня некоторые авторы считают, что наличие метастазов в регионарных лимфоузлах не является противопоказанием к формированию искусственного мочевого пузыря [19, 30].
В нашем исследовании использование современных методик операции (ортотопическая реконструкция мочевого пузыря, операция Бриккера и ректосигмопластика Майнц-2) позволило существенно увеличить общую пятилетнююя выживаемость с 7,7 ± 3,7% до 41,5 ± 11,6% (р = 0,002). Хотя эти группы больных нельзя считать полностью сопоставимыми, так как исследование нерандомизированное, тем не менее, полученные результаты говорят о возможности использования ортотопического отведения мочи у больных с регионарными метастазами после радикальной операции.
Что касается формирования гетеротопического резервуара больным с регионарными и даже отдаленными метастазами, то по нашему мнению наличие метастазов совершенно не влияет на функцию резервуара и не может быть каким-либо ограничивающим фактором для данного вида операции. Единственной особенностью проведения лечения этим больным является необходимость установки постоянного катетера в резервуар на все время проведения химиотерапии для исключения обратного всасывания препаратов, что в свою очередь может привести к передозировке и значительному увеличению токсичности.
Радикальная цистэктомия показана больным с клинической стадией T2-4N0M0. Если клинически выявляются метастазы в лимфатических узлах или отдаленные метастазы, хирургическое лечение не увеличивает выживаемость. Поэтому таким больным операция показана для улучшения качества жизни при выраженной макрогематурии, дизурии и боли, а также в случае задержки мочи [25]. Существенного увеличения выживаемости можно добиться только при проведении таким пациентам комплексного лечения с использованием химиотерапии [7, 23, 31].
Выводы
Стандартная лимфодиссекция при раке мочевого пузыря позволяет достоверно увеличить частоту выявления регионарных метастазов по сравнению с ограниченной лимфодиссекцией. Основное увеличение происходит за счет выявления множественных метастазов в лимфоузлах у пациентов с инвазией опухоли в паравезикальную клетчатку (рТ3).
Данное увеличение объема лимфодиссекции у больных раком мочевого пузыря с регионарными метастазами позволило достоверно сократить количество нерадикально выполненных операций (R1-2) и увеличить общую пятилетнюю выживаемость.
Полученные результаты выживаемости больных раком мочевого пузыря с метастазами в регионарных лимфоузлах после цистэктомии с применением современных методов отведения мочи говорят о возможности использования у данной категории пациентов ортотопического отведения мочи после радикальной операции.
Из всех факторов, влияющих на выживаемость больных данной категории независимое прогностическое значение имеют степень поражения регионарных лимфоузлов и объем лимфодиссекции.
ЛИТЕРАТУРА
- Мавричев А.С., Красный С.А., Поляков С.Л. и др. Онкоурология. Минск, БелЦНМИ. – 2001. – 255с.
- Матвеев Б.П., Фигурин К.М., Карякин О.Б. Рак мочевого пузыря. Москва, «Вердана». - 2001. - 243с.
- Ather M.H., Fatima S., Sinanoglu O. Extent of lymphadenectomy in radical cystectomy for bladder cancer // World Journal of Surgical Oncology. – 2005. - №3, Vol.43. – P.1-5.
- Bochner B.H., Cho D., Herr H.W., et al. Prospectively packaged lymph node dissections with radical cystectomy: evaluation of node count variability and node mapping // J. Urol. – 2004. – Vol.172. – P.1286–1290.
- Bochner B.H., Herr H.W., Reuter V.E. Impact of separate versus en block pelvic lymph node dissection on the number of lymph nodes retrieved in cystectomy specimens // J. Urol. – 2001. – Vol.169. – P.2295–2296.
- Brössner C., Pycha A., Toth A., et al. Does extended lymphadenectomy increase the morbidity of radical cystectomy? // BJU Int. – 2004. – Vol.93. – P.64–66.
- Busby J.E., Evans C.P. Old friends, new ways: revisiting extended lymphadenectomy and neoadjuvant chemotherapy to improve outcomes // Curr. Opin. Urol. – 2004. - Vol.14. P.251–257.
- Campbell’s Urology, 8th ed. Edited by P.C. Walsh, A.B. Retik, E.D. Vaughan and A. J. Wein. Philadelphia: W. B. Saunders Co. - 2002. - 3150 p.
- Fleischmann A., Thalmann G.N., Markwalder R., Studer U.E. Prognostic implications of extracapsular extension of pelvic lymph node metastases in urothelial carcinoma of the bladder // Am. J. Surg. Pathol. – 2005. – Vol.29. - 89–95.
- Frank I., Cheville J.C., Blute M.L., et al. Transitional cell carcinoma of the urinary bladder with regional lymph node involvement treated by cystectomy: clinicopathologic features associated with outcome // Cancer. - 2003. – Vol.97. – P. 2425-2430.
- Hautmann R.E., Stein J.P. Neobladder with prostatic capsule and seminal-sparing cystectomy for bladder cancer: A step in the wrong direction // Urol. Clin. North. Am. – 2005. – Vol.32, №2. – P.177–185.
- Hoshi S., Orikasa S., Suzuki K., et al. Diagnosis and treatment of pelvic lymph node metastasis in bladder cancer // International Journal of Urology. – 1999. – Vol. 6. – P. 400–407.
- Herr H.W. Superiority of ratio based lymph node staging for bladder cancer // J. Urol. – 2003. – Vol.169. – P.943–945.
- Herr H.W. Surgical factors in bladder cancer: more (nodes) + more (pathology) = less (mortality) // BJU Int. – 2003. – Vol.92. – P.187–188.
- Herr H.W. The natural history of a T1 bladder cancer: life-long tumour diathesis // BJU Int. – 1999. – Vol.84. – P.1102-1103.
- Herr H.W., Faulkner J.R., Grossman H.B., R., et al. Surgical factors influence bladder cancer outcomes: a cooperative group report // J. Clin. Oncol. - 2004. – Vol.22. – P. 2781-2785.
- Knap M.M., Lundbeck F., Overgaard J. The role of pelvic lymph node dissection as a predictive and prognostic factor in bladder cancer // Eur. J. Cancer. – 2003. – Vol.39. – P.604–613.
- Konety B.R., Joslyn S.A. Factors influencing aggressive therapy for bladder cancer: an analysis of data from the SEER program // J. Urol. – 2003. – Vol.170. – P.1765–1771.
- Lebret T., Herve J.M., Yonneau L. et al. After cystectomy, is it justified to perform a bladder replacement for patients with lymph node positive bladder cancer? // Eur. Urol. – 2002. – Vol.42. – P.344–349.
- Leissner J., Ghoneim M.A. Abol-Enein H., et al. Extended radical lymphadenectomy in patients with urothelial bladder cancer: results of a prospective multicenter study // J. Urol. – 2004. – Vol.171. – P.139–144.
- Liedberg F., Mansson W. Lymph node metastasis in bladder cancer // Eur. Urol. - 2006. – Vol. 49. – P.13–21.
- Madersbacher S., Hochreiter W., Burkhard F., H., et al. Radical cystectomy for bladder cancer today – a homogeneous series without neoadjuvant therapy // J. Clin. Oncol. – 2003. – Vol.21. – P.690–696.
- Nishiyama H., Habuchi T., Watanabe J., et al. Clinical outcome of a large-scale multi-institutional retrospective study for locally advanced bladder cancer: a survey including 1131 patients treated during 1990–2000 in Japan // Eur. Urol. - 2004. – Vol.45. – P.176–181.
- Sanderson K.M., Stein J.P., Skinner D.G. The evolving role of pelvic lymphadenectomy in the treatment of bladder cancer // Urol. Oncol. - 2004. – Vol.22. – P.205-213.
- Shekarriz B., Pontes J.E. Management of poor risk patients with muscleinvasive transitional cell carcinoma of the bladder // AUA Update Series. – 2001. – Vol.20. – P.90–95.
- Shvarts O., Han K.R., Seltzer M., et al. Positron emission tomography in urologic oncology // Cancer Control. – 2002. – Vol.9. – P.335–342.
- Solsona E., Iborra I., Dumont R., et al. Risk groups in patients with bladder cancer treated with radical cystectomy: statistical and clinical model improving homogeneity // J. Urol. – 2005. - Vol. 174. – P.1226–1230.
- Stein J.P., Cai J., Groshen S., Skinner D.G. Risk factors for patients with pelvic lymph node metastases following radical cystectomy with en block pelvic lymphadenectomy: the concept of lymph node density // J. Urol. – 2003. – Vol.170. – P.35–41.
- Stein J.P., Lieskovsky G., Cote R., et al. Radical cystectomy in the treatment of invasive bladder cancer: long-term results in 1054 patients // J. Clin. Oncol. – 2001., Vol. 19. – P.666–775.
- Stein J.P., Quek M.L. Skinner D.G. Lymphadenectomy for invasive bladder cancer: I. historical perspective and contemporary rationale // BJU Int. – 2006. – Vol.97. – P.227 – 231.
- Stein J.P., Quek M.L. Skinner D.G. Lymphadenectomy for invasive bladder cancer: II. technical aspects and prognostic factors // BJU Int. – 2006. – Vol.97. – P.227 – 231.
- Stenzl A., Nagele U., Kuczyk M., et al. Cystectomy - technical considerations in male and female patients // EAU Update Series. – 2005. - №3. – P.138–146.
Таблица 1. Характеристика больных раком мочевого пузыря после радикальной цистэктомии
| Характеристика | Число больных |
% |
Пол: рN0 М0 Гистологический тип опухоли: Степень дифференцировки опухоли: |
4 517 651
|
0,6 77,5 97,5
|
Таблица 2. Частота поражения регионарных лимфоузлов в зависимости от объема лимфодиссекции
| Критерий Т |
Ограниченная лимфодиссекция |
Стандартная лимфодиссекция |
||
рN0 абс. (%) |
рN+ абс. (%) |
рN0 абс. (%) |
рN+ абс. (%) |
|
рТ1 |
36 (100) |
- |
46 (100) |
- |
Всего: |
175 (82,2) |
38 (17,8) |
342 (75,2) |
113 (24,8) |
Таблица 3. Степень поражения регионарных лимфоузлов у пациентов с инвазией опухоли в жировую клетчатку (рТ3)
| Критерий N |
Ограниченная лимфодиссекция абс. (%) |
Стандартная лимфодиссекция абс. (%) |
Всего: абс. (%) |
N0 |
56 (80,0) |
72 (62,1) |
128 (68,8) |
Всего: |
70 (100) |
116 (100) |
186 (100) |
Таблица 4. Зависимость общей пятилетней выживаемости больных после радикальной цистэктомии от местной распространенности опухоли
| Местная распространенность процесса |
Число больных |
Пятилетняя выживаемость, % |
рТ0-1 |
82 |
48,2 ± 6,3 |
рN0 |
517 |
33,3 ± 2,7 |
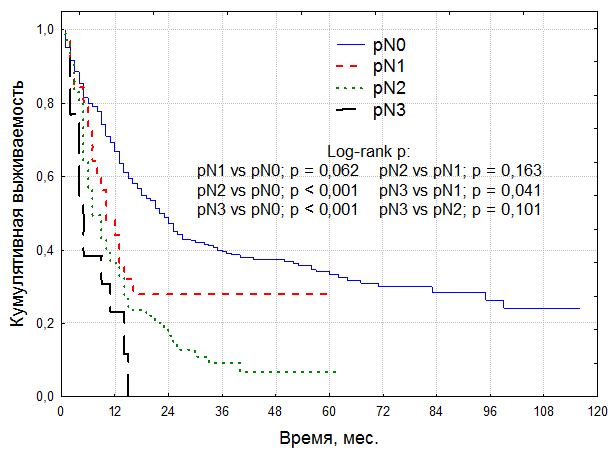
Рисунок 1. Общая выживаемость больных раком мочевого пузыря в зависимости от степени поражения регионарных лимфоузлов
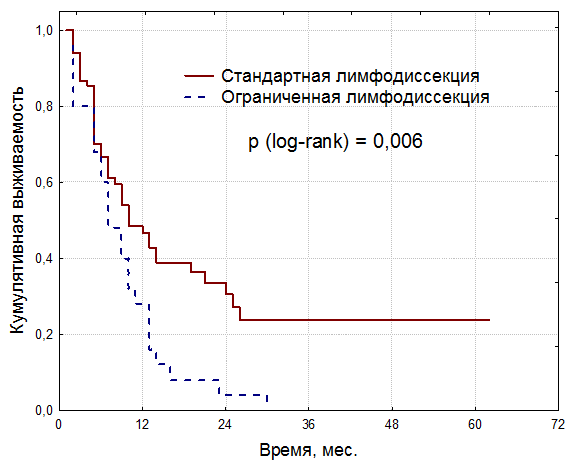
Рисунок 2. Зависимость общей выживаемости больных раком мочевого пузыря с метастазами в регионарных лимфоузлах от объема лимфодиссекции
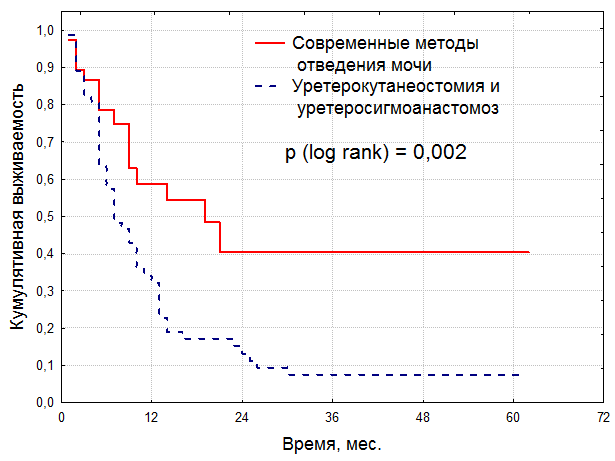
Рисунок 3. Зависимость общей выживаемости больных раком мочевого пузыря с метастазами в регионарных лимфоузлах от метода отведения мочи
Реферат
Красный С.А., Суконко О.Г., Ролевич А.И.
Результаты лечения больных раком мочевого пузыря с метастазами в регионарных лимфоузлах
По материалам 668 радикальных цистэктомий изучены результаты лечения 151 (22,6%) больного раком мочевого пузыря с метастазами в регионарных лимфоузлах и оценено влияние объема лимфодиссекции на частоту выявления метастазов и выживаемость больных.
Стандартная лимфодиссекция при раке мочевого пузыря позволяет достоверно увеличить частоту выявления регионарных метастазов по сравнению с ограниченной лимфодиссекцией с 17,8% до 24,8% (р = 0,04). Данное увеличение объема лимфодиссекции у больных раком мочевого пузыря с регионарными метастазами позволило достоверно увеличить общую пятилетнюю выживаемость (р = 0,006).
Полученные результаты выживаемости больных раком мочевого пузыря с метастазами в регионарных лимфоузлах после цистэктомии с применением современных методов отведения мочи говорят о возможности использования у данной категории пациентов ортотопического отведения мочи после радикальной операции.
Из всех факторов, влияющих на выживаемость больных данной категории независимое прогностическое значение имеют степень поражения регионарных лимфоузлов (р=0,04) и объем лимфодиссекции (р=0,02).







Комментарии