В апреле 2024 г. вышло в свет пособие для врачей Диагностика и лечение в схемах и алгоритмах: пособие для врачей / под. ред. А.А. Камалова. – М., ООО «Научно-методический организационный медицинский центр», 2024. – 184 с. ISBN 978-5-6051616-9-1. Данное пособие освещает основные заболевания в урологии и андрологии, с которыми в рутинной клинической практике сталкивается практически каждый врач-уролог. Разработанные схемы и алгоритмы позволяют в короткие сроки наметить структурированный план обследования пациентов с разъяснением и обоснованием характеристик каждого шага. Особое внимание уделяется вопросам лечения пациентов, причём как с использованием консервативных, так и оперативных методик. В рамках лечения подробно описываются группы препаратов, а также различные варианты оперативных вмешательств в зависимости от каждой конкретной клинической ситуации. Данное издание представляет собой настольную книгу, особенно полезную для специалистов амбулаторного звена здравоохранения, когда за ограниченное время консультации необходимо принять взвешенное и обоснованное решение относительно диагностической и лечебной тактики ведения пациента. Пособие подготовлено сотрудниками кафедры урологии и андрологии ФФМ МГУ имени М.В. Ломоносова.
Представляем Вашему вниманию один из алгоритмов. Инфографика построена на основе клинических рекомендаций «Эректильная дисфунк ция» https://cr.minzdrav.gov.ru/schema/15_2#doc_a1
Диагностика
В рамках первичного приёма пациента с ЭД особенно важным является создание непринуждённой атмосферы для создания доверительных отношений «врач– пациент»
Эректильная дисфункция – неспособность достижения или поддержания эрекции, достаточной для проведения полового акта. Основным критерием установления ЭД является наличие жалоб на расстройства эрекции длительностью не менее 3 месяцев [1, 2].
В рамках первичного приёма пациента с жалобами на ЭД необходимо уточнять длительность, характер и стабильность нарушений эрекции, влияние отдельных факторов и обстоятельств, наличие постоянного полового партнёра и характер взаимоотношений с партнёром.
Список обязательных вопросов в рамках данного блока:
- Как давно у пациента проблема?
- Бывают ли успешные половые контакты?
- Женат ли пациент? Есть ли у него постоянная партнёрша?
- Является ли партнёрша единственной? Отношение партнёрши к проблеме.
- Если партнёрша не единственная – есть ли разница в качестве эрекции?
- Имеется ли различие при проведении половых актов в разное время суток?
В рамках первичного приёма необходимо оценить наличие полового влечения, частоту и продолжительность половых актов, наличие оргазмов. Список обязательных вопросов в рамках данного блока:
- Наличие сексуального желания?
- Как часто проводятся половые контакты из расчёта на 1 неделю?
- Возможен ли повторный половой контакт в тот же день?
- Какая максимальная и минимальная длительность полового акта?
- Удовлетворённость пациента и партнёрши?
- Яркость и выраженность оргазма? Характер семяизвержения?
В рамках первичного приёма пациента с ЭД необходимо уточнить наличие утренних эрекций.
В рамках первичного приёма пациента с ЭД необходимо уточнить обращался ли пациент с данной проблемой ранее, какие схемы лечения и препараты использовал и было ли данное лечение эффективным.
Пациентам с ЭД целесообразной является оценка качества сна с целью выявления потенциальных нарушений режима сна и бодрствования, указывающих на наличие синдрома хронической усталости. Наличие ночного храпа может указывать на наличие синдрома обструктивного апноэ сна. Список обязательных вопросов в рамках данного блока:
- Качество сна и удовлетворённость сном?
- Какая средняя продолжительность сна?
- Наличие храпа?
Всем пациентам с ЭД при сборе анамнеза рекомендуется выявлять наличие сопутствующих заболеваний и вредных привычек, которые являются потенциальным фактором риском развития ЭД [3–6]:
- Метаболические нарушения – сахарный диабет, гиперлипидемия, ожирение, метаболический синдром.
- Сердечно-сосудистые заболевания – гипертоническая болезнь, окклюзивные поражения сосудов, атеросклероз.
- Неврологические заболевания – инсульты, болезнь Паркинсона, рассеянный склероз, травмы головного и спинного мозга, новообразования центральной и периферической нервной системы, периферические нейропатии, полинейропатии, депрессии.
- Заболевания эндокринной системы – гипогонадизм, гиперпролактинемия, болезнь Иценко–Кушинга.
- Оперативные вмешательства или лучевая терапия на органах малого таза и забрюшинного пространства.
- Вредные привычки и факторы окружающей среды – табакокурение, алкоголизм, употребление наркотических средств, неблагоприятные факторы окружающей среды (радиация, электромагнитное излучение).
У всех пациентов с ЭД при сборе анамнеза необходимо уточнить факт приёма лекарственных препаратов, способных ухудшать качество эректильной функции и быть потенциальной причиной лекарственно-индуцированной ЭД: тиазидные диуретики, неселективные бета-адреноблокаторы, антидепрессанты, антиандрогены, психолептики, опиоиды [7].
У пациентов с ЭД в рамках первичного приёма необходимо уточнять наличие и характер нарушений мочеиспускания и наличие сопутствующих болей в промежности, пояснице, нижних конечностях, а также связи боли с половой активностью и мочеиспусканием. Наличие болей или нарушений мочеиспускания может свидетельствовать о воспалительных заболеваниях органов малого таза или заболеваниях неврологического характера.
В рамках первичного физикального обследования пациента с подозрением на ЭД необходимо провести тщательный осмотр промежности, полового члена, органов мошонки. При осмотре оценивают следующие параметры:
- Чувствительность кожи промежности.
- Нарушение анатомии полового члена: искривления, наличие уплотнений и бляшек, аномалии расположения уретры.
- Наличие признаков гипогонадизма: уменьшение размера яичек, изменение вторичных половых признаков.
- Определение типа оволосения.
Пациентам с ЭД в рамках физикального обследования рекомендуется оценка состояния сердечно-сосудистой системы: измерение артериального давления, пульса, индекса массы тела, окружности талии.
Всем пациентам с жалобами на ЭД с целью объективизации жалоб, количественной характеристики сексуальных нарушений рекомендуется использовать один из предложенных валидированных опросников эректильного скрининга. Наиболее распространённая анкета – Международный индекс эректильной функции (МИЭФ-15) и его сокращённый вариант (МИЭФ-5) [8, 9].
Дополнительно для оценки ригидности полового члена возможно использование шкалы твёрдости эрекции (EHS – Erectile Hardness Score), для выявления симптомов андрогенодефицита – опросника возрастных симптомов андрогенодефицита (AMS– Aging Male Screening), для выявления корреляции сексуальной активности и возрастного снижения базовых уровней половых гормонов – шкалы количественной оценки мужской копулятивной функции (МКФ) [10].
Для оценки психического статуса пациентам с ЭД в рамках первичного приёма рекомендовано заполнение шкалы тревоги и депрессии HADS и/или шкалы депрессии Бека. Признаком невроза или повышенного уровня тревожности считается 8 баллов и более по шкале HADS и 10 баллов и выше по шкале Бека [11].
«Виагра-тест» проводится всем пациентам с подозрением на ЭД при отсутствии противопоказаний к назначению иФДЭ-5. Тест позволяет оценивать все компоненты копулятивного цикла в течение заданного периода времени. Стандартное время выполнения – 4 недели, с условием сексуальной активности не менее 1 эпизода в неделю. Ингибитор ФДЭ-5 назначается при жалобах на снижение либидо ежедневно, при нормальном либидо – по требованию. Все половые контакты должны быть зафиксированы в виде дневника. Фиксируются дата, факт использования иФДЭ-5, факт семяизвержения и оценка качества от 1 до 5 баллов. Если у пациента есть жалобы на продолжительность интимного контакта – добавляется субъективное время продолжительности [12].
Всем пациентам с ЭД рекомендуется обязательное исследование уровня гликемическогопрофиля(глюкозыигликированногогемоглобина) илипидного профиля (общего холестерина, липопротеинов низкой и высокой плотности, триглицеридов), а также оценка уровня мочевой кислоты для определения наличия сопутствующих заболеваний, ассоциированных с развитием ЭД и их потенциальных факторов риска [13].
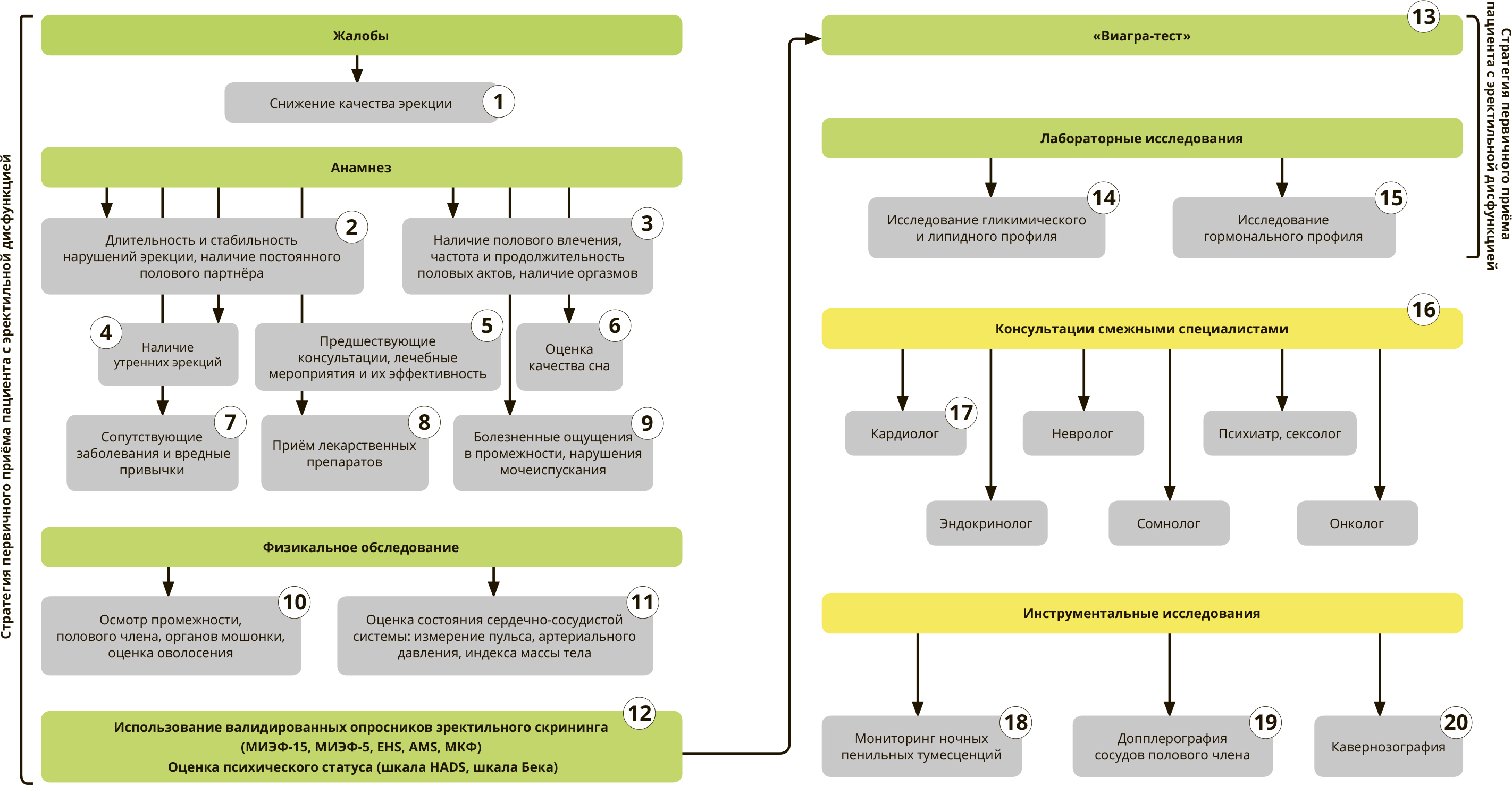
Всем пациентам с ЭД рекомендуется обязательное исследование уровня общего тестостерона, однако целесообразным является исследование уровня ряда других гормонов для уточнения возможности лекарственной коррекции имеющихся эректильный нарушений: ГСПГ, ЛГ, эстрадиол, прогестерон, ТТГ, пролактин, ПСА [13, 14].
После первичного приёма пациента с ЭД при выявлении или подозрении на наличиесопутствующихфакторов, которыемогутпровоцироватьилиусиливать ЭД, в рамках междисциплинарного подхода требуется дополнительное обследование с привлечением смежных специалистов:
- Кардиолог – при наличии жалоб и анамнестических данных на наличие кардиологических заболеваний и их факторов риска.
- Невролог – при выявлении клинических признаков неврологических заболеваний.
- Психиатр (психотерапевта для пациента), сексолог – при подозрении на психогенные формы ЭД, наличие отягощённого психосоматического статуса, выявлении признаков невроза, повышенного уровня тревожности и депрессии.
- Эндокринолог – при выявлении клинических признаков сахарного диабета, метаболического синдрома, нарушении гормонального профиля неясного генеза.
- Сомнолог – при наличии жалоб на нарушение сна, ночного храпа, подозрении на синдром обструктивного апноэ сна.
- Онколог – в случае отягощённого онкологического анамнеза и необходимости дальнейшей гормональной терапии.
На основании результатов первичного приёма в большинстве случаев удается диагностировать наличие ЭД, а также выявление возможных органических и/или психогенных причин.
При необходимости в рамках дальнейшего обследования пациентов может потребоваться консультация смежными специалистами и проведение специализированных инструментальных исследований.
Учитывая высокую распространённость заболеваний сердечно-сосудистой системы объём обследования пациента с ЭД в рамках кардиологического обследования должен быть достаточным для заключения о допустимой сексуальной активности и об отсутствии противопоказаний к терапии ЭД. Для стандартизации врачебных рекомендаций по сексуальной активности в зависимости от состояния сердечно-сосудистой системы был разработан консенсус, согласно которому пациентов разделяют на группы низкого, среднего и высокого рисков [15]. При низкой степени риска сексуальную активность и лечение ЭД считают безопасным. При средней и высокой степенях рисков необходимо дополнительное обследование у врача-кардиолога [2].
Регистрация ночных пенильных тумесценций с помощью специальных приборов, фиксирующих в онлайн-режиме изменение диаметра и ригидности полового члена во время сна. Данная методика является единственным объективным методом дифференциальной диагностики психогенной и органической ЭД: в случае наличия нормальных показателей мониторинга ночных пенильных тумесценций при жалобах на ЭД имеет место психогенный вариант [16–18].
Фармакодопплерография сосудов полового члена с помощью УЗИ с использованием инъекций вазоактивными препаратами дает информацию о состоянии прироста кровотока по кавернозным артериям. Основные количественные показатели – максимальная (пиковая) систолическая скорость, конечная диастолическая скорость и индекс резистентности. В норме пиковая систолическая скорость составляет более 30 см/с и индекс резистентности более 0,8 [19–21].
С учетом высокой психологической нагрузки для пациента при проведении исследования, полученная информация не всегда корректна.
Фармакодопплерография сосудов полового члена проводится при наличии у пациентов:
- первичной ЭД, не связанной с выявленными органическими или психогенными нарушениями;
- перенесенной травмы или операций на органах таза или промежности в анамнезе, деформации полового члена;
- сложных эндокринных, психических и неврологических нарушениях, а также перед фаллопластикой с протезированием [20, 22].
Кавернозография с помощью рентгенографии или МРТ – метод визуализации сосудистой системы полового члена для оценки функционального состояния вено-окклюзивного механизма. Проводится на фоне фармакопробы алпростадилом и его аналогами. После установки окклюзирующей повязки на половой член проксимальнее точки введения вводится контрастное вещество. При несостоятельности вено-окклюзивного механизма идет массивный сброс контраста с кровью по глубокой дорсальной вене и системе глубоких вен [23].
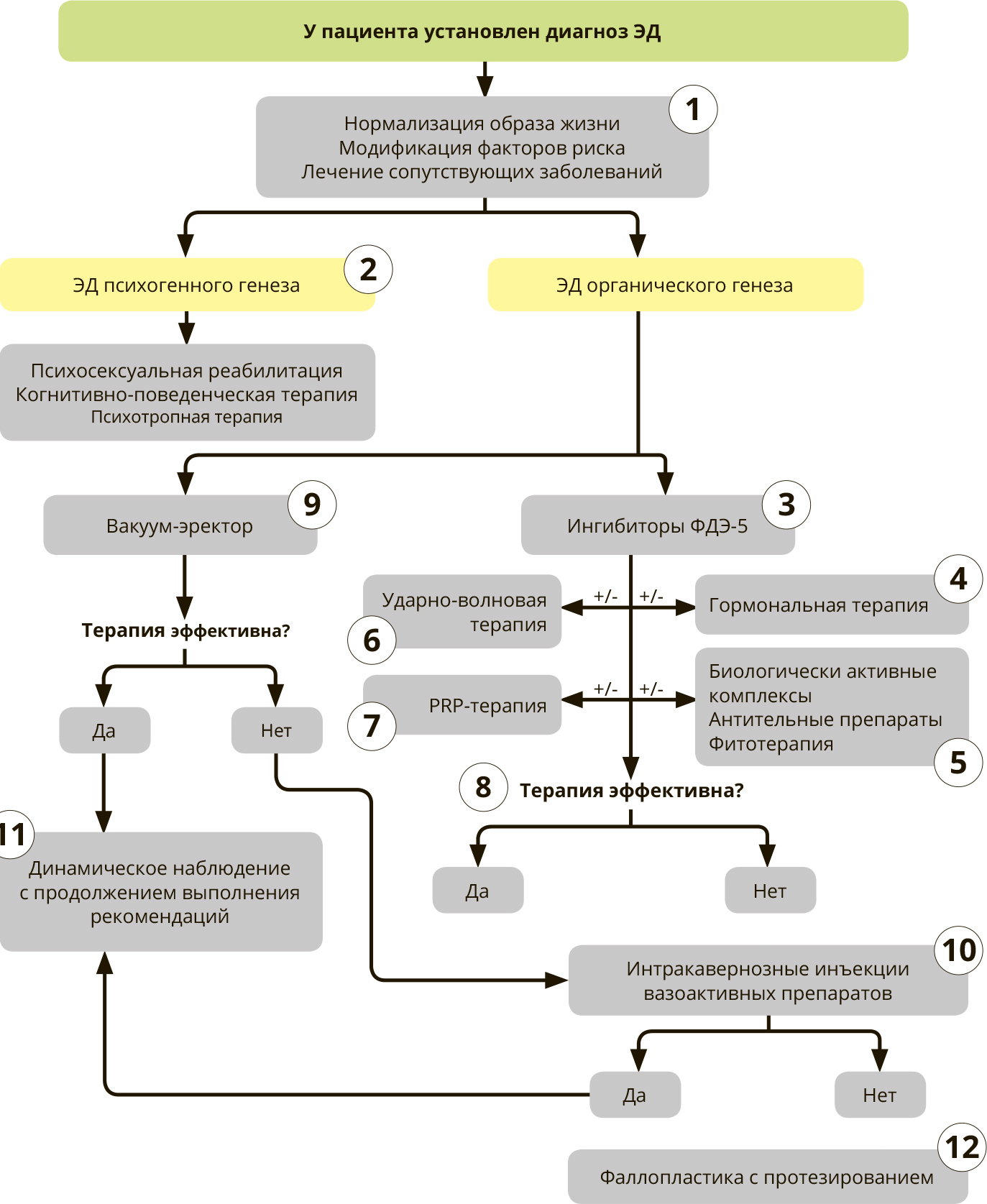
Лечение
Перед началом лечения ЭД всем пациентам для улучшения эректильной функции и/или увеличения эффективности лечебных мероприятий рекомендуется проведение мероприятий по минимизации факторов риска заболевания (отказ от курения, снижение веса, оптимизация физической нагрузки), нормализация образа жизни и лечение у смежных специалистов по поводу сопутствующих заболеваний, потенциально ассоциированных с ЭД [24, 25].
При ЭД психогенного генеза лечение рекомендовано начинать совместно с психиатрами (психотерапевт для пациента) и сексологами с психосоциальной реабилитацией, включающей обучение сексуальным навыкам, интимной гармонии (вовлечение женщины в решение проблем партнёра), психосексуальное образование [26], а также когнитивную и поведенческую терапию (КПТ – групповой формат или формат пары) [27]. При необходимости дополнительно могут быть назначены психотропная терапия, препараты из группы психостимуляторов, антидепрессантов, ноотропов.
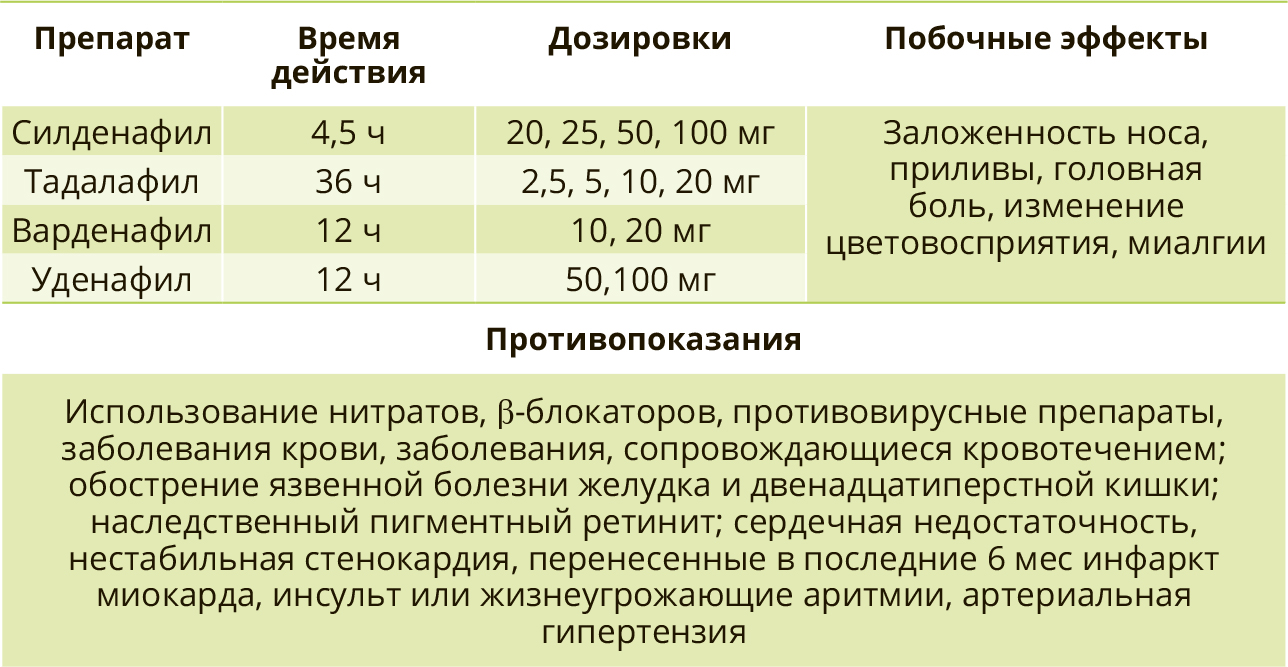
При ЭД органического характера в качестве препаратов первой линии терапии рекомендуется назначение ингибиторов фосфодиэстеразы 5 типа (иФДЭ-5) [28, 29]. В настоящее время в России доступны четыре препарата этой группы, выпускаемые в таблетированном виде в разных дозировках: силденафил, тадалафил, варденафил и уденафил. Их отличительная особенность – эффективность при всех формах ЭД и хорошая переносимость. Ингибиторы ФДЭ-5 используются эпизодически (по требованию) и курсами за определённое время перед половым актом, причём для наступления эффекта от препарата необходимо наличие визуальной сексуальной стимуляции. Дозы подбирают индивидуально: предпочтительнее начинать лечение со средних дозировок с последующей титрацией в зависимости от эффективности в сторону уменьшения или увеличения. Ингибирование ФДЭ-5 приводит к релаксации гладких мышц, вазодилатации и эрекции [30–32].
Ингибиторы ФДЭ-5 нельзя принимать параллельно с органическими нитратами из-за потенцирования гипотензивного действия.
При сочетании ингибиторов ФДЭ-5 с антигипертензивными препаратами и альфа-адреноблокаторами наблюдается склонность к гипотензии.
При лечении пациентов с ЭД рекомендуется руководствоваться принципом этапного подхода в проведении лечебных мероприятий [33].
Этапный подход предполагает последовательное применение лечебных методов с увеличением их стимулирующего действия, начиная от лекарственной терапии ингибиторами фосфодиэстеразы 5 типа в виде монотерапии или комбинации с другими лекарственными и нелекарственными методами до интракавернозных инъекций алпростадила и фаллоп ластики с протезированием.
Смена ступени лечения производится при ее неэффективности или неприемлемости для пациента [33, 34].
Для ведения пациентов с гормональными нарушениями по рекомендации эндокринолога целесообразно дополнительное назначение гормональных препаратов: андрогенов, антиэстрогенов, гонадотропинов, анаболических стероидов [14]. При наличии показаний терапия тестостероном (внутримышечная, трансдермальнаяилипероральная) можетбытьрассмотрена для мужчин с низким уровнем тестостерона и сопутствующими проблемами с эректильной функцией, сексуальным желанием, неудовлетворенностью половым актом и сексуальной жизнью в целом [35]. Терапия гормональными препаратами назначается длительно под контролем уровня гормонов.
В рамках комбинированной терапии ЭД пациентам в дополнение к основному лечению может быть рекомендовано назначение биологически активных комплексов, источников аминокислот, фитопрепаратов, препаратов на основе антител. C учетом того, что ЭД может сопровождаться эндотелиальной дисфункцией, в обязательном порядке должны назначаться средства коррекции уровня NO в эндотелиоцитах, для обеспечения адекватной эластичности кровеносных сосудов.
Ежедневное пероральное применение L-аргинина – предшественника NO в сочетании с использованием иФДЭ-5 улучшает сексуальную функцию [36]. L-аргинин назначается по схеме 1 табл. (500 мг) х 2 р/день – не менее чем на 1 месяц. При необходимости доза может быть увеличена до 2000 мг/сутки, а время приема может быть продлено до 6 месяцев.
В рамках комбинированной терапии ЭД пациентам в дополнение к основному лечению при недостаточной эффективности терапии иФДЭ-5 может быть рекомендовано проведение ударно-волновой терапии (УВТ). Методика основана на воздействии на пещеристую ткань полового члена слабых акустических волн. Проходя через биологические ткани разной плотности, акустические волны вызывают сдвиговое напряжение, которое запускает каскад реакций, стимулирующих процесс неоваскуляризации в кавернозных телах [38].
В составе комбинированной терапии ЭД пациентам в дополнение к основному лечению в рамках клинических испытаний может быть рекомендована PRP (platelet-rich plasma) – терапия, заключающаяся в интракавернозном введении обогащенной тромбоцитами аутоплазмы [39–43]. Регенеративный эффект PRP проявляется за счет высоких концентраций тромбоцитов, содержащих факторы роста, такие как VEGF, EGF, IGF-1, PDGF и FGF [44], которые ответственны за стимуляцию ангиогенеза и привлечение стволовых клеток [44]. Однако единого мнения относительно оптимальной концентрации тромбоцитов и режимов введения нет.
Комбинированная терапия назначается на протяжении 4 недель под контролем интимного дневника, который представляет собой обычный лист бумаги, где зафиксирована следующая информация – дата, когда был проведен половой контакт, факт приема таблетки-стимулятора, факт семяизвержения как показатель контроля завершения контакта и оценка качества полового контакта по – 5 балльной шкале. Дневник необходим для контроля эффективности терапии, поэтому в нем должны быть зафиксированы все интимные контакты пациента за обследуемый период.
У соматически отягощённых пожилых пациентов с низкой сексуальной активностью и невозможностью применения лекарственной терапии в качестве альтернативной первой линии терапии рекомендуется использовать
вакуумные эректоры [45]. Половой член помещают в специальную колбу, где создают отрицательное давление с помощью вакуумного насоса. Это приводит к увеличению притока крови к пещеристым телам, что обусловливает эрекцию, для сохранения которой на основание полового члена накладывают специальное сжимающее кольцо, ограничивающее венозный отток. Эффективность метода и удовлетворённость им составляют от 27 до 94%. Примерно 30% пациентов отказываются от применения вакуумных устройств в связи с возникновением боли, подкожных кровоизлияний, затруднённой эякуляции и снижения чувствительности головки полового члена [45, 46].
При отсутствии эффекта от комбинированной терапии в качестве препаратов второй линии терапии ЭД применяются интракавернозные инъекции вазоактивных препаратов. Для проведения интракавернозных инъекций используются алпростадил и его аналоги [47, 48]. Эффективность данной терапии составляет около 85%.
При ЭД сосудистого и смешанного генеза начальная дозировка алпростадила составляет 2,5 мкг. Вторая инъекция может быть в дозе 5–7,5 мкг. Шаг последующего увеличения дозировок варьирует от 5 до 10 мкг. Препарат растворяют в 1 мл 0,9%-ного раствора натрия хлорида.
Начальная доза алпростадила у пациентов с ЭД на фоне повреждений спинного мозга составляет 1,25 мкг. Дозировка второй и третьей инъекций в таких случаях составляет 2,5 и 5 мкг соответственно. Шаг последующего увеличения доз у пациентов данной категории равен 5 мкг.
Эрекция наступает через 5–15 мин после введения препарата, её продолжительность зависит от дозы, составляя в среднем около 90 мин. После подбора необходимого количества препарата и соответствующего обучения пациента переводят на выполнение аутоинъекций, частота их не более 3 раз в неделю.
Осложнения: боль в половом члене, приапизм, кавернозный фиброз. Боль облегчается при использовании раствора натрия гидрокарбоната и анестезии. Данная терапия противопоказана пациентам при повышенной чувствительностью к используемому препарату; с риском развития приапизма; с грубыми анатомическими дефектами полового члена.
Пациента нужно предупредить, что в случае сохранения эрекции более 4 ч ему необходимо обратиться к врачу [49].
В случае получения удовлетворительного эректильного ответа при использовании лекарственной и нелекарственной терапии на следующем этапе требуется закрепление успеха проводимого лечения с формированием эректильной психологической доминанты, которая формируется в течение 3–4 месяцев при условии 100%-ного клинического эректильного ответа на используемые рабочие схемы.
В качестве третьей линии лечения пациентов с ЭД при неэффективности консервативной терапии, а также в случае желания пациента рекомендуется применять фаллопластику с протезированием полового члена ригидным протезом или трёхкомпонентным протезом полового члена [7, 33, 34]. Большинство пациентов предпочитают трёхкомпонентный протез в силу достижения более натуральной эрекции. Удовлетворенность половой жизнью после их имплантации отмечают свыше 90% прооперированных пациентов и их партнерш.
Литература
- Korneyev I.A., Alexeeva T.A., Al-Shukri S.H., et al. Prevalence and risk factors for erectile dysfunction and lower urinary tract symptoms in Russian Federation men: analysis from a national population-based multicenter study. // International journal of impotence research. England, 2016. Vol. 28, № 2. P. 74–79.
- EAU Guidelines. Edn. presented at the EAU Annual Congress Milan, Italy 2023. ISBN 978-94-92671-19-6. Kouidrat Y., Pizzol D., Cosco T., et al. High prevalence of erectile dysfunction in diabetes: a systematic review and meta-analysis of 145 studies. // Diabetic medicine : a journal of the British Diabetic Association. England, 2017. Vol. 34, № 9. P. 1185–1192.
- Besiroglu H., Otunctemur A., Ozbek E. The relationship between metabolic syndrome, its components, and erectile dysfunction: a systematic review and a meta-analysis of observational studies. // The journal of sexual medicine. Netherlands, 2015. Vol. 12, № 6. P. 1309–1318.
- Corona G., Rastrelli G., Morgentaler A., et al. Meta-analysis of Results of Testosterone Therapy on Sexual Function Based on International Index of Erectile Function Scores. // European urology. Switzerland, 2017. Vol. 72, № 6. P. 1000–1011.
- Navaneethan S.D., Vecchio M., Johnson D.W., et al. Prevalence and correlates of self-reported sexual dysfunction in CKD: a meta-analysis of observational studies. // American journal of kidney diseases: the official journal of the National Kidney Foundation. United States, 2010. Vol. 56, № 4. P. 670–685.
- Глыбочко П.В., Аляев Ю.Г., Чалый М.Е., et al. Половые расстройства у мужчин. ГЭОТАР-Ме. Москва, 2012.
- Rosen R.C., Cappelleri J.C., Smith M.D., et al. Development and evaluation of an abridged, 5-item version of the International Index of Erectile Function (IIEF-5) as a diagnostic tool for erectile dysfunction. // International journal of impotence research. England, 1999. Vol. 11, № 6. P. 319–326.
- Rosen R.C., Riley A., Wagner G., et al. The international index of erectile function (IIEF): a multidimensional scale for assessment of erectile dysfunction. // Urology. United States, 1997. Vol. 49, № 6. P. 822–830.
- Лоран О.Б., Сегал А.С. Шкала количественной оценки мужской копулятивной функции (шкала МКФ) // Урология и нефрология. 1998. № 5. P. 24–27.
- Gray J.S., Petros T., Stupnisky R. Confirmatory factor analysis of Beck Depression Inventory-II with two American Indian samples. // The American journal of orthopsychiatry. United States, 2023. Vol. 93, № 4. P. 316–320.
- Мазо Е.Б., Жуков О.Б., А.Р. З. Виагра-тест в ультразвуковой диагностике васкулогенной эректильной дисфункции // РМЖ. 2003. № 24. P. 1333.
- Ghanem H.M., Salonia A., Martin-Morales A. SOP: physical examination and laboratory testing for men with erectile dysfunction. // The journal of sexual medicine. Netherlands, 2013. Vol. 10, № 1. P. 108–110.
- Maggi M., Buvat J., Corona G., et al. Hormonal causes of male sexual dysfunctions and their management (hyperprolactinemia, thyroid disorders, GH disorders, and DHEA). // The journal of sexual medicine. Netherlands, 2013. Vol. 10, № 3. P. 661–677.
- Nehra A., Jackson G., Miner M., et al. The Princeton III Consensus recommendations for the management of erectile dysfunction and cardiovascular disease. // Mayo Clinic proceedings. England, 2012. Vol. 87, № 8. P. 766–778.
- Giesbers A.A.G.M., Bruins J.L., Kramer A.E.J.L., et al. New methods in the diagnosis of impotence: RigiScan® penile tumescence and rigidity monitoring and diagnostic papaverine hydrochloride injection // World Journal of Urology. 1987. Vol. 5, № 3. P. 173–176.
- Chaliy M., Ohobotov D., Sorokin N., et al. A comparison of the international index of erectile function and measurement of nocturnal penile tumescence using the Androscan MIT device // Urological Science. 2023. Vol. 34, № 1. P. 18–22.
- Chaliy M.E., Ohobotov D.A., Sorokin N.I., et al. [Normative parameters for monitoring of nocturnal penile tumescences: a systematic review and algorithm development]. // Urologiia (Moscow, Russia : 1999). Russia (Federation), 2021. № 6. P. 110–117.
- LeRoy T.J., Broderick G.A. Doppler blood flow analysis of erectile function: who, when, and how. // The Urologic clinics of North America. United States, 2011. Vol. 38, № 2. P. 147–154.
- Altinbas N.K., Hamidi N. Penile Doppler ultrasonography and elastography evaluation in patients with erectile dysfunction. // Polish journal of radiology. Poland, 2018. Vol. 83. P. e491–e499.
- Sikka S.C., Hellstrom W.J.G., Brock G., et al. Standardization of vascular assessment of erectile dysfunction: standard operating procedures for duplex ultrasound. // The journal of sexual medicine. Netherlands, 2013. Vol. 10, № 1. P. 120–129.
- Mulhall J.P., Giraldi A., Hackett G., et al. The 2018 Revision to the Process of Care Model for Evaluation of Erectile Dysfunction. // The journal of sexual medicine. Netherlands, 2018. Vol. 15, № 9. P. 1280–1292.
- Андрология. Фармакология без ошибок под редакцией акад. РАН Камалова А.А. руководство для врачей.// Е-ното Подольск, 2017, ISBN 978-5-906023-15-5, 384 с.
- Lue T.F., Giuliano F., Montorsi F., et al. Summary of the recommendations on sexual dysfunctions in men. // The journal of sexual medicine. Netherlands, 2004. Vol. 1, № 1. P. 6–23.
- Gupta B.P., Murad M.H., Clifton M.M., et al. The effect of lifestyle modification and cardiovascular risk factor reduction on erectile dysfunction: a systematic review and meta-analysis. // Archives of internal medicine. United States, 2011. Vol. 171, № 20. P. 1797–1803.
- Frühauf S., Gerger H., Schmidt H.M., et al. Efficacy of psychological interventions for sexual dysfunction: a systematic review and meta-analysis. // Archives of sexual behavior. United States, 2013. Vol. 42, № 6. P. 915–933.
- Brotto L., Atallah S., Johnson-Agbakwu C., et al. Psychological and Interpersonal Dimensions of Sexual Function and Dysfunction. // The journal of sexual medicine. Netherlands, 2016. Vol. 13, № 4. P. 538–571.
- Hatzimouratidis K. Sildenafil in the treatment of erectile dysfunction: an overview of the clinical evidence. // Clinical interventions in aging. New Zealand, 2006. Vol. 1, № 4. P. 403–414.
- Yuan J., Zhang R., Yang Z., et al. Comparative effectiveness and safety of oral phosphodiesterase type 5 inhibitors for erectile dysfunction: a systematic review and network meta-analysis. // European urology. Switzerland, 2013. Vol. 63, № 5. P. 902–912.
- Peng Z., Yang L., Dong Q., et al. Efficacy and Safety of Tadalafil Once-a-Day versus Tadalafil On-Demand in Patients with Erectile Dysfunction: A Systematic Review and Meta-Analyses. // Urologia internationalis. Switzerland, 2017. Vol. 99, № 3. P. 343–352.
- Ahmed N.S. Tadalafil: 15 years’journey in male erectile dysfunction and beyond. // Drug development research. United States, 2018.
- Chung E., Broc G.B. A state of art review on vardenafil in men with erectile dysfunction and associated underlying diseases. // Expert opinion on pharmacotherapy. England, 2011. Vol. 12, № 8. P. 1341–1348.
- Hatzimouratidis K., Salonia A., Adaikan G., et al. Pharmacotherapy for Erectile Dysfunction: Recommendations From the Fourth International Consultation for Sexual Medicine (ICSM 2015). // The journal of sexual medicine. Netherlands, 2016. Vol. 13, № 4. P. 465–488.
- Chen L., Staubli S.E.L., Schneider M.P., et al. Phosphodiesterase 5 inhibitors for the treatment of erectile dysfunction: a trade-off network meta-analysis. // European urology. Switzerland, 2015. Vol. 68, № 4. P. 674–680. Rizk P.J., Kohn T.P., Pastuszak A.W., et al. Testosterone
- therapy improves erectile function and libido in hypogonadal men. // Current opinion in urology. United States, 2017. Vol. 27, № 6. P. 511–515.
- Xu J., Xu Z., Ge N., et al. Association between folic acid, homocysteine, vitamin B12 and erectile dysfunction-A cross-sectional study. // Andrologia. Germany, 2021. Vol. 53, № 11. P. e14234. https://www.vidal.ru/drugs/impaza 6968.
- Chung E., Wang J. A state-of-art review of low intensity extracorporeal shock wave therapy and lithotripter machines for the treatment of erectile dysfunction. // Expert review of medical devices. England, 2017. Vol. 14,
№ 12. P. 929–934.
- Alkhayal S., de Lourdes M. PO-01-091 Platelet rich plasma penile rejuvenation as a treatment for erectile dysfunction: An update // The Journal of Sexual Medicine. 2019.
- Ruffo A., Franco M., Illiano E., et al. Effectiveness and safety of Platelet rich Plasma (PrP) cavernosal injections plus external shock wave treatment for penile erectile dysfunction: First results from a prospective, randomized, controlled, interventional study // European Urology Supplements. 2019. Vol. 18. P. e1622–e1623.
- Chalyj M.E., Grigorjan V.A., Epifanova M. V, et al. The effectiveness of intracavernous autologous platelet-rich plasma in the treatment of erectile dysfunction. // Urologiia (Moscow, Russia : 1999). Russia (Federation), 2015.
№ 4. P. 76–79.
- Banno J.J., Kinnick T.R., Roy L., et al. 146 The Efficacy of Platelet-Rich Plasma (PRP) as a Supplemental Therapy for the Treatment of Erectile Dysfunction (ED): Initial Outcomes // The Journal of Sexual Medicine. 2017. Vol. 14. P. e59–e60.
- Artemenko S., Epifanova M. Combined therapy for treating erectile dysfunction: first results on the use of low-intensity extracorporeal shock wave therapy and platelet-rich plasma // BJU International. 2019. Vol. 123. P. 25.
- Oudelaar B.W., Peerbooms J.C., Huis In ’t Veld R., et al. Concentrations of Blood Components in Commercial Platelet-Rich Plasma Separation Systems: A Review of the Literature. // The American journal of sports medicine. United States, 2019. Vol. 47, № 2. P. 479–487.
- Brison D., Seftel A., Sadeghi-Nejad H. The resurgence of the vacuum erection device (VED) for treatment of erectile dysfunction. // The journal of sexual medicine. Netherlands, 2013. Vol. 10, № 4. P. 1124–1135.
- Yuan J., Hoang A.N., Romero C.A., et al. Vacuum therapy in erectile dysfunction--science and clinical evidence.
- // International journal of impotence research. England, 2010. Vol. 22, № 4. P. 211–219.
- Hanchanale V., Eardley I. Alprostadil for the treatment of impotence. // Expert opinion on pharmacotherapy. England, 2014. Vol. 15, № 3. P. 421–428.
- Minhas S., Bettocchi C., Boeri L., et al. European Association of Urology Guidelines on Male Sexual and Reproductive Health: 2021 Update on Male Infertility. // European urology. Switzerland, 2021. Vol. 80,
№ 5. P. 603–620.
- Coombs P.G., Heck M., Guhring P., et al. A review of outcomes of an intracavernosal injection therapy programme. // BJU international. England, 2012. Vol. 110, № 11. P. 1787–1791.









Комментарии