В.А. Божедомов
ФБГУ «Поликлиника №1» УДП РФ, Каф. акушерства, гинекологии, перинатологии и репродуктологии ФППОВ ГБОУ ВПО «Первый МГМУ им. И.М.Сеченова», каф. клинической андрологии ФПКМР ГБОУ ВПО «РУДН»;Москвы
Введение. По данным Всемирной Организации Здравоохранения 10-20% супружеских пар репродуктивного возраста страдают от отсутствия детей, и в половине случаев причиной бесплодия является та или иная патология у мужчины [28]. Учитывая неблагоприятную демографическую ситуацию в России, эта проблема требует особенного внимания всех отечественных специалистов, занимающихся вопросами репродукции: урологов-андрологов, гинекологов, эмбриологов, эндокринологов. Статья посвящена рассмотрению основных вопросов этиопатогенеза, диагностики и лечения нарушений репродуктивной функции мужчин на основе междисциплинарного подхода с учетом организационно-методических аспектов.
Этиопатогенез. Мужское бесплодие представляет собой многофакторный синдром, включающий широкий спектр нарушений, симптом множества различных патологических состояний, затрагивающих как половую, так и другие системы организма: эндокринную, нервную, кровеносную, иммунную [1, 6, 8, 11, 17, 20, 21]. Собственный опыт и данные публикаций обобщены нами в таблицах 1 и 2.
Таблица 1. Этиология и распространенность различных форм мужского бесплодия, %
| Причины бесплодия | WHO, 2000 (n=7053) | Nieschlag E., Behre H.M. (Eds.), 2010 (n=12945) | Божедомов В. и соавт., 2004 (n=2800) |
| Сексуальные дисфункции | 1.7 | 2.4 | 0.5 |
| Урогенитальные инфекции | 6.6 | 9.3 | 32.0 |
| Врожденные аномалии развития (гермафродитизм, крипторхизм и др.) | 2.1 | 11.2 | 7.2 |
| Действие неблагоприятных внешних факторов | 2.6 | - | 7.0 |
| Варикоцеле | 12.3 | 14.8 | 27.4 |
| Эндокринные нарушения | 0.6 | 10.1 | 2.5 |
| Иммунологический фактор | 3.1 | 3.9 | 17.5 |
| Другие ненормальности | 3.0 | 8.5 | 5.0 |
| Идиопатические нарушения | 75.1 | 30.0 | 38.0 |
Из представленных данных видно, что в недавнем прошлом в России существенно чаще, чем странах Европы и Америки, причиной снижения качества спермы мужчин были инфекционно-воспалительные и аутоиммунные процессы в репродуктивной системе, вредные факторы внешней среды и образа жизни (курение, злоупотребление алкоголем и др.).
Таблица 2. Причины снижения мужской репродуктивной функции
| Нарушения эякуляции |
|
| Воздействия окружающей среды |
перегревание
|
| Приобретенные |
|
| Анатомические |
|
| Аномалии развития и строения |
|
| Нарушения качества спермы |
|
| Гормональные причины и нечувствительность к андрогенам |
|
| Идиопатические причины |
|
Важно, что одни и те же факторы риска в зависимости от генетических особенностей мужчин могут либо снижать фертильность, либо нет. Например, в качестве предрасполагающих факторов бесплодия при варикоцеле описаны микроделеции некоторых митохондриальных генов, недостаточность белков теплового шока, экспрессии каспаз, Bak, р53 и ряда других факторов, противостоящих оксидативному стрессу и нарушающих соотношение пролиферация-апоптоз, аутоиммунные реакции против сперматозоидов [3, 12, 16, 18]. Факторами риска развития бесплодия при хроническом простатите является присутствие в сперме Anaerococcus, нарушение равновесия активация/апоптоз спермальных лейкоцитов, степень гиперпродукции активных форм кислорода (АФК), сочетание с синдромом раздражения толстой кишки и др. [4, 10, 19].
В последние годы стало ясно, что плохое качество сперматозоидов – причина не только отсутствия беременности, но также нарушений развития зародыша, врожденных аномалий и даже рака у детей [11, 20, 21, 24]. В основе этого лежат – нарушения структуры хроматина сперматозоидов [2, 21, 24]. Вероятность оплодотворения in vivo и при внутриматочной инсеминации близка к нулю, если количество сперматозоидов с повреждением (фрагментацией) ДНК превышает 25-30%; до 40% выкидышей может быть предсказано с помощью оценки целостности спермальной ДНК. Между фрагментацией ДНК и процентом патологических форм имеется положительная корреляция, с подвижностью – отрицательная, но повышенная фрагментация ДНК может иметь место даже при «нормозооспермии» [2, 21, 22, 24, 26].
Различные функциональные характеристики сперматозоидов, нарушения которых приводит к снижению фертильности и аномалиям развития зародыша, отражены на рисунке 1.
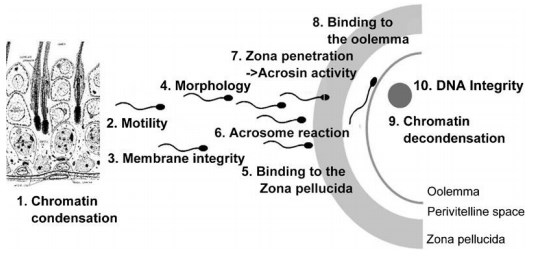
Рис.1. Показатели функции сперматозоидов, характеризующие фертильность мужчин
Обследование мужчин из вынужденно бездетных пар
Стандартизированный подход к обследованию пациентов, четкие принципы и алгоритм диагностики причин, лежащих в основе бесплодия, описаны в Руководстве ВОЗ [28], уточнены и дополнены в последующих Руководствах и монографиях [1, 6, 8, 11, 17, 20, 21]. Причины в большинстве случаев (в 60-70%) удается выявить при тщательном сборе анамнеза, физикальном обследовании, проведении анализа спермы, специальных гормональных, генетических, микробиологических и других исследованиях. В частности, в соответствии с современными требованиями андрологическая лаборатория должна выполнять анализ спермы, включающий: оценку жизнеспособности и подвижности сперматозоидов, признаков воспаления (лейкоциты, эластаза, активные формы кислорода), антиоксидантную активность эякулята, повреждения ДНК сперматозоидов, антиспермальных антитела (АСАТ), делать анализ постэякуляторной мочи, оценивать взаимодействие сперматозоидов с цервикальной слизью и другие функциональные тесты [23, 27].
Естественно, объем обследования и методическая оснащенность лабораторий должны отличаться в различных ЛПУ. По нашему мнению, с позиций организации здравоохранения можно выделить три уровня обследования и, соответственно, оснащения.
Первый является обязательным для всех ЛПУ, имеющих в своем составе кабинет уролога. Он включает:
- первичное обследование мужчины, обратившегося к урологу поликлиники в связи с отсутствием желаемой беременности у постоянной половой партнерши (жалобы, анамнез, физикальное обследование);
- выполнение минимального лабораторного обследования мужчины, планирующего отцовство (анализы крови на ВИЧ (с согласия пациента), вирусные гепататы В и С, сифилис, мазок из уретры);
- УЗИ органов мошонки, предстательной железы и семенных пузырьков.
Второй является обязательным для всех ЛПУ, в той или иной форме занимающихся проблемой бесплодного брака андрологических кабинетов окружных (кустовых, районных и т.п.) урологических амбулаторно-поликлинических отделений, в т.ч. системы УДП РФ, консультаций «Брак и семья», центров планирования семьи и репродукции. Он включает:
- стандартную спермограмму, в т.ч. окраску сперматозоидов специальными красителями и «строгую» оценку морфологии;
- определение АСАТ на подвижных сперматозоидах (MARили IBT-тест);
- выявление инфекционно-воспалительных процессов репродуктивного тракта (лейкоциты в сперме и секрете простаты, при необходимости – микробиологическое и молекулярно-генетическое исследование на инфекции);
- гормональные (определение ФСГ, пролактина, ингибина В, тестостерона, андрогенсвязывающего глобулина и др.).
Это позволяет выделить группу мужчин с нарушениями качества спермы и направить их для более углубленного обследования в специализированные клиники третьего уровня, где должны быть проведены дополнительные исследования:
- генетические (кариотипирование, диагностика микроделеций и точечных мутаций AZF, муковисцидоза, полиморфизма рецепторов андрогенов и др.);
- биохимические исследования эякулята (фруктоза, цитрат, цинк, альфа-гликозидаза, акрозин и др.);
- оценка взаимодействия сперматозоидов с цервикальной слизью in vivo и in vitro;
- гипо-осмотический тест;
- оценка акросомой реакции (иммунофлюоресценция, проточная цитометрия);
- измерение продукции активных форм кислорода (хемилюминесценция);
- оценка фрагментации ДНК (TUNEL, COMET, SCD);
- оценка нарушений упаковки и конденсации хроматина (CMA3, AB, AO);
- комплексное исследование «отмытых» в градиенте Перкола сперматозоидов.
Урологи-андрологи кабинетов второго и третьего уровней должны владеть специальными теоретическими знаниями и практическими навыками, позволяющими целенаправленно выявлять патологические состояния, приводящие к снижению фертильности мужчины, назначать соответствующую терапию, при необходимости выполнять оперативные пособия, а также проводить отбор пациентов для вспомогательных репродуктивных технологий (ВРТ).
Установление конкретных патогенетических механизмов нарушения мужской репродуктивной функции позволяет шире использовать возможности специфической терапии, повысить ее эффективность и снизить стоимость.
Сохранение и восстановление репродуктивной функции мужчин
Рекомендации по лечению мужчин из бездетных пар представлены во многих Руководствах, монографиях и статьях [1, 6, 8, 11, 17, 20, 21 и др.]. Но имеющиеся на сегодняшний день данные противоречивы и недостаточно надежны с точки зрения доказательной медицины. Стандарты помощи бездетным парам с мужским фактором не существуют ни в одной стране мира.
По нашему мнению, ведение мужчин из бездетных пар следует рассматривать в виде трех взаимосвязанных этапов комплексной профилактики нарушений репродуктивной функции.
I этап: первичная профилактика устранение потенциально вредных факторов окружающей среды, работы и образа жизни (см. табл.2). При некоторых аномалиях, например, крипторхизме, травмах, инфекциях, действии токсических веществ и лекарственных препаратов бесплодие можно предотвратить.
Для восстановления фертильности мужчин необходимо:
- наладить нормальный ритм труда и отдыха, полноценное питание, лечение сопутствующих заболеваний, ритм половой жизни;
- исключить перегревание, снизить физические нагрузки при занятиях экстремальными видами спорта;
- устранить факторы, вызывающие депрессию, состояние страха, неврозы.
Выполнение этих условий во многих случаях способствует улучшению показателей спермограммы.
II этап: вторичная профилактика – адекватное обследование и патогенетическое лечение.
Методы обследования, необходимые для постановки обоснованного диагноза, описаны выше.
В ряде случаев возможно этиотропное лечение: при инфекционно-воспалительных заболеваниях, варикоцеле, непроходимости семявыносящего тракта, гиперпролактинемии при опухолях гипофиза и др. [1, 6, 8, 11, 17, 20, 21].
Во многих случаях возможно патогенетическое лечение: при гипогонадотропном гипогонадизме, оксидативном стрессе, секреторной недостаточности дополнительных половых желез, сексуальной и эякуляторной дисфункций и др. [1, 5, 6, 8, 11, 17, 20, 21].
Поскольку во многих случаях патогенез снижения фертильности мужчин не ясен (чаще из-за недостаточного объема обследования), применяют т.н. «эмпирическую терапию»: карнитины, витамины А, В и С, калликреин, инозин, альфа-адренергические агонисты (клонидин), альфа-блокаторы (буназозин) и др. [1, 6, 8, 11, 17, 20, 21]. Ни для одного из методов эмпирической терапии эффективность с точки зрения доказательной медицины не подтверждена, но опыт показывает, что эти препараты могут быть рекомендованы определенным группам пациентов, если удается понять реальный патогенез ухудшения качества спермы. Например, антиоксиданты при оксидативном стрессе; антиэстрогены – при сниженном уровне гонадотропинов и наличии ответа гипофиза; карнитины, фруктоза, лимонная кислота – при функциональной недостаточности придатка яичек, семенных пузырьков и простаты.
В ряде случаев этиопатогенетическое лечение кажется невозможным: при врожденном отсутствии семявыносящего протока, после лечения онкологических заболеваний цитостатиками, при микроделеции в локусе AZFc и других генетических нарушениях, приводящих к гипосперматогенезу. В этом случае рекомендованы методы ВРТ, в первую очередь ИКСИ.
Последние годы появились биомедицинские клеточные технологии, которые позволяют снять блок сперматогенеза – т.н. «арест» сперматогенеза, и на некоторое время обеспечить его завершение до образования зрелых сперматозоидов [8]. Однако первопричина – генетические нарушения, при этом не устраняется, и сперматозоиды могут передать потомству дефектный ген.
Продолжительность этиопатогенетического и эмпирического лечения не должна быть больше 1-2 лет. В случаях, когда этиопатогенетическое лечение оказалось не эффективным (или невозможно) используют симптоматическое лечение. Применительно к лечению мужского бесплодия это методы ВРТ, в первую очередь ЭКО ИКСИ [7]. За 20 лет технология ЭКО ИКСИ доказала свою эффективность – при мужском факторе бесплодия после 3-4 циклов дети рождаются у половины пар [8, 9, 11, 20, 21].
В ряде случаев лечение невозможно: при нечувствительности к андрогенам, микроделециях в локусах AZFa и b, других генетических дефектах, приводящих к синдрому «только клетки Сертоли». В этом случае паре должны быть предложены альтернативные способы достижения социального отцовства: инсеминация донорской спермой или усыновление.
III этап: третичная профилактика – уменьшение осложнений симптоматического лечения.
При ВРТ возможны осложнения: в 15-20% вследствие стимуляции суперовуляции, в 35% после пункции [8, 9, 11, 21]. Самый сложный вопрос – здоровье детей после ИКСИ. «…Дети, рожденные после оплодотворения по методу ИКСИ, подвержены более высокому риску хромосомных аберраций de novo (в три раза по сравнению с детьми, зачатыми естественным путем) и наследуемых структурных хромосомных аномалий. ЭКО было сопряжено с повышенным риском сердечно сосудистых, скелетно-мышечных, мочеполовых и желудочнокишечных нарушений и детского церебрального паралича…» отмечают эксперты Европейской урологической ассоциации [17] со ссылкой не несколько опубликованных работ [13, 14, 25]. Пока не ясно, является это следствием ВРТ, или отражает особенности популяции, включенных в ВРТ [15].
Следует иметь виду, что методы ВРТ – способ преодоление бесплодия, который не устраняет факторов, приводящих к привычному спонтанному аборту на ранних сроках, в том числе обусловленному плохим качеством сперматозоидов. Использование методов ВРТ не исключает, а дополняет применение патогенетического лечения, которое, по возможности, должно проводиться в течение осуществления всей программы ВРТ.
Заключение. Установление конкретных патогенетических механизмов нарушения мужской репродуктивной функции позволяет шире использовать возможности специфической терапии, повысить ее эффективность и снизить стоимость. Реализация предлагаемого алгоритма ведения мужчин из бездетных пар подразумевает совершенствование работы системы ЛПУ, в т.ч. системы УДП РФ, создание специальных подразделений уроандрологического, гинекологического, клинико-лабораторного профиля, тесно взаимодействующих между собой, и их соответствующего оснащения. Необходима программа последипломного повышения квалификации урологов по андрологии для усвоения необходимых знаний, в т.ч. из смежных дисциплин: эндокринологии, дерматовенерологии, сексологии, гинекологии, эмбриологии, иммунологии, генетики. «Мужской фактор» следует рассматривать не только в качестве частой причины бесплодного брака, но и фактора риска невынашивания беременности, т.е. вынужденно бездетного брака.
Литература
1. Божедомов В.А. Мужское бесплодие / Андрология. Клинические рекомендации / Под ред. П.А.Щеплева, 2012: 30-58.
2. Божедомов В.А., Липатова Н.А., Спориш Е.А., и соавт. // Андрология и генитальная хирургия.2012.№3.С.83-91.
3. Божедомов В.А., Николаева М.А., Ушакова И. В. и соавт. // Акушерство и гинекология. – 2012. -№8/2. – С.64-69
4. Божедомов В.А., Семенов А.В., Сотникова Н.Ю. и соавт. // Андрология и генитальная хирургия.2013. №2. – С.85-86.
5. Божедомов В.А., Ушакова И. В., Торопцева М. В. и соавт. //Урология.2009.№2.С.51-56.
6. Оль Д., Шустер Т., Кволич С. Мужское бесплодие // Репродуктивная медицина и хирургия / Под ред. Т.Фальконе, В.Херд, 2013: 616-631.
7. Приказ Министерства здравоохранения РФ от 30 августа 2012 г. N 107н «О порядке использования вспомогательных репродуктивных технологий, противопоказаниях и ограничениях к их применению».
8. Сухих Г.Т., Божедомов В.А. МУЖСКОЕ БЕСПЛОДИЕ. Практическое руководство для урологов и гинекологов, М.: Эксмо, 2009; 240 с ил. – Медицинская практика.
9. Экстракорпоральное оплодотворение и его новые направления в лечении женского и мужского бесплодия / под ред. Кулакова В.И., Леонова Б.В. М, 2000, 781.
10. Alshahrani S, McGill J, Agarwal A. // J. Reprod. Immunol.2013.№9. [Epub ahead of print]
11. Andrology: Male Reproductive Health and Disfunction. 3rd. E.Nieschlag., H.M.Behre, S.Nieschlag (Ed.), 2010; 629.
12. Chang FW, Sun GH, Cheng YY, et al. // Andrologia. -2010.V.42,№4. – Р.225-230.
13. Davies MJ, Moore VM, Willson KJ et al. // N. Engl. J. Med.2012.V.366/ P.1803-1813.
14. ESHRE Capri Workshop group Intracytoplasmic sperm injection (ICSI) in 2006: evidence and evolution. Hum Reprod Update. 2007; 13(6): 515-26.
15. Feuer SK, Camarano L, Rinaudo PF. //Mol Hum Reprod. – 2013. – V.19, №4. – P.189204.
16. Gashti NG, Salehi Z, Madani AH, Dalivandan ST. // Andrologia. – 2013.V.20 [Epub ahead of print]
17. Guidelines on Male Infertility / A. Jungwirth, T. Diemer, G.R. Dohle et al. (Ed.) © European Association of Urology 2013; 60.
18. Guo SJ, Sun ZJ, Li W. // Med Hypotheses. – 2012. – V.78, №4.P.536-538.
19. Hou D, Zhou X, Zhong X, et al. //Fertil Steril. – 2013. – V.29. [Epub ahead of print]
20. Infertility in the male. Fourth ed. / L.I.Lipshults, S.S.Howards, C.S.Niederberger (Ed.), 2009; 677.
21. Male infertility / S.J.Parekattil, A.Agarwal (Ed.), 2012, Springer; 518.
22. Robinson L. et al. // Hum. Reprod.2012. – V.27, №10. – P.2908-2917.
23. Snow-Lisy D, Sabanegh E Jr. // Front Biosci (Elite Ed).2013. – V.1, №5. – P.289-304.
24. Sperm chromatin: biological and clinical application in male infertility and assisted reproduction / A.Zini, A.Agarwal (Ed.), 2011, Springer, 512. 34
25. Van Steirteghem A, Bonduelle M, Devroey P, et al. // Hum. Reprod. Update.2002.V.8, №2. – P.111-116.
26. Varshini J, Srinag BS, Kalthur G, et al. // Andrologia.2012. – V.44. – P.642-649.
27. WHO laboratory manual for the examibation and processing of human semen. Fifth ed., WHO, 2010; 271.
28. WHO Manual for the Standardized Investigation, Diagnosis and Management of the Infertile Male. Cambridge: Cambridge University Press, 2000; 91.









Комментарии