В.К. Карпов1,3, Б М. Шапаров 1,2
1Факультет фундаментальной медицины МГУ им. М.В. Ломоносова, кафедра урологии и андрологии, Москва, Россия |
2МНОЦ МГУ им. М.В. Ломоносова, Москва, Россия
3ГБУЗ «ГКБ №31 ДЗМ», Москва, Россия
Мы продолжаем работу рубрики «Рентгенэндоваскулярные методы диагностики и лечения в урологии». Сегодня мы продолжим разговор об одном из наиболее перспективных малоинвазивных способов лечения гиперплазии простаты – эмболизация простатических артерий.

Карпов В.К.
к.м.н., врач-уролог ГКБ №31 ДЗМ, доцент кафедры
урологии и андрологии ФФМ МГУ
им. М.В. Ломоносова, ведущий
научный сотрудник отдела урологии
и андрологии МНОЦ МГУ
им. М.В. Ломоносова
Шапаров Б.М.
врач-уролог
ГКБ №17 ДЗМ, аспирант кафедры
урологии и андрологии ФФМ МГУ
им. М.В. Ломоносова
Введение
Эмболизация артерий предстательной железы (ПЖ) – эффективный и безопасный рентгенэндоваскулярный метод лечения пациентов с доброкачественной гиперплазией ПЖ (ДГПЖ). Данная методика описана в клинических рекомендациях Минздрава РФ по лечению больных ДГПЖ и рекомендована к применению в США и Европе [1].
Артерии малого таза могут иметь сложную анатомию, разные варианты ветвления, а также анастомозы с другими ветвями внутренней подвздошной артерии (ВПА). Этим обусловлена техническая сложность идентификации и катетеризации простатических артерий (ПА), а также возможность развития осложнений, связанных с нецелевой эмболизацией анастомозов ПА.
В данной статье мы подробно рассмотрим наиболее распространенные варианты кровоснабжения ПЖ и различные способы идентификации ПА.
Ангиоархитектоника органов малого таза
Органы малого таза кровоснабжаются ветвями ВПА. Обычно это короткая (около 3–4 см в длину) артерия, которая разветвляется на 2 больших ствола – передний и задний, дальнейшее разветвление которых очень вариабельно. Как правило, задний ствол дает начало верхней ягодичной (a. glutea superior), подвздошно-поясничной (a. iliolumbalis) и боковым крестцовым артериям (a. sacralis lateralis). От переднего ствола отходят верхняя (ВПА, a.vesicalis superior) и нижняя (НПА, a.vesicalis inferior) пузырные артерии, запирательная артерия (a. obturatorius), средняя прямокишечная (a. rectalis media), нижняя ягодичная (a. glutea inferior) и внутренняя половая (a. pudenda interna) артерии. ПА (a. prostatica) могут иметь множество вариантов отхождения, различаться по числу и особенностям строения [2].
По данным T. Bilhim и соавт. [3], в группе из 75 пациентов наиболее частым вариантом отхождения a. prostatica было отхождение общим стволом с a. vesicalis inferior (везикопростатический ствол, tr. vesicoprostatici) от средней трети a. pudenda interna (34,1%). Далее по частоте встречаемости расположились: отхождение общим стволом с a. vesicalis superior (20,1%), отхождение от общего ягодично-полового ствола (17,8%), от a. obturatorius (12,6%) и отхождение общим стволом с a. rectalis media (8,4%). Редким вариантом были нижняя ягодичная артерия (3,7%), добавочная половая артерия (1,9%) и верхняя ягодичная артерия (1,4%).
На основе анализа ангиоархитектоники малого таза у 173 пациентов de Assis и соавт. [4] под руководством F.C. Carnevale предложили анатомическую классификацию отхождения ПА (табл. 1).
D. Maclean и соавт. [5] при анализе КТ-ангиографий малого таза у 110 пациентов сообщили о том, что только 53 (48,2%) из них имели одинаковую конфигурацию ПА с обеих сторон. Анализ ангиоархитектоники малого таза показал применимость классификации по F.C. Carnevale в клинической практике (табл. 2).
По данным С.А. Капранова [5], при анализе ангиоархитектоники в группе из 168 пациентов наиболее частым вариантом отхождения ПА была внутренняя срамная артерия (30,9%), за которой следовали передняя порция ВПА (27,9 %), нижняя ягодичная артерия (17,2%) и запирательная артерия (14,3%). Более редкими анатомическими вариантами была средняя прямокишечная артерия (5,4%), верхняя пузырная артерия (2,3%) и др. (табл. 3).
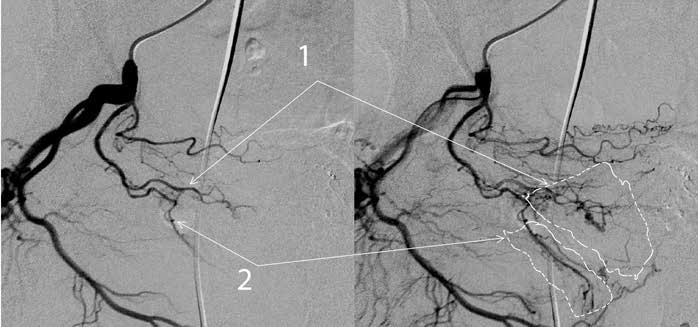
Кровоснабжение ПЖ обычно осуществляется двумя основными артериальными ветвями: переднемедиальной, или краниальной ветвью, которая питает центральную часть железы, включая среднюю долю, и заднебоковой, или каудальной ветвью, которая кровоснабжает периферическую зону и верхушку (рис. 1). В большинстве случаев эти 2 ветви происходят из общего ствола, однако они могут возникнуть из независимых источников, что имеет важные технические последствия. T. Bilhim и соавт. [3] в своем исследовании выявили одну ПА в 57% случаев и две независимых ПА в остальных 43%.
Анастомозы ПА
ПА имеют анастомозы с другими артериями органов малого таза в 57% случаев [3]. Большинство из этих анастомозов характеризуются низкой текучестью и идентифицируются на ангиограмме только при инъекции рентгенконтрастного препарата под давлением. Однако некоторые из анастомозов могут быть клинически значимыми, ввиду гемодинамической проходимости и сообщения с пузырными, прямокишечными артериями, артериями полового члена и концевыми разветвлениями внутренней половой и запирательной артериями. Также возможно наличие внутрипростатических междолевых артериальных анастомозов (рис. 2) [7].



Нецелевая миграция эмболизационного препарата через эти анастомозы, а также ретроградный сброс эмболизационных частиц обусловливают клинические проявления осложнений данной группы.
Правильная предоперационная подготовка, планирование этапов операции и рациональная интраоперационная тактика позволяют улучшить результаты выполнения суперселективной эмболизации ПА, а также избежать возможных осложнений.
Методы визуализации и навигации
Чрезвычайно сложная ангиоархитектоника малого таза, вариабельность отхождения ПА, а также наличие анастомозов с другими артериями значительно затрудняют выполнение суперселективной эмболизации ПА. Поэтому для повышения эффективности и безопасности эмболизации артерий ПЖ (ЭПА) большое значение имеет применение методов пред- и интраоперационной визуализации.
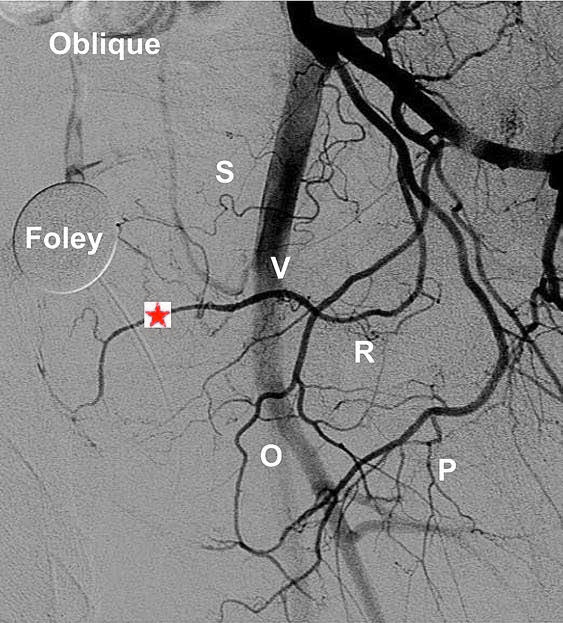
Для облегчения интраоперационной рентгеннавигации может быть применен алгоритм идентификации ПА – PROVISO (a. pudenda interna – внутренняя срамная артерия, a. rectalis media – средняя прямокишечная артерия, a. obturatoria – запирательная артерия, a. vesicalis inferior – НПА, a. vesicalis superior – ВПА и obligue view –косая проекция). На этапе освоения ЭПА также может использоваться установка ориентировочного уретрального катетера, баллон которого раздут разведенным рентгенконтрастным препаратом (рис. 3) [8].
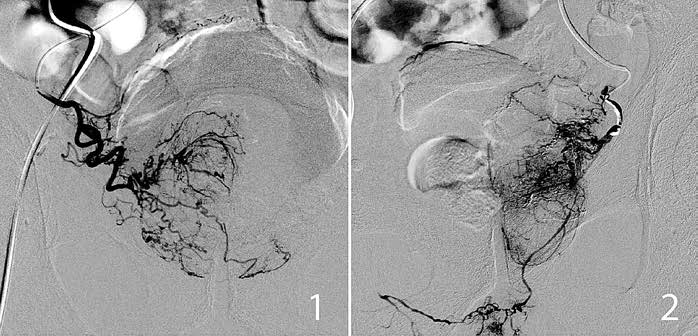
Предоперационная визуализация с помощью МСКТ- и МРТ-ангиографии малого таза позволяет сократить длительность операции и время флуороскопии. D. Maclean и соавт. [5] сообщают об опыте сопоставления МСКТ-ангиографии с интраоперационной цифровой субтракционной ангиографией в группе из 110 пациентов. ПА была успешно идентифицирована в 97,3% наблюдений. В отношении идентификации анастомозов МСКТ-ангиография продемонстрировала чувствительность в 59% и специфичность в 94,2%. По данным A.Y. Kim и соавт. [9], с помощью МРТ-ангиографии удалось идентифицировать ПА в 79,4% наблюдениях, в 87% наблюдениях из них удалось правильно определить вариант отхождения ПА. По данным С.А. Капранова [6], применение предоперационной МСКТ-ангиографии в сочетании с интраоперационной цифровой субтракционной ангиографией позволило определить вариант отхождения ПА у всех пациентов (168 пациентов, 336 сторон мужского таза). Одна ПА выявлена в 307 (91,4%) случаях с тазовых сторон, 2 независимые ПА – в 29 (8,6%) наблюдениях. Симметричный вариант отхождения ПА с обеих сторон выявлен у 24 (14,3%) пациентов, у остальных 144 (85,7%) пациентов выявлена асимметричность с двух сторон.
Интраоперационное применение плос-кодетекторной (ПДКТ) и конусно-лучевой КТ увеличивает лучевую нагрузку на пациента, но позволяет более эффективно визуализировать анастомозы ПА за счет комбинирования КТ и таргетного контрастирования (рис. 4). В исследовании M.Q. Wang и соавт. [10] с участием 148 пациентов применение конусно-лучевой КТ позволило идентифицировать отхождение ПА в 94,7% наблюдений и выявить ее анастомозы у 97% пациентов.
Заключение
ЭПА – это эффективный и безопасный малоинвазивный способ лечения больных ДГПЖ. Артерии малого таза обладают чрезвычайно вариабельной анатомией. Для улучшения результатов лечения необходимо детальное понимание особенностей ангиоархитектоники органов малого таза и самой ПА. В качестве эффективного метода визуализации может применяться предоперационная МСКТ-ангиография артерий малого таза.
Литература
- EAU Guidelines. Edn. presented at the EAU Annual Congress Amsterdam 2020. ISBN 978-94-92671-07-3.
- Carnevale F.C., Soares G.R., de Assis A.M., et al.Anatomical Variants in Prostate Artery Embolization: A Pictorial Essay. Cardiovasc. Intervent. Radiol. 2017;40(9):1321–37. doi: 10.1007/s00270-017-1687-0. [Epub 2017 May 15. PMID: 28508252].
- Bilhim T., Pisco J.M., Rio Tinto H., et al. Prostatic arterial supply: anatomic and imaging findings relevant for selective arterial embolization. J. Vasc. Interv. Radiol. 2012;23:1403–15.
- de Assis A.M., Moreira A.M., de Paula Rodrigues V.C., et al. Pelvic arterial anatomy relevant to prostatic artery embolization and proposal for angiographic classification. Cardiovasc. Intervent. Radiol. 2015;38:855–61.
- Maclean D., Maher B., Harris M., et al. Planning Prostate Artery Embolisation: Is it Essential to Perform a Pre-procedural CTA? Cardiovasc. Intervent. Radiol. 2018;41:628–32.
- Капранов С.А., Златовратский А.Г., Карпов В.К. и др. Варианты кровоснабжения простаты при выполнении суперселективной эмболизации простатических артерий. Вестн. урологии. 2021;9(3):32–43.
- Garcia-Monaco R., Garategui L., Kizilevsky N., et al. Human cadaveric specimen study of the prostatic arterial anatomy: implications for arterial embolization. J. Vasc. Interv. Radiol. 2014;25:315–22.
- Капранов С.А., Камалов А.А., Карпов В.К. и др. Эндоваскулярные вмешательства при доброкачественной гиперплазии предстательной железы. Национальное руководство: в 3 т. Рентгенэндоваскулярная хирургия под ред. Б.Г. Алекяна. М., 2017, т. 3. С. 531–45.
- Kim A.Y., Field D.H., De Mulder D., et al. Utility of MR angiography in the identification of prostatic artery origin prior to prostatic artery embolization. J. Vasc. Interv. Radiol. 2018;29(3):307–10.
- Wang M.Q., Duan F., Yuan K., et al. Benign prostatic hyperplasia: cone-beam CT in conjunction with DSA for identifying prostatic arterial anatomy. Radiology. 2017;282(1):271–80.









Комментарии