С.А. Пульбере1, И.И. Бабиченко2, С.В. Котов1, Р.И. Гуспанов1
1 ФГБОУ ВО«Российский национальный исследовательский медицинский университет имени Н.И. Пирогова» МЗ РФ; Москва, Россия
2 ФГБОАУ ВО«Российский университет дружбы народов» МЗ РФ; Москва, Россия
Автор для связи: Пульбере Сергей Александрович
Тел.: +7 (926) 581-46-47; e-mail: pulpiv@mail.ru
Введение
Учитывая глобальное постарение населения, в том числе мужского, проблема дифференциальной диагностики и прогноза болезней предстательной железы у мужчин старше 40 лет в ближайшем будущем не утратит своей остроты. Рак предстательной железы (РПЖ) является одним из самых распространенных заболеваний у мужчин. Как свидетельствуют статистические данные, в 2015 г. в России РПЖ впервые диагностирован у 38812 пациентов, при этом прирост заболеваемости с 2005 г. составил 135%. В структуре смертности от злокачественных новообразований в 2015 г. в России РПЖ составил 7,6%, с 2005 по 2015 гг. прирост 42% [1]. Диагностическая ценность комплекса рутинных методов обследования пациентов с болезнями предстательной железы в настоящее время преимущественно определяется исследованием уровня простат-специфического антигена (ПСА) и его фракций, ТРУЗИ, пальцевого ректального исследования и МРТ, обладающих довольно низкой специфичностью.
Количество ложноотрицательных результатов при первичной биопсии простаты достигает 30%. Проводятся многочисленные исследования с внедрением в широкую практику различных методов для выявления данного новообразования на стадии локализованного процесса, однако диагностика поздних стадий и смертность от рака предстательной железы как России, так и в других странах остаются высокими. У многих мужчин изначально диагностируют местно-распространенные (38,5%) и метастатические (23,2%) опухоли [2]. Следовательно, одной из приоритетных задач остается выявление данного новообразования на стадии локализованного процесса.
В настоящее время иммуногистохимические (ИГХ) методы исследования занимают важную роль в дифференциальной диагностике новообразований различной локализации, в том числе и РПЖ. Не вызывает сомнения то обстоятельство, что развитие патологического процесса в предстательной железе носит мультифакторный характер и сопряжено с нарушением и перестройкой большей части внутриклеточных механизмов. Иммуногистохимические методы позволяют увеличить выявляемость РПЖ на стадии локализованного процесса, сократить количество необоснованных повторных биопсий и необходимость повторных госпитализаций. Одним из важных направлений являются исследования, показывающие роль различных факторов роста в развитии и факторов прогрессирования новообразований предстательной железы [3, 4]. Деградация базальной мембраны межклеточного матрикса и различных строгальных элементов, включающих в состав структурные белковые компоненты, определяют инвазию и метастазирование опухоли. Данный механизм опосредован секрецией протеолитических ферментов, таких как матричные металлопротеиназы (ММП) — клеточных энзиматических продуцентов. [5].
В связи этим, на протяжении нескольких десятилетий повышается интерес к ММП, вовлекающим внеклеточный матрикс в процессы структурно-функционального ремоделирования, чаще всего путем деградации цепей коллагена. Уже идентифицировано около 30 энзимов данного семейства, которые характеризуются наличием общих свойств: разрушают внеклеточный матрикс, секретируются в виде профермента и активируются в результате протеолитического расщепления, проявляют активность в нейтральной среде. Однако для большинства из них до сих пор четко не обозначена их роль. В физиологических условиях существуют различные биологические механизмы по предотвращению протеолиза тканей, вызванного активацией ММП, такие как секреция клетками стромы тканевых ингибиторов ММП илиTIMP (tissue inhibitor of metalloproteinases). [4, 5, 6].
Ki-67 - это специфический белок, антиген ракового процесса, который является регуляторным. Его появление соответствует вступлению клетки в митоз, что позволяет использовать его в качестве универсального маркера пролиферации при оценке роста злокачественных опухолей, в том числе и РПЖ. Индекс Ki-67, определяемый как отношение количества клеток с интенсивной ядерной реакцией на Ki-67 к общему числу клеток, является независимым показателем прогноза рецидива и выживаемости у больных РПЖ. [7, 8].
На сегодняшний день описаны около 30 типов коллагена, которые кодируются различными генами. Они отличаются друг от друга по аминокислотной последовательности, а также по степени модификации-интенсивности гидроксилирования или гликозилирования. Общим для всех коллагенов является присутствие их во внеклеточном матриксе. Коллаген IV является основным компонентом базальной мембраны эпителиальных клеток, встречается в стенке артериальных сосудов и собственном веществе соединительной ткани. Инвазивные свойства опухолевых клеток связаны с разрушением этого важного компонента соединительной ткани [9].
В данном исследовании с использованием иммуногистохимических методов проведен анализ продукции матриксной ММП 9 типа, ингибитора металлопротеиназы TIMP-1, маркера пролиферации Ki-67, и изучение распределения коллагена IV в неизмененных клетках секреторного эпителия при доброкачественной гиперплазии предстательной железы (ДГПЖ) и атипических клетках аденокарциномы простаты различных градаций по шкале Глисона с целью изучения молекулярных механизмов инвазивного роста рака предстательной железы.
Материалы и методы
Когорта пациентов, включенных в исследования составила 184 мужчин, разделенных на 2 группы, средний возраст 68,2±2,17 лет. 65 пациентов с ДГПЖ и 118 пациентов с верифицированным раком предстательной железы различной степени анаплазии.
Для проведения ИГХ исследовании использовались следующие антитела к антигенам человека: моноклинальные мышиные антитела к белку Ki-67 (MM1, Diagnostic Biosystems, 1: 200); моноклинальные мышиные антитела к коллагену IV (PHM-12, Thermoscientific, 1:100); очищенные антитела кроличьей антисыворотки к матриксной металлопротеиназе-9 (Thermoscientific, 1:400); моноклинальные кроличьи антитела к ингибитору TIMP-1 (EPR 1550, 1:100, EPITOMICS).
Распределение коллагена IV в базальной мембране желез предстательной железы и строме оценивали полуколичественным методом в баллах по следующим показателям: 0 — отсутствие коллагена вдоль базальной мембраны и стромы; 1 — наличие тонкой полоски коллагена; 2 — толстая полоска коллагена вдоль базальной мембраны, сравнимая по толщине и интенсивности окрашивания со стенкой сосудов. Продукцию ММП-9 исследовали в различных опухолевых образованиях: ДГПЖ и аденокарциноме простаты различной градации от 2 до 5. Как правило, протеиназа выявляется в цитоплазме опухолевых клеток в виде мелких или крупных гранул, при этом отмечается различная интенсивность окрашивания. Оценку интенсивности ИГХ реакции с MMП-9 проводили в баллах по следующим параметрам: 0 — отсутствие коричневых гранул в цитоплазме клеток, 1 — наличие отдельных мелких гранул в цитоплазме, 2 — распределение в отдельных клетках крупных гранул, 3 — наличие крупных гранул в цитоплазме большинства клеток. Оценку интенсивности ИГХ реакции с ингибиторомTIMP-1 проводили по той же бальной шкале, что и ММП-9.
Статистическую обработку полученных данных проводили с помощью программы STATISTICA 10.0, с последующим математическим анализом полученных материалов. Корреляционные взаимоотношения между числом Глисона опухоли, ПСА, индексом пролиферации клеток, выраженностью продукции оценивали с помощью коэффициента корреляции Спирмена (rs).
Результаты и обсуждение
Пропорционально увеличению возраста пациентов в неизмененных эпителиальных клетках предстательной железы увеличивается продукция показателя клеточной пролиферации Ki-67 (3,24±0,61), но различия статистически недостоверны (р>0,05). В биоптатах пациентов с ДГПЖ отдельно расположенные пролиферирующие клетки локализовались только в базальном клеточном слое, пролиферативная активность клеток секреторного клеточного слоя не определялась. В аденокарциномах различных градаций выявлен широкий спектр пролиферативной активности секреторных железистых клеток (рис. 1а). При исследовании больных с опухолями 2-й и 3-й градации по шкале Глисона выявлена умеренная пролиферативная активность секреторных опухолевых клеток, где ИП Ki-67 составил 5,3+1,1% и 7,2+1,4%, (р<0,05) соответственно (рис. 1с). Анализ высокоинвазивных аденокарцином простаты 4-й и 5-й градаций показал выраженное увеличение пролиферативной активности атипических клеток (рис. 1е).
В ходе данного исследования коллаген IV типа прослеживался в виде тонкой коричневой полоски различной интенсивности вдоль базальной мембраны железистых клеток. Коллаген IV мелких артериол соединительно-тканной стромы, как правило, окрашивает стенку сосудов в интенсивный коричневый цвет. В соединительно-тканной строме ДГПЖ определяются толстые коричневые полоски коллагена IV, распределяющиеся вдоль базальной мембраны желез (интенсивность - 2 балла). Большое количество коллагена выявляется и в соединительно-тканной строме простаты (рис. 1b). В соединительно-тканной строме аденокарциномы предстательной железы 2-й градации по шкале Глисона интенсивность окраски менее выражена по сравнению с ДГПЖ и соответствует 1 баллу, однако тонкие волокна коллагена окружают отдельные клеточные элементы (рис. 1d). С увеличением числа Глисона более 3-й градации коллагеновые волокна вокруг опухолевых клеток полностью исчезают, что является достоверным критерием разграничения доброкачественных и злокачественных опухолей предстательной железы (p<0,05) (рис. 1f).
В железистых клетках при ДГПЖ в большом количестве определяются различные по строению и размеру гранулы MMП-9 (интенсивность — 3 балла) (рис. 2a). При изучении биоптатов аденокарциномы предстательной железы выявлено снижение интенсивности ИГХ окрашивания ММП-9. Сравнение показателей продукции MMП-9 при ДГПЖ и аденокарциноме различных градаций выявило следующую закономерность: оказалось, что продукция этого протеолитического фермента выше в тканях доброкачественных новообразований, где не наблюдается протеолитическая деструкция коллагена базальной мембраны, в отличие от аденокарциномы, характеризующейся инфильтративным ростом и разрушением базальной мембраны опухолевых желез. Вместе с тем, в полуколичественных исследованиях выявлено, что продукция ММП-9 в секреторных опухолевых клетках снижается по мере возрастания градации аденокарциномы, при этом в аденокарциномах 2-й и 3-й градаций уровень продукции этого фермента достоверно в 2 раза превышает этот показатель в аденокарциномах 4-й и 5-й градаций. Не выявлено достоверных различий в продукции ММП-9 между адено-карциномами 2-й и 3-й градаций, а также между 4-й и 5-й градаций (рис. 2с и 2е).
Для дальнейшего изучения механизмов инвазии аденокарциномы, были предприняты аналогичные исследования продукции в опухолевых клетках белка, ингибирующего активность ММП-9 в клетках TIMP-1. При аналогичном исследовании продукции TIMP-1 в различных опухолевых образованиях предстательной железы от ДГПЖ до аденокарциномы различной градации в подавляющем большинстве исследуемого гистологического материала, кроме описанных выше патологических состояний железистого эпителия, отмечены отдельные неизмененные железистые структуры, которые послужили контролем для последующих ИГХ исследований. В железистых клетках при ДГПЖ выраженная ИГХ реакция: в секреторных клетках крупных желез, в большом количестве определяются крупные, средние и мелкие гранулы TIMP-1, отмечается интенсивная окраска желез (интенсивность3 балла) (рис. 2b).
При оценке распределения TIMP-1 в аденокарциноме различной градации от-2 до-5 во всех случаях интенсивность окрашивания оказалась ниже, чем при ДГПЖ, и составила на фоне неизмененных желез 0 или 1 балл (рис. 2d и2f).
По мере увеличения градации по шкале Глисона и повышения пролиферативной активности секреторных клеток аденокарциномы простаты, происходит снижение выработки матриксной ММП-9. При этом инвазивные свойства опухолевых клеток, выражающиеся в разрушении коллагена IV — белка базальной мембраны и соединительнотканной стромы простаты, можно объяснить нарушением баланса между MMП-9 и TIMP-1 — белком, блокирующим этот фермент, продукция которого существенно снижается в аденокарциномах различной градации. Обнаружено, что уровень продукции TIMP-1 снижается в опухолях по мере нарастания в них анапластиче-ских изменений, при этом в аденокарциномах всех градаций его уровень более чем в 3 раза меньше, чем в клетках при ДГПЖ либо в неизмененных железах.
Кроме того, не выявлено достоверных различий в уровне продукции TIMP-1 между аденокарциномами различных градаций. Полученные данные свидетельствуют, что продукция матриксной металлопротеиназы 9 типа в аденокарциномах значительно снижена, и разрушение коллагена IV базальной мембраны железистых структур и стромы происходит за счет прогрессивного (до интенсивности в 0,8+0,4 балла по мере нарастания анапластических изменений) снижения выработки ингибитора матриксных металлопротеиназ TIMP-1 (p≤0,05). Низкой продукцией ингибитораTIMP-1 в аденокарциномах можно объяснить и инвазивные свойства этих опухолей.
В ходе исследования выявлена положительная корреляционная связь между градацией по шкале Глисона и индексом пролиферации клеток по показателю Ki 67 (rs=0,674) и отрицательная корреляционная связь этой градации с уровнем продукции ММП-9 (rs=-0,660). Достоверная отрицательная корреляция существует между уровнем пролиферативной активности клеток и продукции секреторными опухолевыми клетками MMП-9 (rs=-0,369). Отсутствие корреляционной взаимосвязи между продукцией TIMP-1 и другими клиническими, морфологическими и ИГХ показателями свидетельствует о том, что уровень этого белка в секреторных клетках аденокарциномы снижен.
Проведенное исследование показало значение таких методов иммуногистохимических исследований, как исследование пролиферативной активности белка Ki-67; распределения коллегановых волокон вокруг клеток; уровня продукции ММП9 типа и ингибитора TIMP-1 для дифференциальной диагностики доброкачественных и злокачественных новообразований предстательной железы. Доброкачественная гиперплазия характеризуется высокой продукцией ММП9 типа, разрушающей коллаген базальных мембран и стромы, протеолитическое действие которой блокируется высоким содержанием ингибитора TIMP-1. В опухолях продукция ММП9 типа снижена, разрушение коллагена IV базальной мембраны железистых структур происходит на фоне резкого снижения продукции ингибитора металлопротеиназы TIMP-1. При отсутствии гистологических изменений в предстательной железе, характерных для опухолевого роста, необходимо дополнительное определение пролиферативной активности белка Ki-67; распределения коллегановых волокон вокруг клеток; уровня продукции ММП-9 типа и ингибитора TIMP-1, что позволит улучшить выявление опухолей предстательной железы на стадии локализованного процесса и сократить количество необоснованных повторных биопсий.
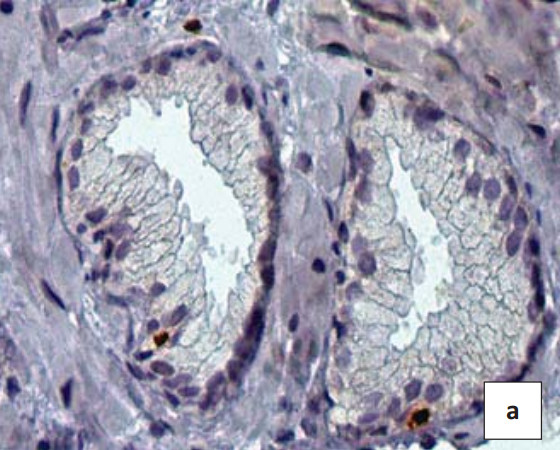
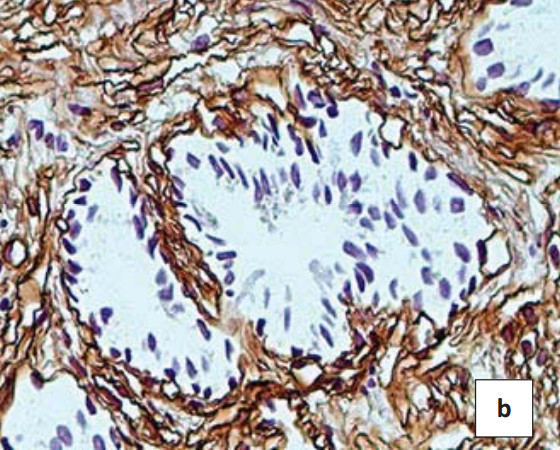
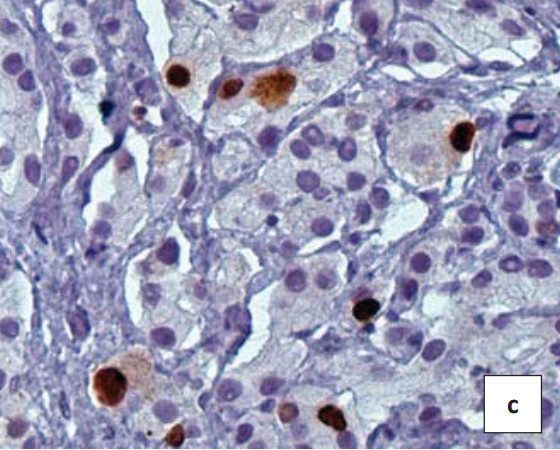
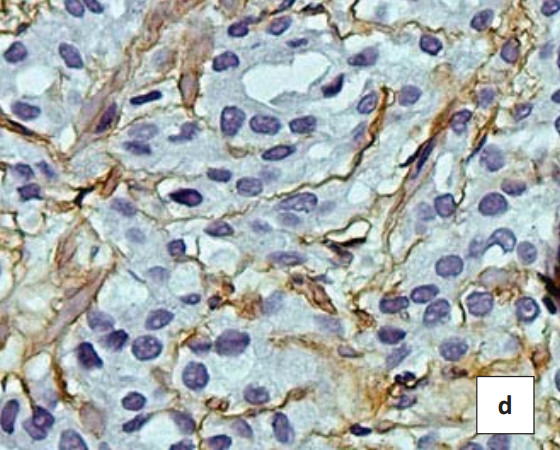
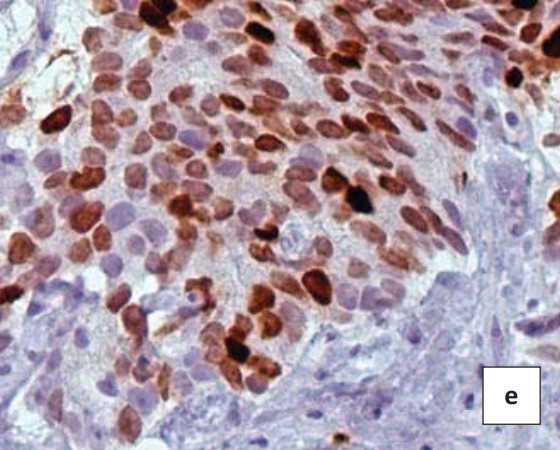
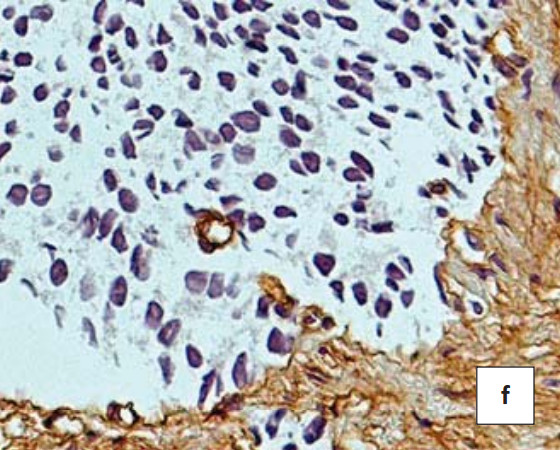
Рисунок 1. ИГХ реакция в биоптатах пациентов с ДГПЖ (a, b) и аденокарциномой простаты Глисон 2 (c, d) и 4 (e, f) с антителами к белку Ki 67 (a, c, e) и коллагену IV типа(b, d, f). Окраска: ДАБ-гематоксилин (х400)
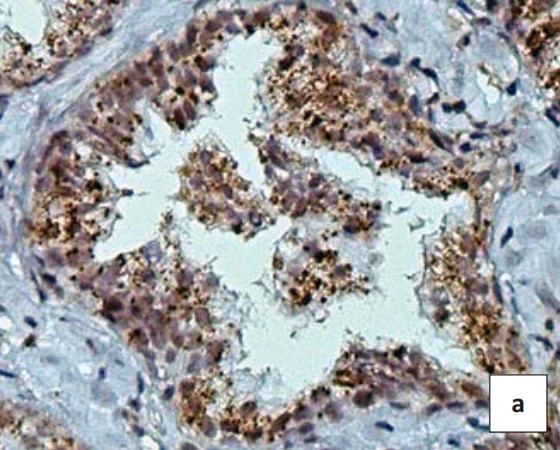
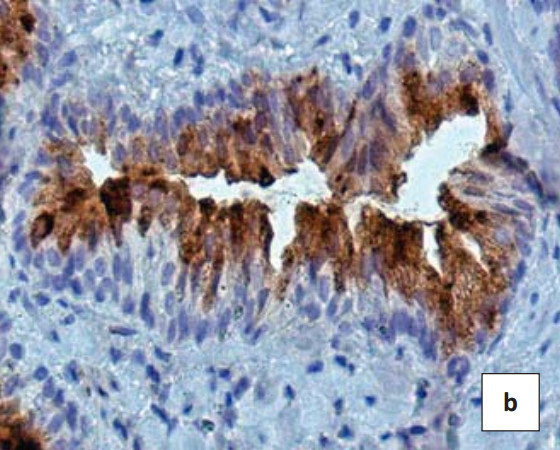
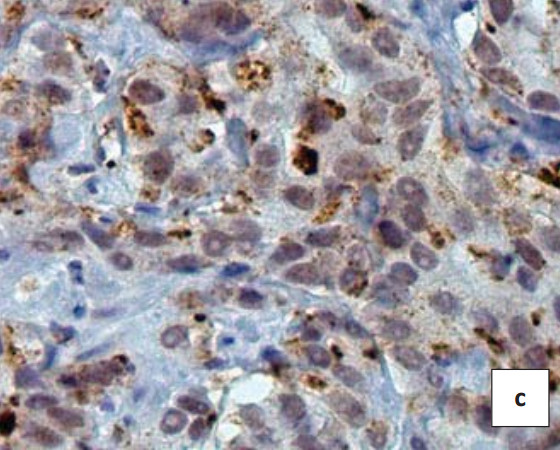
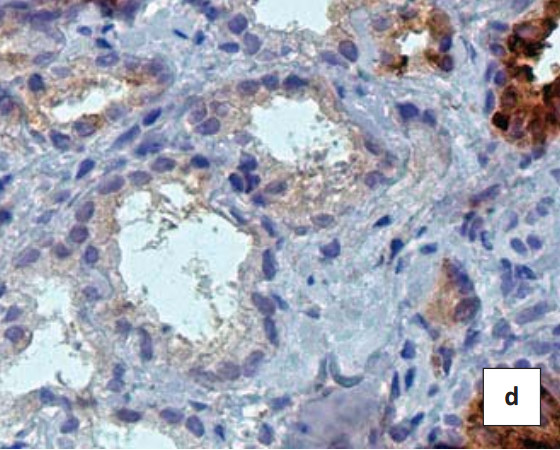
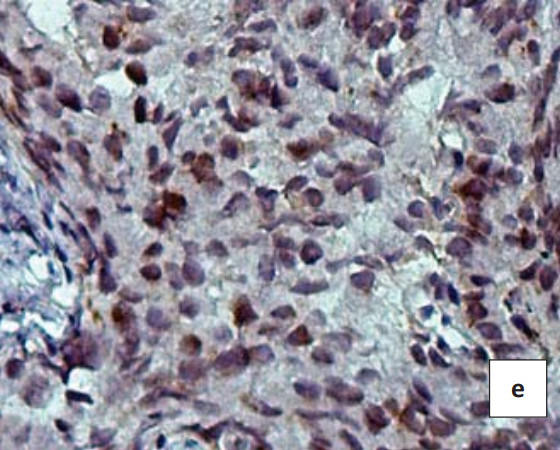
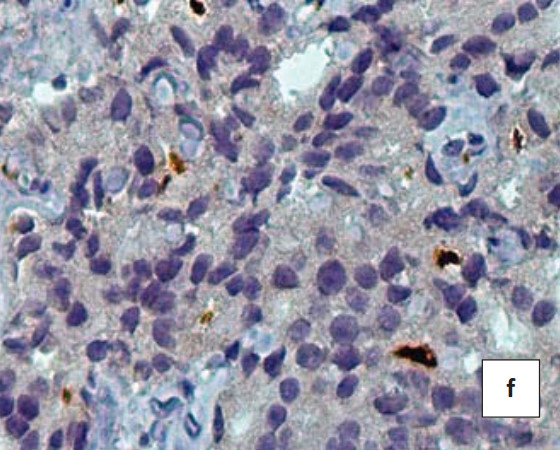
Рисунок 2. ИГХ реакция в биоптате пациентов с ДГПЖ(a, b) и аденокарциномой простаты Глисон2 (c, d) и 4 (e, f) с антителами к белку MMP-9 (a, c, e) иTIMP-1 (b, d, f). Окраска ДАБ-гематоксилин (х400)
Выводы
В рамках проведенного исследования доказана диагностическая и прогностическая ценность ИГХ маркеров, таких как определение пролиферативной активности белка Ki-67; распределения коллегановых волокон вокруг клеток; уровня продукции ММП9 типа и ингибитораTIMP-1. Полученные результаты открывают перспективы дальнейших исследований в этой области, среди которых оценка диагностической ценности других маркеров болезней предстательной железы, выявление взаимосвязи ИГМ маркеров и эффективности лечения различных болезней предстательной железы.
Исследование не имело спонсорской поддержки. Авторы заявляют об отсутствии конфликта интересов.
Литература
- Злокачественные новообразования в России в 2015 году (заболеваемость и смертность). Под ред. Каприна АД, Старинского ВВ, Петровой ГВ. 2017; 11-15.
- Аляев Ю.Г., Крупинов Г.Е., Амосов А.В. Рак простаты и HIFU-терапия. Урология. 2007; (6):32-38.
- Кушлинский Н.Е. Молекулярные и клеточные маркеры пролиферации, дифференцировки, метастазирования и неоангиогенеза при раке предстательной железы. Избранные главы гериатрической урологии. Ньюдиамед. 2000; 227-273.
- Березин А.Е. Регуляторы активности матриксных металлопротеиназ как новые биологические маркеры кардиоваскулярного ремоделирования: обзор литературы. Український медичний часопис. 2011; (1):36-43.
- Brehmer B, Biesterfeld S, Jakse G. Expression of matrix metalloproteinases (MMP-2 and -9) and their inhibitors (TIMP-1 and -2) in prostate cancer tissue. Prostate Cancer Prostatic Dis. 2003;6:217-222. doi:10.1038/sj.pcan.4500657
- Gouyer V, Conti M, Devos P, Zerimech F, Copin MC et al. Tissue inhibitor of metalloproteinase-1 is an independent predictor of prognosis in patients with non-small cell lung carcinoma who undergo resection with curative intent. Cancer. 2005; (103):1676-1684. doi:10.1002/cncr. 20965
- Rubio J, Ramos D, Lopez-Guerrero JA, Iborra I, Collado A, et al. Immunohistochemical expression of ki-67 antigen, cox-2 and bax/bcl-2 in prostate cancer; prognostic value in biopsies and radical prostatectomy specimens. Eur. Urol. 2005;48 (5):745-751. doi:10.1016/j.eururo. 2005.06.014
- Авдошин В.П., Бабиченко И.И., Котельникова Е.В. Прогностическое значение экспрессии иммуногисто-химических маркеровKi 67, MMP 9 и коллагенаIV у больных папиллярным уротелиальным раком мочевого пузыря. Онкоурология. 2011; (3):66-70.
- Schnoor M. Production of type VI collagen by human macrophages: a new dimension in macrophage functional heterogeneity. J Immunol. 2008; (180):5707–19. doi:10.4049/jimmunol.180.8.5707









Комментарии