Борисов В.В.
Кафедра нефрологии и гемодиализа ФППО врачей Первого Московского государственного медицинского университета им. И.М. Сеченова, г.Москва Адрес: 119019, г.Москва, Никитский бул., 13, строен. 1, тел. елефон: (495)6902663 Эл.почта: vvb56@yandex.ru
В нашей стране сегодня лекарства производят около 350 фармацевтических предприятий, однако на рынке лекарственной продукции их доля в стоимостном выражении составляет по разным данным от 10 до 20%. Все остальное – импортные лекарства. В 2008 году по данным Минпромторга РФ импорт фармацевтической продукции в Россию вырос на 51,5% по сравнению с 2007 годом и составил 6,457 миллиардов долларов. В 2009 году наблюдается некоторый спад импорта, тем не менее, в рамках федеральных программ лекарственного обеспечения на долю российских препаратов приходится менее 10 процентов всех контрактов. По мнению руководителей нашего государства необходимо в корне изменить политику государственных закупок, иначе отечественный производитель так и останется «гостем на собственном рынке». Тем более что ежегодный общегосударственный объем закупок лекарств сегодня составляет 230 млрд. рублей. По мнению руководителей государства в ближайшие годы необходимо добиться, чтобы более половины бюджетных денег, отпущенных на закупки лекарств, тратились на отечественные препараты.
В связи с этим нельзя не остановиться более подробно на положении и перспективах фармацевтической промышленности и обеспечения больных лекарственными препаратами в нашей стране. В соответствии с разработанной «Стратегией развития фармацевтической промышленности РФ на период до 2020 года «, уже в ближайшие три года должен измениться баланс производимых в России и импортируемых лекарственных средств в пользу отечественных препаратов, которые по качеству должны соответствовать международному уровню. Задачами государственной программы «Стратегия развития фармацевтической промышленности РФ на период до 2020 года« являются:
- Увеличение обеспеченности населения, учреждений системы здравоохранения и Вооруженных Сил РФ жизненно необходимыми и важнейшими лекарственным средствами отечественного производства, а также лекарственными средствами для лечения редких заболеваний.
- Повышение конкурентоспособности отечественной фармацевтической промышленности путем гармонизации российских стандартов по разработке и производству лекарственных средств с международными требованиями.
- Стимулирование разработки и производства инновационных лекарственных средств и поддержка экспорта российских лекарств, в том числе за счет выработки дополнительных механизмов финансирования оригинальных разработок.
- Защита внутреннего рынка от недобросовестной конкуренции и выравнивание условий доступа на рынок для отечественных и зарубежных производителей.
- Осуществление технологического перевооружения российской фармацевтической отрасли.
- Совершенствование системы подтверждения соответствия качества лекарственных средств, включая меры по устранению избыточных административных барьеров по регистрации отечественных лекарств и обеспечение надлежащего контроля за их качеством.
- Совершенствование системы подготовки специалистов для фармацевтической промышленности, в том числе создание новых программ обучения в соответствии с международными стандартами.
Проектная мощность созданных уже сегодня современных предприятий такова, что может потенциально обеспечивать потребности всех российских больниц в основных рецептурных лекарствах. Основные направления деятельности таких предприятий – научноисследовательская деятельность, производство высокодоходных современных лекарств, а также контрактное производство генериков – лекарств, идентичных «фирменным» препаратам, но стоящим за счет экономии на рекламе и разработке подчас в разы меньше. Инфраструктура предприятий должна соответствовать европейским стандартам организации фармацевтических производств, быть промышленным производством полного цикла по стандартам GMP (Good Manufacturing Practice, «надлежащая производственная практика»), выпускающим основные виды лекарственных форм, поскольку без внедрения GMP и других международных стандартов в этой сфере отечественная фармацевтическая отрасль не сможет на равных конкурировать с зарубежными производителями. Необходим поэтапный план перехода на международные стандарты, после реализации которого препараты, не соответствующие этим стандартам, не должны больше закупаться на бюджетные средства.
По мнению руководства страны необходимо заметно расширить номенклатуру производимых в России лекарственных средств, как за счет размещения лицензионных производств, так и организуя выпуск генериков. Главная цель – максимально снизить зависимость России от импортных препаратов. Деньги, которые государство и сами больные тратят на лекарства, должны оставаться внутри страны и использоваться отечественными компаниями для разработки новых, инновационных лекарств. В результате реализации «Стратегии развития фармацевтической промышленности РФ на период до 2020 года« доля отечественных производств должна возрасти с 19 до 50% в стоимостном выражении, не менее 60% выпуска должны составлять современные инновационные препараты, а доля отечественных средств как жизненно необходимых важнейших лекарств должна достичь 85%»
Новый оригинальный препарат – это впервые синтезированное и прошедшее полный цикл исследований лекарственное средство, активные ингредиенты которого (способ получения, показания к применению, торговое название) защищены патентом в течение определенного срока (20 лет). Каждое новое лекарственное средство – это впервые синтезированное химическое вещество. Каждый новый препарат – это научное открытие, еще один шаг на пути прогресса, т.к. только 1 из 10 000 потенциальных лечебных молекул становится лекарственным средством. Время, потраченное на научные разработки в 60-е годы, составляло в среднем 8 лет, в 70-е – 11, в 80-е – 14, к концу 90-х прошлого века оно достигло 15 лет.
Неоспоримый факт, что научная разработка нового лекарственного препарата может длиться десятилетиями. Доклинические исследования обычно занимают 3-5 лет и включают поиск нового действующего вещества, химический синтез и начальные исследования для выявления активного фармакологического компонента, выбор лекарственной формы и ее тестирование на стабильность. Клинические исследования включают 4 фазы. 1-я фаза (2-3 года) – исследование безопасности препарата на 20-100 здоровых добровольцах. При этом до 25% препаратов отсеивают. 2-я фаза (3-4 года) – изучение эффективности и краткосрочных рисков у 100-500 пациентов-добровольцев, отсев при этом достигает в среднем 38,8%. 3-я фаза (1-2 года) – изучение безопасности и эффективности нового препарата у 1000-3000 пациентов, отсев составляет 13,2%. Всего на этапах клинических исследований 77% новых препаратов по тем или иным причинам разрабатывать прекращают.
В случае успеха осуществляется регистрация, которая занимает 1-2 года. Все это время (12 лет) составляет потерянные годы патентной защиты нового лекарства. 4-я фаза клинических исследований – постмаркетинговый этап, когда запатентованное лекарство в свободной продаже применяется, эффективный срок его патентной защиты составляет уже всего 8 лет. Количество необходимых клинических исследований созданного препарата в 19771984 г. составляло 30 (2000 больных), к 1995 году оно возросло до 80 (8000 больных). В Европе документация для получения лицензии на новый препарат составляет 4100 папок и содержит 1850000 страниц. Если их все сложить в одну стопку, то ее высота достигает 230 м, а если все страницы необходимой документации сложить в одну линию, она протянется на 550 км. По зарубежным данным материальные затраты в процессе создания оригинального препарата составляли в 70-е годы в среднем 54 млн. долларов США, к 2000 г. они возросли до 450млн. долларов, а к 2007 г. достигли 1 млрд. долларов. В качестве примера можно привести инвестиции компании «Pfizer» в разработку и производство препарата Виагра, которые составили 2,5 млрд. долларов США.
Таким образом, в итоге оригинальный препарат – это доказанная эффективность, доказанная безопасность, заведомо известное «поведение» препарата в организме больного (фармакокинетика и фармакодинамика), оптимально подобранные дозировки и курсы лечения. Генериками («generic» англ. – родственный, общий) называют лекарственные препараты, которые выпускает фармацевтическая компания, не тратившая денег на их разработку и испытания. Основная характеристика препарата-генерика – его низкая стоимость. Генерик – воспроизведенное лекарственное средство, взаимозаменяемое с его патентованным аналогом, выведенное на рынок по окончании срока патентной защиты оригинала (бренда). Невольно возникают вопросы, на которые следует получить ответ:
- Являются ли генерики при качественном и количественном соответствии действующего вещества адекватными заменителями оригинальных препаратов?
- Являются ли они столь же эффективными и безопасными?
- Означает ли фармацевтическая эквивалентность эквивалентность клиническую?
Этапы создания генериков – это получение (покупка) патента на продукт (химическое вещество) и на его производство, а затем производство лекарственного средства и его реализация. Требования к качеству препаратов-генериков значительно ниже по сравнению с брендом. В частности, они должны обладать доказанной терапевтической взаимозаменяемостью с оригинальным препаратом. К сожалению, это не всегда так. В качестве примера можно привести препарат Дифлюкан («Pfizer» США). В опытах in vitro для подавления роста тест-культур Candida species требовалась в 2-4 раза большая концентрация генерика по сравнению с Дифлюканом-брендом (рис. 1)
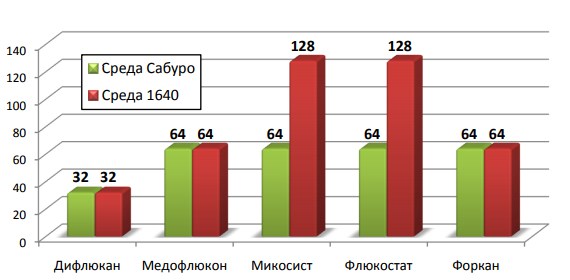
Рис. 1. Концентрации генериков Дифлюкана в опытах in vitro для подавления роста тест-культур Candida species
Генерик допускается в обращение на основании оценки регистрационного досье сокращенного объема и данных по биоэквивалентности. Рассматривается эквивалентность фармацевтическая, фармакокинетическая и фармакотерапевтическая. Фармацевтическая эквивалентность – это полное соответствие в препарате-генерике качественного и количественного состава, физико-химических свойств лекарственной формы оригинальному препарату, оцениваемое фармакопейными тестами. Допускается отличие содержания действующего вещества не более 5%. Однако стоимость субстанции (действующего вещества), как известно, составляет 50% себестоимости лекарственного средства, поэтому фармацевтические компании, производящие генерики, стремятся приобретать ее по возможно более низкой цене в странах со слаборазвитыми технологиями. Это может приводить к повышению содержания в лекарственном средстве токсических примесей, выявление которых возможно только благодаря специальному химическому анализу, к сожалению, не предусмотренному в фармакопейных статьях.
Фармацевтическая эквивалентность препарата-генерика не гарантирует эквивалентности фармакокинетической (биоэквивалентности). Фармакокинетическая биоэквивалентность – главное условие регистрации препарата-генерика. Она означает одинаковую биодоступность, что возможно при одинаковой степени и скорости всасывания лекарственного вещества. Возможные различия могут составлять до 15-20%. Кроме того, фармакокинетическая биоэквивалентность зависит от вспомогательных веществ, предъявляемые требования к которым такие же, как и к активной субстанции.
В качестве примера можно привести данные о препарате Кардура («Pfizer» США) и ее многочисленных генериках.
Изменения в составе вспомогательных веществ (таблица 1) могут существенно повлиять на растворимость и биодоступность действующего вещества, его концентрацию в крови и длительность действия. Это может привести к токсическим явлениям и аллергическим реакциям. Косвенным отражением изменений состава генериков являются и отличные от бренда правила хранения таблеток (таблица 2), его температурный режим (таблица 3), а также сроки годности препарата (таблица 4).
Таблица 1. Содержание вспомогательных веществ в таблетке Кардуры и генериков
| Торговое название, производитель, страна | Содержание вспомогательных веществ в таблетке |
|---|---|
| Кардура (Пфайзер, США) Доксазозин (НИОПИК ГНЦ, Россия) | крахмал, лактоза, натрий гликолат, МКЦ, магния стеарат, натрия лаурилсульфат |
| Зоксон (Зентива, Чехия) | + целлюлоза микрокристаллическая гранулированная, целлюлоза микрокристаллическая, натриевая соль карбоксиметилкрахмала А, коллоидная двуокись кремния |
| Артезин (Валента, Россия) | + повидон или коллидон 25, аэросил, натрия додецилсульфатнатрия гликолат, натрия лаурилсульфат |
| Остальные препараты | Данные отсутствуют |
Таблица 2. Правила хранения таблеток Кардуры и генериков
| Торговое название препарата, страна | Правила хранения |
|---|---|
| Кардура (США), Доксазозин (Россия-Канада), Зоксон (Чехия), Артезин (Россия), Доксазозин (Россия) | В сухом защищенном от света месте |
| Доксазозин-ратиофарм (Германия) | В обычных условиях |
| Камирен (Словения), Магурол (Кипр) | Указания отсутствуют |
Таблица 3. Температурный режим хранения таблеток Кардуры и генериков
| Торговое название препарата, страна | Температура хранения, °С |
|---|---|
| Кардура (США), Камирен (Словения) | до 30 |
| Магурол (Кипр), Артезин (Россия), Доксазозин (Россия 2) | до 25 |
| Зоксон (Чехия) | 10-25 |
| Доксазозин (НИОПИК ГНЦ, Россия) | 5-25 |
| Доксазозинратиофарм (Германия), Доксазозин (Канада-Россия), Доксазозин-Веро (Россия) | Указаний нет |
Таблица 4. Сроки годности таблеток Кардуры и генериков
| Торговое название препарата, страна | Срок годности, лет |
|---|---|
| Кардура (США) | 5 |
| Камирен (Словения) | 3 |
| Зоксон (Чехия), Магурол (Кипр), Артезин (Россия), Доксазозин-ратиофарм (Германия), Доксазозин (Россия-Канада), Доксазозин (Россия) | 2 |
Именно поэтому фармацевтическая эквивалентность и биоэквивалентность еще не гарантируют эквивалентность терапевтическую. Это подтверждает отсутствие доказательных исследований, которые позволили бы сравнить терапевтическую эффективность генериков и Кардуры.
Другой пример. Результаты клинических исследований, показавшие эффективность максимальной андрогенной блокады (МАБ) при раке простаты были получены с применением оригинального препарата Флутамид (Флуцином компании Шеринг Плау США). Исследования аргентинского генерика Тафенил (Флутамид) выявило его сниженную в 8,5 раз растворимость по сравнению с Флуциномом, абсолютно недостаточную для достижения необходимого антиандрогенного эффекта. Данные о сопоставимой клинической эффективности Флуцинома и его генериков в литературе также отсутствуют. Автоматический перенос эффективности бренда на генерик не может быть осуществлен без доказательных исследований по сравнительной биоэквивалентности, биодоступности и клинической эффективности.
Современная стратегия лечения больных принимает во внимание не только эффективность способа лечения, но и потенциальные осложнения. Основными причинами неудовлетворенности и врачей, и больных методами оперативного лечения многих заболеваний являются риск операции и обезболивания, а также высокий процент послеоперационных осложнений, ухудшающих качество жизни больных. Именно это нередко делает лекарственное лечение в отличие от оперативного более предпочтительным. Если в качестве примера рассмотреть гиперплазию (аденому) простаты, то наиболее мощными стимулами к разработке новых средств лекарственной терапии служат:
- совершенствование ранней диагностики, выявление заболевания на стадиях, не требующих оперативного лечения;
- удовлетворенность медикаментозным лечением, позволяющим, особенно в пожилом и старческом возрасте стабилизировать болезненный процесс и, прежде всего, нарушенное мочеиспускание, не только препятствовать его ухудшению, но и способствовать улучшению;
- возможность под влиянием лекарств уменьшения размеров аденомы простаты, а, следовательно, и уменьшения выраженности симптомов заболевания.
При этом во главу угла не ставят стремление во что бы то ни стало избавить больного от аденомы, а стараются реализовать возможность препятствовать прогрессированию болезни, ухудшению мочеиспускания, возможность сохранить и повысить качество жизни больного на фоне постоянного приема лекарства без риска оперативного вмешательства – положение о том, что лечение не должно быть тяжелее болезни. Именно поэтому с появлением эффективных лекарств к концу 90-х прошлого века аденома простаты перестала быть чисто хирургическим заболеванием, а медикаментозную терапию по сводным мировым данным уже получали около 75%, а сегодня более 90% больных.
Необходимо учитывать наиболее важные аспекты современного лекарственного лечения:
- научно-практический – создание, производство и распространение новых эффективных лекарственных препаратов;
- этический – изменение стереотипа врача верить только в успех операции;
- моральный – уверенность врача и больного в успехе лечения при условии правильного назначения по-настоящему эффективного лекарства;
- экономический (для больного и государства) – эффективные препараты в силу высокой стоимости могут быть недоступными нуждающимся больным, а льготное государственное обеспечение лекарствами должно соответствовать потребностям больного.
Современная фармакотерапия больных аденомой простаты охватывает применение ингибиторов 5-альфа-редуктазы, альфа-1-адреноблокаторов и препаратов растительного происхождения. Монотерапия или сочетание различных по действию лекарственных средств – одна из сложных задач, решение которой возложено на врача-уролога. Правильное и рациональное решение этой задачи – это, прежде всего, эффективное консервативное лечение, однако, не следует забывать и об экономической стороне проблемы – расходах на приобретение лекарства, лежащих на плечах пациента, или государства при льготном лекарственном обеспечении. В идеале эти стороны проблемы не должны вступать в конфликт, а медикаментозное лечение больного должно включать минимум лекарственных препаратов, обеспечивающих максимально эффективное консервативное лечение индивидуально у каждого больного.
Появившиеся на лекарственном рынке в середине 90-х альфа-1-адреноблокаторы (альфузозин – Дальфаз, теразозин – Хайтрин, тамсулозин – Омник и доксазозин – Кардура) позволили значительно повысить эффективность медикаментозной терапии больных аденомой простаты. Они имеют во многом аналогичный механизм действия, сходные показания и противопоказания и относительно небольшие индивидуальные особенности, которые и являются критериями их назначения различным пациентам. Ни для кого не секрет, что Альфузозин (Дальфаз) не проникает через гематоэнцефалический барьер и, поэтому, обладает преимущественно периферическим действием, лечение этим препаратом и в обычной дозировке, и, особенно в форме «ретард» мало управляемо, а постуральные нежелательные эффекты бывают выражены. Теразозин (Хайтрин) обладает более выраженным гипотензивным действием, при нормотонии может вызывать ортостатический коллапс, особенно выражен «эффект первой дозы», показан не всем больным аденомой простаты, а преимущественно пациентам с сопутствующей артериальной гипертензией. Тамсулозин (Омник) не позволяет отрабатывать индивидуальную дозировку, его 16-часовое действие не всегда достаточно эффективно, а часто возникающая ретроградная эякуляция порой смущает больных и может быть поводом для отказа от лечения. Определенные перспективы имеет таблетированный Омник Окас, действующий 24 часа.
Значительные преимущества имеет Доксазозин, который разработала и выпускает американская компания «Pfaizer» под названием Кардура. Этот препарат блокирует лишь гиперактивные альфа-адренорецепторы, не вызывая снижение артериального давления при нормотонии и способствует его эффективному снижению при артериальной гипертензии, что позволяет осуществлять рациональную многоцелевую монотерапию этих заболеваний. Влияние Кардуры на липидно-стероидный обмен, уменьшение агрегации тромбоцитов, снижение инсулин-резистентности тканей под влиянием этого препарата значительно расширяет спектр его применения у мужчин, страдающих атеросклерозом и сахарным диабетом. Сосудистые эффекты Кардуры позволяют эффективно применять ее в терапии больных хроническим простатитом, эректильной дисфункцией и т.д. Именно эти эффекты Кардуры со временем поставили всю группу альфа-1-адреноблокаторов в ряд ведущих медикаментозных средств, применяемых в урологической практике.
Оценка любого лекарственного препарата для консервативной терапии аденомы простаты врачом и пациентом сегодня должна включать видение препарата в спектре известных, отрицание понятий «единственный», «неповторимый», «лучший», «наиболее предпочтительный», «золотой стандарт». К выбору препарата для лечения аденомы следует подходить сугубо индивидуально, подбирая его в соответствии с особенностями действия и проявлениями заболевания, особенно у пациентов пожилого и старческого возраста. Врачу и пациенту необходимо всесторонне изучать положительные и отрицательные стороны принимаемого препарата, не скрывать их, а пристально анализировать, стремиться к профилактической направленности лекарственной терапии на основе знаний симптомов, течения, осложнений и исходов этого заболевания. Эффективное лечение во многом зависит от:
- Знаний и квалификации врача, соотнесенных с научными достижениями и собственным опытом на основе полученного образования и систематического последипломного усовершенствования.
- Вторым компонентом, бесспорно, являются экономические возможности лекарственного обеспечения, которые находятся в прямой зависимости от финансирования фармацевтической отрасли и здравоохранения, социальной сферы и, что не менее важно, от благосостояния больного.
На оба компонента свое положительное и отрицательное влияние оказывает реклама лекарств в средствах массовой информации. Она должна быть направлена врачу, а не больному, минуя врача. Реклама, обращенная непосредственно больному стимулирует самолечение при аденоме простаты, за которым может скрываться недиагностированный рак предстательной железы с фатальным исходом. Подчинять здоровье и жизнь больного эгоистическим коммерческим интересам лекарственных производителей преступно. Медицина, как известно, это и ремесло, и искусство, их разумное сочетание – залог успеха в лечении и повышении качества жизни пациентов.
Производители Кардуры приложили огромные усилия для всестороннего изучения фармакологических свойств этого препарата, его дозирования, эффективности, безопасности, возможности сочетания с другими лекарствами, побочных эффектов и пр. Именно они сделали все, чтобы расширить лечебные возможности применения Кардуры. В силу высокой эффективности и многогранного лечебного эффекта у больных аденомой простаты и другими заболеваниями количество генериков Кардуры максимально: Доксапростан (Акрихин, Россия, Нью Фарм, Канада), Доксазозин (Нью-Фарм Инк, ВекторМедика, Россия), Доксазозин (Россия) – 4 препарата, выпускаемых компаниями ЗАО «Здоровье», Оболенское фармпредприятие, НИОПИК ГНЦ, ВероФарм), Артезин (Валента, Россия), Камирен (КРКА, Словения), Зоксон (Зентива, Чехия), Магурол (Медохеми, Кипр). Основным преимуществом каждого генерика является его более низкая цена на рынке. Так, для большинства генериков Кардуры стоимость месячного курса лечения в средней дозировке в 2 раза ниже бренда.
Необходимо подчеркнуть, что химическое вещество (Доксазозин) может быть получено в ходе технологических процессов, от которых во многом зависят свойства лекарственного препарата (не только физические и химические, чистота, растворимость и пр.), но и биодоступность, биоэквивалентность и безопасность. Новая более дешевая технология – это научный прорыв, но эквивалентен ли он исходным данным? Нет, поскольку ни один из производителей этих многочисленных генериков не проводил глубокого и всестороннего изучения полученного ими продукта, как «Pfizer» в отношении Кардуры. Результаты успешного применения своего препарата каждый производитель генерика нередко стремится необоснованно подтвердить сведениями об успешном применении Кардуры, лукаво заменяя это название на «Доксазозин», и лишь потом приводя свои более скромные результаты ориентировочных исследований. Но, будучи честным и принципиальным, записать эти успехи себе в актив можно лишь пройдя путь своего предшественника. Никто из производителей генериков, к сожалению, не проводил и не будет проводить многогранных дорогостоящих клинических исследований, которые были проведены компанией «Pfizer» по Кардуре.
Порой одни сведения производители генериков пытаются подменить другими. Так, в доказательство биоэквивалентности Камирена (Словения) приводят кривые сравнения его концентраций в плазме крови по сравнению с Кардурой, а не концентрации непосредственно на альфа-1-адренорецепторах, как это было сделано для Кардуры. Эффективность Камирена подтверждают результатами исследования ПРЕДИКТ, которое проводилось с Кардурой. Основными аргументами в пользу генериков становятся название (Доксазозин) и значительно меньшая цена на рынке. Никаких достоверных исследований для сравнения эффективности генериков и Кардуры не проводили. Создатели генериков забывают, что не корректно и не допустимо переносить данные, полученные при исследовании эффективности и безопасности оригинального препарата, на их копии.
Сведения, публикуемые в проспектах генериков, порой парадоксальны. Так в рекламе Доксазозина (Вектор Медика) указано, что препарат зарегистрирован, и инструкция к его применению утверждена в 2002 году, а данные по его применению за рубежом (!) датированы 1996 годом, в России он, якобы, длительно применялся, и результаты опубликованы в 2000 году в журнале «Урология». Столь неблаговидный подход в рекламе не может не заставить усомниться в полноценности и качестве предлагаемых продуктов, пусть даже и по более низкой цене.
Основной проблемой назначения генериков является невозможность гарантировать взаимозаменяемость лекарственных препаратов, которая может нанести вред здоровью и безопасности пациентов. Отсутствие достоверных данных о клинической эффективности генерика, а также данных о биоэквивалентности генерика и оригинального препарата ставят под сомнение целесообразность применения генерика в качестве лечебного средства. Ведущие фармацевтические компании, работающие на Российском рынке, правомерно насторожило предложение выписывать рецепты по международному непатентованному названию, что может не только снизить оборот компаний, выпускающих брендовые препараты на 20-30%, а выведет на рынок и приведет к необоснованному росту оборота производителей дешевых и более доступных, но менее эффективных генериков. Формально выгодные ценовые характеристики дешевого, но малоэффективного препарата могут обернуться существенным ростом затрат на лечение больных за счет:
- удлинения курса лечения,
- повышения частоты рецидивов,
- повышения частоты осложнений,
- возможности перехода заболеваний в хроническую форму.
Нет сомнения в том, что, делая выпуск генериков частью программы лекарственного обеспечения больных, руководство страны формально исходит из идеальных качеств генериков:
- окончание сроков патентной защиты бренда,
- соответствие фармакопейным требованиям, производство в условиях GCP,
- почти полное соответствие оригинальному продукту по составу, назначение и продажа под международным непатентованным названием,
- сравнительно низкая цена.
Однако, к сожалению, данные доказательных клинических исследований в нашей стране обязательны для регистрации только новых оригинальных препаратов-брендов. Такого жесткого законодательного регулирования регистрации генериков у нас сегодня не существует, а сравнительные исследования клинической эффективности генериков и бренда, к сожалению, выполнены только для единичных генериков. Поэтому их широкое распространение обусловлено не только отсутствием необходимых доказательных клинических исследований, отсутствием должного изучения профилей безопасности препаратов, но и отсутствием необходимых сравнительных исследований эффективности генерика и оригинального препарата. Эти своеобразные законодательные недоработки порой приводят к тому, что первыми страдают наши пациенты. Поэтому нельзя не согласиться с народной мудростью. «Мы не настолько богаты, чтобы покупать дешевые вещи» гласит английская пословица. Известно, что «скупой платит дважды», а русская народная мудрость говорит «дешево хорошо не бывает».
Специалисты нашей страны существенно обеспокоены качеством генериков. В сентябре 2008 г. в Москве состоялся «Круглый стол» с участием представителей Росздравнадзора, Альянса клинических химиотерапевтов и микробиологов, Межрегиональной ассоциации по клинической микробиологии и антимикробной терапии (МАКМАХ) и других специалистов. Темой обсуждения стали вопросы эфективности генериковых препаратов, в первую очередь, идентичности их действия на организм пациентов по сравнению с оригинальными лекарственными средствами. Эта проблема особенно актуальна для России, где доля генериков на фармацевтическом рынке превышает 75%, тогда как в США она составляет порядка 12%, а в Европе – 30-60%. Наиболее актуальными были признаны следующие вопросы:
- Какими должны быть исследования генериковых препаратов, по каким нормативным документам они будут проводиться, и кто будет их финансировать?
- Как сделать доступной для врачей информацию о случаях обнаружения неадекватных генериков в пострегистрационный период?
В отличие от США в России, к сожалению, не существует централизованной базы данных по оригинальным и воспроизведенным препаратам. В то же время доступность объективной информации о терапевтической эквивалентности генериков позволила бы обеспечить более адекватное медицинское обслуживание в нашей стране, а врачи более уверенно использовали бы генерики с учетом их эффективности, безопасности и экономических преимуществ.
С проблемой мало контролируемого распространения множества генериков связана другая проблема отечественных производителей лекарств – распространенная среди врачей практика лоббирования интересов крупных мировых фармацевтических компаний, производящих бренды. Руководство страны уверено, что, имея возможность порекомендовать пациенту дешевый генерик – полностью идентичное отечественное средство – многие доктора советуют лечиться заведомо более дорогими импортными брендовыми препаратами. При этом абсолютно не учитывается терапевтический эффект лекарства, который у бренда нередко значительно выше. С формальных позиций руководители отрасли видят в этом глубоко эшелонированную систему лоббирования российскими врачами интересов крупных фармацевтических компаний. В том или ином виде подобное существует во всем мире, полностью запретить производителям рекламировать и продвигать на внутреннем рынке свои лекарства нельзя, однако в России они должны делать это цивилизовано и в полном соответствии с общепринятыми нормами врачебной этики и с российским законодательством. Производители лекарственных препаратов – и отечественные, и иностранные – когда защищают свои интересы, быстро привлекают на свою сторону необходимые структуры, находят поддержку, создают различные клубы сторонников и пр. Однако это ни в коей мере не должно противоречить интересам больных, а соответствовать интересам общегосударственным, а не только корпоративным. Делая социальную защиту населения одной из первоочередных задач страны, ни в коем случае не следует забывать о том, что лечение должно быть не только дешевым, а в первую очередь высоко эффективным.
Литература
1. Кульчавеня Е.В. Влияние α-блокатора Сетегис (теразозин) на микроциркуляцию в стенке мочевого пузыря (предварительные результаты) / Е.В. Кульчавения, Е.В. Брижатюк // Русский медицинский журнал. – 2003. – Т.11. – №4. – С.31-35.
2. Гориловский, Л.М. Современные представления о диагностике и лечении доброкачественной гиперплазии предстательной железы. / Л.М. Гориловский // В кн.: «Аденома предстательной железы». – Харьков, «Факт», 1997. – C.6776.
3. Градец, Э. Медикаментозная терапия нарушений мочеиспускания. / Э. Градец, Т. Гануш, Ю.А. Пытель, В.В. Борисов // Сов. медицина, – 1984. – №12. – С.16.
4. Кан, Я.Д., Использование альфаадреноблокаторов в лечении расстройств мочеиспускания у больных, перенесших оперативное лечение по поводу ДГПЖ / Я.Д. Кан, А.Е. Вишневский // В кн.: «Пленум Правления Российского общества урологов. – М.,1998. – С.189-190.
5. Кварацхелия А.А. Празозин в терапии больных аденомой предстательной железы: дис.... канд. мед. наук. – М.,1992. – С.112-114.
6. Мазо, Е.Б. Фармакопрофилометрия с альфа-1-А-адреноблокаторами в диагностике инфравезикальной обструкции / Е.Б. Мазо, Г.Г. Кривобородов // В кн.: «Пленум Правления Российского общества урологов. – М.,1998. – С.204-205.
7. Мазо, Е.Б. Значение урофлоуметрического мониторинга при консервативной терапии селективными альфа-1адреноблокаторами больных доброкачественной гиперплазией предстательной железы / Е.Б. Мазо, И.А. Матушевский, Ю.Ю. Никитин // В кн.: «Пленум Правления Российского общества урологов. – М.,1998. – С.205-206.
8. Винаров А. З. Медикаментозная терапия больных гиперплазией предстательной железы: дис… док. мед. наук. М.,1999. – С.64-65.
9. Градец, Э. Медикаментозная терапия нарушений мочеиспускания / Э. Градец, Т. Гануш, Ю.А. Пытель, В.В. Борисов // Советская медицина. – 1984. – №12. – С.16-22.
10. Корниенко В.И. Эффективность медикаментозной терапии больных доброкачественной гиперплазией предстательной: дис.... канд. мед. наук. – Санкт-Петербург, 1997, – С.81-83.
11. Лоран, О.Б. Лечение расстройств мочеиспускания у больных доброкачественной гиперплазией простаты α-адреноблокаторами / О.Б. Лоран, Е.Л. Вишневский, А.Е. Вишневский // Урология. – 1998. – №3 – С.11-13.
12. Сивков, А. В. Применение тамсулозина (Омник) в качестве прогностического теста эффективности лечения ДГПЖ α1-адреноблокаторами / А.В. Сивков, О.И. Аполихин, С.С. Толстова и др. // В кн. «Пленум правления Российского общества урологов». – М.,1998. – С.240-241.
Статья опубликована в журнале "Вестник урологии". Номер №3/2013 стр. 54-68









Комментарии