Мосоян М.С.1 , Аль-Шукри С.Х.1 , Семенов Д.Ю.2 , Есаян А.М.3 , Ильин Д.М.1
1Кафедра урологии, 2 кафедра общей хирургии, 3 кафедра нефрологии и диализа ГБОУ ВПО Первого Санкт-Петербургского государственного медицинского университета имени академика И.П. Павлова Минздрава России, г.Санкт-Петербург Адрес: 197022, г.Санкт-Петербург, ул.Льва Толстого, д.6-8., тел. (921) 9632277 Эл.почта: moso03@yandex.ru, al-shukri@spbmedu.ru, semenov_du@mail.ru, essaian.ashot@gmail.com, melker@mail.ru
Введение
Основным методом лечения больных с локализованным почечно-клеточным раком является хирургический [1]. Все больший интерес хирургов вызывают так называемые «функциональные» результаты резекции почки и нефрэктомии [2,3]. Доподлинно известно, что резекция почки и нефрэктомия, выполненные по поводу локализованного почечно-клеточного рака (ПКР), обеспечивают сопоставимую 5-летнюю опухоль-специфическую выживаемость [4,5]. Также было установлено, что резекция почки имеет преимущество перед нефрэктомией в вопросе сохранения функции почки, что выражается в меньшей вероятности развития или усугубления хронической болезни почек (ХБП) [6,7,8]. Состояние клубочковой системы почек после операции может быть оценено на основании данных о скорости клубочковой фильтрации (СКФ) или нефросцинтиграфии. Неоспорим тот факт, что возникновение или прогрессирование ХБП является серьезным предиктором развития у пациента неблагоприятных сердечнососудистых событий: инфаркта миокарда, инсульта, смерти [9,10]. Все последствия операции, за исключением онкологических показателей, являют собой так называемые «функциональные» результаты, над улучшениями которых и работают исследователи, занимающиеся хирургическим лечением ПКР. Как альтернатива существующим способам улучшения почечной функции при резекции почки (контролируемая гипотензия, селективное выделение и клипирование питающих опухоль сосудов, операция без пережатия почечной ножки) нами был предложен способ резекции в условиях селективной паренхиматозной (регионарной) ишемии. Мы разработали и применили на практике 3 инструмента, которые могут быть использованы в ходе открытой, лапароскопической и роботассистированной резекции почки.
Целью работы явилась сравнительная оценка эффективности выполнения резекции почки в условиях регионарной ишемии и в условиях тотальной ишемии с пережатием сосудов почки.
Материалы и методы
В период с января 2011 г. по октябрь 2013 г. на базах ПСПбГУ им.академика И.П.Павлова и ФМИЦ им. В.А.Алмазова нами было выполнено 110 открытых, лапароскопических и робот-ассистированных резекций почек пациентам с почечно-клеточным раком в стадии T1-2N0M0 (таблица).
Таблица. Предоперационные данные
| Показатель | Группа пережатия почечных сосудов (ПС), п=86 | Группа пережатия почечной паренхимы (ПГ1), п=24 | Р |
| Возраст, лет | 56,3±13,1 (18,0-87,0) | 60,2± 10,7 (42,0-76,0) | 0,183 |
| Пол Мужской Женский |
Количество 47(54,7%) Количество 39 (45,3%) |
Количество 13 (54,2%) Количество 11 (45,8%) |
0,966 |
| Локализация Верхний полюс Средний сег мент Нижний ПОЛЮС |
Количество 21 (24,4%) Количество 34 (39,5%) Количество 31 (36,1%) |
Количество 6 (23,0%) Количество 9 (37,5%) Количество 9 (37,5%) |
0,953 |
| Стадия Т,а (ДО 4 СМ) T1b (4-7 см ) T2a (более 7 см) |
Количество 49 (56,9%) Количество 35 (40,8%) Количество 2 (2,3%) |
Количество 13(54,2%) Количество 11 (45,8%) Количество 0 |
0,806 |
| СКФ, мл/мин/1,73м2 | 76,0±12,1 (58,2-94,5) | 74,0± 11,8 (56,3-91,7) | 0,473 |
Пациенты были поделены на группу резекции с пережатием почечных сосудов (группа ПС, 86 пациентов) и группу резекции с пережатием почечной паренхимы (группа ПП, 24 пациента). В обеих группах операции выполняли открытым, лапароскопическим и роботассистированным способами. Основные данные пациентов по группам достоверно не различались. Так, средний возраст составил 56,3 (18,0-87,0) и 60,2 (42,0-76,0) лет для групп ПС и ПП, соответственно (p=0,183). В группе ПС 54,7% пациентов составляли мужчины, в группе ПП мужчин было 54,2%. В обеих группах для установки диагноза и стадирования процесса выполняли МРТ или КТ с внутривенным контрастированием. По данным лучевой диагностики расположение опухолей в паренхиме почки по группам не различалось. Также группы были сопоставимы и по стадиям опухолевого процесса, однако в группе ПС в 2 случаях резекцию почки выполняли на стадии опухоли Т2а, тогда как в группе ПП операции производили только на стадии Т1.
В группе ПС резекции почек выполняли традиционной техникой с полным выключением почки из кровотока путем наложения сосудистого зажима на почечную ножку. Пациентам группы ПП операции осуществляли в условиях регионарной ишемии, когда из кровотока исключался лишь тот участок почечной паренхимы, который содержал в себе опухоль. Для этих целей было использовано 3 разработанных нами зажима на почечную паренхиму (патенты РФ №107471 от 20.08.2011, №118540 от 27.07.2012, №125837 от 20.03.2013, №2011150672 от 27.06.2013), два из которых применяли в ходе открытой (рисунки 1,2), и один – в ходе робот-ассистированной и лапароскопической резекции (рис. 3,4).
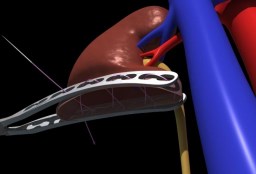
Рис. 1. Зажим Аль-Шукри-Мосояна для открытой резекции почки
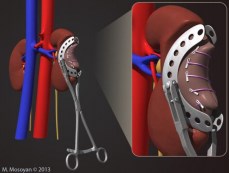
Рис. 2. Зажим Короста-Мосояна для открытой резекции почки
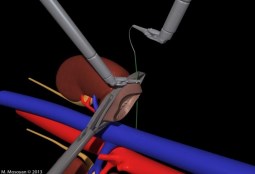
Рис. 3. Зажим Семенова-Мосояна при роботассистированной резекции почки
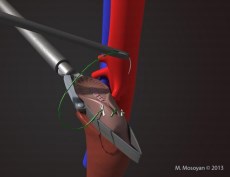
Рис. 4. Зажим Семенова-Мосояна при лапароскопической резекции почки
Оценивали скорость клубочковой фильтрации (СКФ) по формуле CKDEPI до операции, через 24 часа и 1 год после операции. Исходные показатели СКФ по группам достоверно не различались и составляли 76 (58,2-94,5) и 74 (56,3-91,7) мл/мин/1,73 м3 для группы ПС и ПП, соответственно (p=0,473). Изучали также время операции, средний объем кровопотери, время тепловой ишемии (ВТИ, в группе ПС) и длительность селективного пережатия почечной паренхимы (в группе ПП).
Результаты
Средний размер удаленной опухоли был равен 3,4 (1,3-9,0) и 2,8 (2,0-5,6) см для группы ПС и ПП соответственно (p=0,071). Длительность операции по группам достоверно не различалась и составила 118 и 140 мин для группы ПС и ПП, соответственно (p=0,069). Средний объем кровопотери был достоверно ниже в группе ПП: 240 (110-560) мл против 298 (70-700) мл в группе ПС (p=0,047). ВТИ в группе ПС составило 14,4 (8,0-21,9) мин, что превышало длительность селективной ишемии почечной паренхимы в группе ПП (11,8 (7,216,8) мин, p=0,011).
Различия в скорости клубочковой фильтрации были достоверны между группами ПС и ПП как через 24 часа после операции (59 против 70 мл/мин/ /1,73м2 , p=0,0001), так и спустя 1 год наблюдения (50,5 против 65 мл/мин//1,73м2 , p=0,0001) (рисунок 5). Опухоль-специфическая выживаемость в обеих группах за период наблюдения 1 год составила 100%.
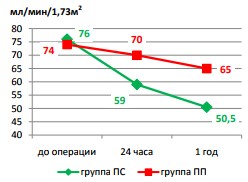
Рис. 5. Динамика СКФ (CKD-EPI) после операции
Обсуждение
Одной из наиболее обсуждаемых тем в сообществе урологов является сохранение почечной функции после резекции почки. С точки зрения «функциональных» результатов на качество резекции может влиять целый ряд факторов, из которых большое значение придается длительности тепловой ишемии [2]. Не существует точного порогового значения ВТИ, ниже которого повреждение почки достоверно не наступает, однако принято считать, что ВТИ менее 20 мин не оказывает существенного влияния на функцию почки [11].
Результаты нашего исследования, напротив, показали, что даже при среднем ВТИ, равном 14,4 мин (группа ПС), снижение почечной функции наступало уже через 24 часа и усугублялось через 1 год. Это позволило нам заключить, что даже относительно непродолжительное ВТИ может сказаться на функциональной способности почек. Наши предположения находят подтверждение в исследованиях Thompson R.H. et al. (2010) и Patel A.R. et al. (2011), которые утверждают, что на отдаленные функциональные результаты резекции почки оказывает влияние каждая минута ишемии [12,13].
Европейские исследователи предлагают ряд способов выполнения резекции почки, которые позволяют исключить тепловую ишемию как фактор, приводящий к худшим функциональным результатам. Одним из таких способов является применение контролируемой гипотензии, при которой системное артериальное давление снижается до 65 mm Hg, что позволяет выполнять резекцию почки без пережатия почечных сосудов с минимально возможной геморрагией [14]. Нельзя не заметить, что при столь низких цифрах АД, особенно в условиях пневмоперитонеума, резко нарушается фильтрация в почечных клубочках. Также могут страдать жизненно важные кислородзависимые органы (сердце, головной мозг), что не позволяет нам считать метод достаточно безопасным.
Более радикальным вариантом этого способа резекции почки является так называемая «беззажимная техника», когда резекция опухоли выполняется без пережатия почечной ножки и при нормальных цифрах АД. Такая процедура неизменно сопровождается значительным, зачастую неконтролируемым, объемом кровопотери из ложа удаленной опухоли [15]. Поэтому способ находит только ограниченное применение при резекции опухолей небольшого размера с преимущественно экзофитным ростом.
Наиболее технически сложным способом выполнить резекцию почки без ишемического повреждения органа является селективная диссекция и клипирование артерий третьего или четвертого порядка, питающих опухоль [16]. Подобные вмешательства могут выполняться в клинике экспертного класса, т.к. требуются значительные навыки работы с сосудами в ограниченном пространстве ворот почки. Для решения таких задач наилучшим образом подходит робот-ассистированный метод резекции почки. Наш опыт применения этого способа резекции подтверждает его эффективность в случаях, когда на этапе предоперационной подготовки по данным МСКТ и МРТ с внутривенным контрастированием визуализируются сосуды третьего и четвертого порядка, питающие опухоль.
Методика селективной паренхиматозной ишемии при резекции почки крайне скупо описана в мировой литературе. Хотя мы предполагаем, что любой опытный хирург в своей практике применял селективную ишемию почечной паренхимы с помощью пальцев рук. В базе данных медицинской литературы PubMed мы находим отдельные работы, в которых авторы описывают наложение различных сосудистых зажимов на паренхиму почки, для того чтобы выполнить резекцию без тотальной ишемии органа [17,18]. Нам не встретилось работ, в которой авторы делились бы опытом применения регионарной ишемии в ходе резекции почки всеми доступными способами: открытым, лапароскопическим и роботассистированным. В малочисленных статьях описан опыт применения специального хирургического зажима Simon (B.Braun, USA) на паренхиму почки [19,20]. В отличие от нашего зажима Семенова-Мосояна для роботассистированных и лапароскопических резекций почки зажим Simon имеет серьезные конструктивные недостатки, которые не позволяют надежно обеспечить гемостаз или избежать соскальзывания. Зажимы Аль-Шукри-Мосояна и Короста-Мосояна, по нашим данным, не имеют аналогов в мире и вместе с роботическим зажимом СеменоваМосояна образуют полноценный набор для выполнения резекции почки без необходимости тотальной ишемии органа. Важной конструктивной особенностью зажима Аль-Шукри-Мосояна является наличие в его браншах специальных отверстий, через которые в зажатом состоянии инструмента возможно наложение непрерывного шва на паренхиматозном органе. К недостаткам лапароскопического инструмента можно отнести то, что использоваться полноценно он может только при опухолях, локализованных в полюсах почки.
В литературе все чаще можно встретить термин «нулевая ишемия» при обсуждении результатов резекции почки. Под этим термином специалисты понимают такие способы выполнения вмешательства, когда на почку не оказывается какого-либо воздействия, приводящего к ишемии даже части органа. К ним относятся описанные выше «беззажимная» техника, техника селективной микродиссекции третичных и четвертичных артерий почки, метод контролируемой гипотензии. Описанный нами подход селективного пережатия почечной паренхимы (селективной паренхиматозной ишемии, регионарной ишемии) скорее всего нельзя в полной мере охарактеризовать как метод «нулевой» ишемии, так как из кровотока временно выключается часть функционирующей паренхимы, окружающей опухолевый узел. Не исключено, что в зоне, которая была подвержена компрессии, возникают изменения, приводящие впоследствии к снижению функциональной активности этого участка паренхимы.
Однако полученные нами результаты динамики СКФ после резекции почки с пережатием сосудов и с пережатием почечной паренхимы позволяют судить о том, что селективная почечная ишемия вызывает меньшее повреждение почечной паренхимы, чем тотальная ишемия почки, и как следствие в большей мере предотвращает развитие и прогрессирование ХБП. Особое значение селективная ишемия паренхимы, как нам представляется, может иметь при резекции единственной (оставшейся) почки.
Данных прямого сравнения регионарной ишемии и «нулевой» ишемии, позволяющих однозначно заявить о преимуществе одного метода над другим, при анализе литературы нами получено не было. Для определения достоверных результатов необходимо накопление большего числа случаев резекции почки в условиях селективной паренхиматозной ишемии, а также требуется проведение рандомизированных сравнительных исследований.
Заключение
Резекция почки в условиях селективного пережатия почечной паренхимы обеспечивает более высокие функциональные показатели, чем классическая резекция с пережатием сосудов почки, сразу после операции и спустя 1 год. Способ селективной (регионарной) ишемии эффективен и легко воспроизводим, и может успешно применяться как при робот-ассистированной, так и при открытой, и лапароскопической резекции почки.
Литература
1. Аляев, Ю.Г. Локализованный и местно распространенный рак почки: нефрэктомия или резекция? / Ю.Г. Аляев, А.А. Крапивин // Онкоурология. – 2005. – Т.№1. – С.10-15.
2. Renal function after partial nephrectomy: effect of warm ischemia relative to quantity and quality of preserved kidney / R.H. Thompson, B.R. Lane, C.M. Lohse et al. // Urology. – 2012. – Vol.79, №2. – P.356-360.
3. Гусев, А.А. Оценка почечных функций и оперативное лечение почечно-клеточного рака / А.А. Гусев, С.В. Евсеев, М.И. Коган // Онкоурология. – 2013. – Т.1. – С.17-23.
4. Novick, A.C. Nephron-sparing surgery for renal cell carcinoma / A.C. Novick // Annu Rev Med. – 2002. – Vol. 53. – P.393-407.
5. Systematic review of oncological outcomes following surgical management of localised renal cancer / S. MacLennan, M. Imamura, M.C. Lapitan et al. // Eur Urol. – 2011. – Vol. 61, №5. – P. 972-993.
6. Systematic review of perioperative and quality-of-life outcomes following surgical management of localised renal cancer / S. MacLennan, M. Imamura, M.C. Lapitan et al. // Eur Urol. – 2012. – Vol. 62, №6. – P.1097-1117.
7. Есаян, А.М. Почечно-клеточный рак и хроническая болезнь почек: внимание к отдаленным неонкологическим исходам / А.М. Есаян, С.Х. Аль-Шукри, М.С. Мосоян // Нефрология. – 2012. – Т.16, №4. – С.94-99.
8. Comparative effectiveness for survival and renal function of partial and radical nephrectomy for localized renal tumors: a systematic review and metaanalysis / S.P. Kim, R.H. Thompson, S.A. Boorjian et al. // J Urol. – 2012. – Vol. 188, №1. – P.51-57.
9. Nephrectomy induced chronic renal insufficiency is associated with increased risk of cardiovascular death and death from any cause in patients with localized cT1b renal masses / C.J. Weight, B.T. Larson, A.F. Fergany et al. // J of Urol. – 2010. – Vol. 183, №4. – P.1317-1323.
10. Muruganandham, K. Chronic kidney disease and small renal tumors: What urologists should know? / K. Muruganandham, A. Mandhani // Indian J Urol. – 2009. – Vol.25, №4. – P.543-544.
11. Assessing the impact of ischaemia time during partial nephrectomy / F. Becker, H. Van Poppel, O.W. Hakenberg // Eur Urol. – 2009. –Vol. 56. – P.625-635.
12. Every minute counts when the renal hilum is clamped during partial nephrectomy / R.H. Thompson, B.R. Lane, C.M. Lohse et al // Eur Urol. – 2010. – Vol. 58. – P.340-345.
13. Patel, A.R. Warm ischemia less than 30 minutes is not necessarily safe during partial nephrectomy: every minute matters / A.R. Patel, S.E. Eggener // Urol Oncol. – 2011. – Vol. 29, №6. – P.826-828
14. Laparoscopic and robotic partial nephrectomy with controlled hypotensive anesthesia to avoid hilar clamping: feasibility, safety and perioperative functional outcomes / R. Papalia, G. Simone, M. Ferriero et al. // J Urol. – 2012. – Vol. 187, №4. – P.1190-1194.
15. Novak, R. Robotic partial nephrectomy without renal ischemia / R. Novak, D. Mulligan, R. Abaza // J Urol. – 2012. – Vol. 79, №6. – P. 1296-1301.
16. Zero ischemia anatomical partial nephrectomy: a novel approach / I.S. Gill, M.B. Patil, A.L. Abreu // J Urol. – 2012. – Vol. 187, №3. – P.807-814.
17. Nephron-sparing surgery for renal tumors using elective parenchymal clamping / F. Denardi, G.M. Borges, W. Silva Jr. et al. // BJU Int. – 2005. – Vol. 96. – P.1036-1039.
18. Efficacy of parenchymal compression in open partial nephrectomies: a comparison with conventional vascular clamping / Y.H. Ko, H. Choi, S.G. Kang et al. // Korean J Urol. – 2010. – Vol. 51. – P.8-14.
19. Laparoscopic partial nephrectomy with selective control of the renal parenchyma: initial experience with a novel laparoscopic clamp / J. Simon, G. Bartsch Jr, F. Finter et al. // BJU Int. – 2009. – Vol. 103, №6. – P.805-808.
20. Whiting, B. Off clamp robotic heminephrectomy: the simon laparoscopic renal pole clamp / B. Whiting, L.-M. Su, A. Yamamoto // J Urol. – 2011. – Vol. 185, №4S. – P.414-415.
Статья опубликована в журнале "Вестник урологии". Номер №3/2014 стр. 3-10









Комментарии