Солодкий В.А, Павлов А.Ю.. Цыбульский А.Д., Пчелинцев А.С.
Сведения об авторах:
- Солодкий В.А. – акад. РАН, д.м.н., профессор, директор ФГБУ РНЦРР Минздрава России, mailbox@rncrr.rssi.ru, AuthorID 440543
- Павлов А.Ю. – д.м.н. профессор, заместитель директора по научно-лечебной работе ФГБУ «РНЦРР» Минздрава России, руководитель клиники урологии, mailbox@rncrr.rssi.ru, AuthorID 206370
- Цыбульский А.Д. – к.м.н., старший научный сотрудник отделения онкоурологии ФГБУ «РНЦРР» Минздрава России, руководитель клиники урологии, vracheg@mail.ru, AuthorID 723876
- Пчелинцев А.С. – клинический ординатор отделения онкоурологии ФГБУ «Российский научный центр рентгенорадиологии» Минздрава, mailbox@rncrr.rssi.ru
Уже более 30 лет низкомощностная брахитерапия с применением радиоактивного 125I (LDR-BT) применяется в качестве лечения локализованного рака предстательной железы (РПЖ) и признана многими руководствами стандартами лечения пациентов групп низкого и промежуточного рисков прогрессирования.
В медицинской практике принято говорить о методах лечения РПЖ, сравнивая последние с радикальной простатэктомией. Радикальная простатэктомия позиционируется как «золотой стандарт» лечения РПЖ. Получая все новые данные о радиотерапевтических методах лечения, сопоставляя качество жизни после различных методов лечения РПЖ и частоту локальных рецидивов, термин «золотой стандарт», применяемый к радикальной простатэктомии, становится довольно-таки спорным. Известно, что контроль над перипростатическим краем предстательной железы (ПЖ) является ключевым в эффективности лечения как при радикальной простатэктомии, так и при брахитерапии. Паталого-анатомические исследования после радикальной простатэктомии показывают, что уже при промежуточном риске инвазивный рост аденокарциномы отмечается у 30-50% пациентов [1,2]. Такая инвазия опухоли является наиболее частой причиной возникновения локального рецидива после хирургического удаления ПЖ [3]. Брахитерапия позволяет захватить в целевой объем перипростатическое пространство, что делает этот метод более перспективным. При планировании брахитерапии такой подход является стандартным, подразумевая постимплантационный отек ПЖ и возможные смещения микроисточников в раннем послеоперационном периоде.
Тем не менее, говоря о развитии локальных рецидивов после LDR-BT, значимой причиной развития последних является именно смещение микроисточников относительно друг друга за счет отека предстательной железы, двигательной активности и половой жизни в раннем послеоперационном периоде. Особое внимание нужно уделять пациентом с объемом ПЖ менее 20 см3, так как при таких объемах железы отмечаются наибольшие риски миграции микроисточников. Именно с целью определения значимости таких смещений через 1 месяц послеоперационного периода проводят компьютерную томографию органов малого таза с последующей повторной дозиметрией [4]. К сожалению, в настоящее время не все пациенты могут провести компьютерную томографию в назначенные сроки.
Несмотря на современные подходы к диагностике и лечению РПЖ, частота рецидивов и прогрессирования у пациентов групп низкого и промежуточного рисков прогрессирования достигает 18% как при радикальной простатэктомии, так и при лучевых методах лечения [5]. Поэтому крайне важно идентифицировать пациентов, которые подвергаются повышенному риску развития рецидива. Инициальный уровень простатспецифического антигена (ПСА), показатель шкалы Глисона и клиническая стадия широко используются в качестве основных факторов риска развития биохимической прогрессии. Тем не менее, остается актуальным вопрос об идентификации других прогностических факторов для улучшения оценки вероятности рецидива у больных РПЖ после различных вариантов лечения.
Цель исследования. Оценить клинические результаты лечения больных локализованным РПЖ, которым применялся метод брахитерапии с использованием радиоизотопа 125I. Определить значимость прогностических факторов, влияющих на раково-специфическую выживаемость.
МАТЕРИАЛЫ И МЕТОДЫ
В настоящее исследование вошли 290 пациентов с диагнозом РПЖ групп низкого и промежуточного рисков прогрессирования. Всем пациентам в условиях Российского научного центра рентгенорадилогии Минздрава России в период с 2011 – 2017 гг. проведена LDR-BT до суммарной очаговой дозы (СОД) 145 Гр. Все имплантации выполнялись под ультразвуковым (УЗ) контролем биплановым датчиком, спинномозговой анестезией, с использованием микроисточника 125I. Средний возраст больных в группе составил 65,7 лет (от 50 до 81 года). Медиана наблюдения составила 42 мес. (12-96 мес.). Подробная характеристика пациентов представлена в таблице 1.
Таблица 1. Характеристика пациентов
| Показатель | Значение | |
|---|---|---|
| Средний возраст (лет) | 47-83 (65,7±6,7) | |
| n | 290 | 100% |
| Стадия | ||
| Т1а-Т2а | 160 | 55,10% |
| 2Ь | 78 | 26,90% |
| Т2с | 52 | 18% |
| Индекс Глисона (Gleason score) | ||
| G1 - Gleason score 5-6 | 235 | 81% |
| G2 - Gleason score 7 (3+4) | 47 | 16,20% |
| G3 - Gleason score 7 (4+3) | 8 | 2,70% |
| Инфильтративный рост/ периневральная инвазия | ||
| Нет | 251 | 86,50% |
| Инфильтративный рост | 26 | 8,90% |
| Периневральная инвазия | 11 | 4,20% |
| Инфильтративный рост + периневральная инвазия | 2 | 0,70% |
| Максимальный уровень ПСА до лечения | ||
| < 10 нг/мп | 195 | 67,30% |
| 10-20 нг/мл | 95 | 32,70% |
| ТУР ПЖ/аденомэктомия | ||
| Нет | 264 | 67,20% |
| ТУР | 23 | 7,9% |
| Аденомэктомия | 2 | 0,7% |
| Группа риска NCCN | ||
| Низкий | 115 | 39,6 % |
| Промежуточный | 175 | 60,4 % |
ПСА – простат-специфический антиген; ТУР ПЖ – трансуретральная резекция предстательной железы; NCCN - National Comprehensive Cancer Network.
При первичном обращении каждому пациенту определялась клиническая стадия заболевания согласно данным магнитно-резонансной томографии (МРТ), остеосцинтиграфии, трансректального ультразвукового исследования (ТРУЗИ), ПЖ, ПСА и гистологического заключения (индекс Глисона). Риск прогрессирования определялся согласно критериям NCCN – NationalComprehensiveCancer Network [6].
Перед процедурой имплантации пациентам определялся объем ПЖ, урофлоуметрия, ультразвуковое исследование почек, мочевого пузыря, количество остаточной мочи. Все пациенты заполняли опросники IPSS и МИЭФ-5.
Динамическое наблюдение после лечения осуществлялось каждые 3 мес. в течение 1-го года, каждые 6 мес. в течение следующих 2 лет и в дальнейшем каждый год. При необходимости сроки наблюдения могли меняться в индивидуальном порядке. При подозрении на рецидив заболевания пациентам проводилась магнитно-резонансная томография органов малого таза, остеосцинтиграфия, позитронно-эмиссионная томография (ПЭТ-КТ) с Ga+PSMA. При подозрении на локальный рецидив, пациентам выполнялась повторная биопсия ПЖ.
В качестве первичной конечной точки исследования выступала ПСАспецифическая выживаемость. Выживаемость без биохимического рецидива (раково-специфическая выживаемость (РСВ)) оценивалась на основании критериев Phoenix (достигнутый при динамическом наблюдении минимальный уровень ПСА + 2нг/мл) методом КапланаМейера. Значения p ниже 0,05 считались статистически значимыми. Статистический анализ был выполнен с использованием программы SPSS v. 17. Оценка поздней токсичности проводилась согласно классификации RTOG/EORTC.
Проведен однофакторный и многофакторный регрессионный анализ пропорциональных рисков Кокса. В качестве изучаемых факторов взяты следующие показатели: клиническая стадия заболевания (cT1a-T2a против T2b и против T2c), индекс Глисона (5-6 против 7 (3+4) и против 7 (4+3)), инфильтративный рост и периневральная инвазия опухоли, максимальный уровень ПСА (ПСА < 10 нг/мл и ПСА ≥ 10 нг/мл), наличие ТУР или аденомэктомии в анамнезе, количество активностей источников, активность источников (активности < 0,3 мКи, 0,3-0,5 мКи, более 0,5 мКи и комбинация высокой и низкой активности (< 0,3 мКи + 0,4-0,7 мКи).
РЕЗУЛЬТАТЫ
Выживаемость
Медиана времени наблюдения в группе составила 42 мес. (от 12 до 96 мес.). Общая выживаемость в группе составила 98,6%. За указанный период времени умерло 4 пациента, из них 1 – по причине прогрессирования РПЖ. Общая безрецидивная ПСА-специфическая выживаемость составила 91,4%. В группах низкого и промежуточного рисков прогрессирования ПСА-специфическая выживаемость составила 98,3% и 86,8%, соответственно. При этом всего прогрессирование заболевания отмечено у 25 пациентов. У 10 из них выявлен биохимический рецидив, у 10 – подтвержден локальный рецидив опухоли, у 4 пациентов отмечены отдаленные метастазы в лимфоузлы или в кости скелета и у 1 пациента выявлен локальный рецидив и отдаленные метастазы. Графики кривых РСВ представлены на рисунке 1. Отмечена статистически значимая разница РСВ в зависимости от группы риска.
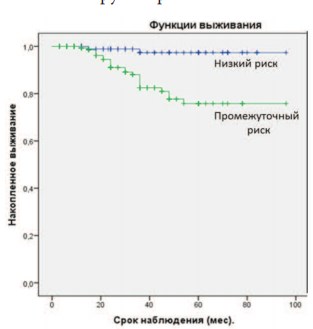
Рис. 1. РСВ в общей когорте пациентов в зависимости от группы риска. (Plog-rank = 0,001)
При анализе зависимости развития прогрессирования заболевания от клинической стадии процесса, мы выявили, что статистически значимой разницы РСВ в группах пациентов со стадиями T1a-T2a и T2b не было и она составляла 96,2% и 94,9%, соответственно. Однако отмечены статистически достоверные отличия РСВ в указанных группах при сравнении их с группой пациентов с клинической стадией T2c, где этот показатель составил 71,2% (р < 0,001) (рис. 2).
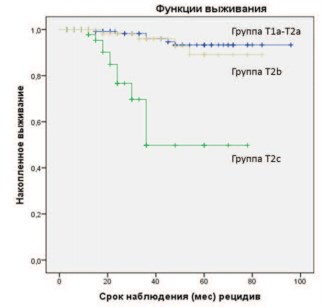
Рис. 2. РСВ в общей когорте пациентов в зависимости от клинической стадии заболеванияа. (Plog-rank < 0,001)
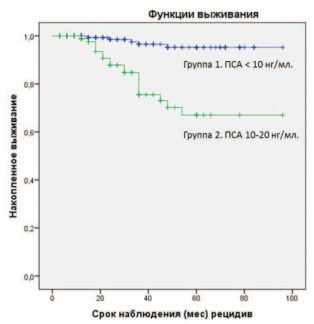
Рис. 3. РСВ в общей когорте пациентов в зависимости от инициального уровня ПСА. (Plog-rank < 0,001)
Как видно из графика на рисунке 2, у пациентов с клинической стадией T2c результаты безрецидивной выживаемости хуже, чем в других исследуемых группах.
Как видно из графика на рисунке 3, уровень инициального ПСА значимо влиял на результат лечения. При этом надо отметить, что РСВ в группах < 10 нг/мл и 10-20 нг/мл составила 97,4 и 79,8 %, соответственно (p<0,001).
При анализе зависимости РСВ и индекса Глисона в группах выявлено, что степень злокачественности опухоли служит существенным фактором, влияющим на выживаемость (рис 4).
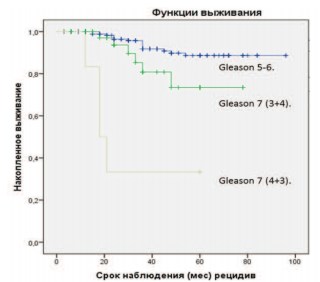
Рис. 4. РСВ в общей когорте пациентов в зависимости от индекса Глисона. (Plog-rank Gleason 5-6 и 7 (4+3)< 0,001; Plog-rank Gleason 5-6 и 7 (3+4) = 0,052; Plog-rank Gleason 7 (3+4) и 7 (4+3) = 0,003;)
Выявлено, что у пациентов, градация опухоли которых соответствовала индексу Глисона 7 (4+3), отмечено прогрессирование в 50% случаев. Этот показатель значимо отличался от групп пациентов, индекс Глисона которых составлял 6 (3+3) и 7 (3+4) (р<0,05). РСВ выживаемость в группах с индексом Глисона 6 (3+3), 7 (3+4) и 7 (4+3) составила 93,5%, 87% и 50% соответственно. Надо отметить, что последняя группа насчитывала всего 8 пациентов. У 2 из них отмечены отдаленные метастазы, а еще у 2 пациентов отмечен биохимический рецидив заболевания, но характер роста кривой ПСА говорит генерализации процесса. Кроме того, у большинства этих пациентов были и такие неблагоприятные прогностические факторы, как клиническая стадия Т2b-T2с и уровень инициального ПСА более 10 нг/мл. Локальных рецидивов в этой группе пациентов отмечено не было.
Так же отмечено, что наличие периневральной инвазии является достоверным фактором, влияющим на РСВ. В группах пациентов без периневральной инвазии и с периневральной инвазией частота локальных рецидивов встречалась в 2,4% и 36,3% соответственно (р = 0,028).
При анализе влияния на РСВ других переменных (ТУР ПЖ, количество активностей источников) нами не отмечено статистически значимых зависимостей (рис. 5).
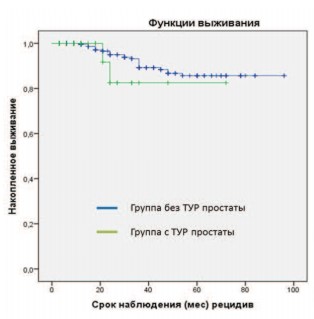
Рис. 5. РСВ в общей когорте пациентов в зависимости от ТУР предстательной железы. (Plog-rank = 0,319)
Качество жизни
При оценке качества жизни пациентов, нужно отметить хорошую переносимость LDR-BT и минимальное количество токсических реакций. В основном все пациенты вернулись к обычному уровню жизни через 5-6 мес. после лечения. Так, средний суммарный балл IPSS до лечения составлял у пациентов моложе 60 лет, 61-70 лет и более 71 года 7,1, 7,3 и 9 баллов, соответственно. Средний суммарный балл IPSS после лечения составлял у пациентов моложе 60 лет, 61-70 лет и более 71 года 8,1, 7,3 и 8,9 баллов, соответственно, что соответствует среднему или умеренному уровню нарушений мочеиспускания. Надо отметить, что у пациентов, в анамнезе у которых была проведена ТУР ПЖ, суммарный балл IPSS после лечения не отличался и оказался даже ниже средне статистических значений (6,4 балла). При этом не получено достоверной связи между количеством имплантированных микроисточников и изменением IPSS в послеоперационном периоде, но, тем не менее, отмечено, что у пациентов, которым было имплантировано более 70 микроисточников, сумма баллов IPSS бала больше, чем у пациентов с меньшим количеством имплантированных источников.
Токсические реакции
Нами проведен анализ выраженности ранних и поздних генитоуринарных (ГУ) и гастро-интерстициальных (ГИ) токсических реакций.
Ранние ГУ токсические реакции 2 и 3 степени отмечены в 17,8% и 1,7% случаев, соответсвенно. Поздние ГУ токсические реакции 2 и 3 степени отмечены в 10,5% и 1,7%. Ранние ГИ токсические реакции 1 и 2 степени отмечены в 29,4% и 2,1% наблюдений, соответственно. Поздние ГИ осложнения отмечались крайне редко. Осложнений IV степени выявлено не было.
При анализе влияния различных факторов на развитие токсических реакций нами были выявлены значимые закономерности. Так, на выраженность ГИ токсических реакций влияла активность имплантированных микроисточников. Отмечено, что у пациентов, которым применялись источники активностью более 0,6 мКи, отмечались более выраженные как ранние, так и поздние ГУ токсические реакции по сравнению с пациентами, которым использовались источники с меньшей активностью (p<0,05). Так же отмечено, что у пациентов, которым применялись комбинации 3-х активностей (с целью обеспечения более гомогенного распределения дозы внутри предстательной железы), ранние и поздние токсические реакции наблюдались реже, чем у пациентов, которым выполнялась имплантация микроисточников 1-й и 2-й активностей (р<0,05). Однако на общую ПСА-специфическую выживаемость количество используемых активностей не влияло. В группе пациентов, которым использовались 3 активности, поздние токсические реакции наблюдались только 1-й степени. У пациентов, в анамнезе у которых отмечалось учащенное мочеиспускание и нарушения мочеиспускания по данным урофлоуметрии и опросников IPSS, так же отмечено значимое увеличение ранних и поздних токсических реакций в послеоперационном периоде. При этом надо отметить, что мы не получили достоверные различия в выраженности ГИ и ГУ токсических реакций в группах пациентов, у которых ранее была выполнена ТУР предстательной железы. Так же не влияли такие переменные как уровень тестостерона до операции и объем предстательной железы.
Развитие эректильной дисфункции
Сохранение эректильной функции (ЭФ) является одним из основных параметров, определяющих уровень качества жизни больных после лечения РПЖ. Это должно учитываться при выборе тактики лечения. Нами проведен анализ влияния брахитерапии на развитие нарушений ЭФ. Было исследовано ЭФ 88 пациентов. Все пациенты были заинтересованы в сохранении ЭФ после лечения основного заболевания. Все 88 больных разделены на 3 возрастные группы (моложе 60 лет, 61-70 лет и более 70 лет). Оценка проводилась по заполнению опросников МИЭФ-5 до и после лечения в течение 4-5 лет наблюдения.
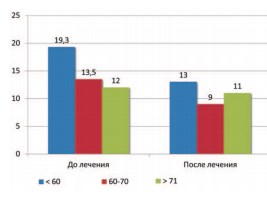
Рис 6. Сравнительная характеристика средних значений баллов МИЭФ-5 до и после брахитерапии в различных возрастных группах
Нами отмечено, что средние значения МИЭФ-5 было больше в группе пациентов младше 60 лет как до, так и после лечения. Наихудшие результаты отмечены в возрастной группе пациентов (рис. 6).
Анализ ЭФ показал, что из 88 пациентов, которые были заинтересованы в сохранении половой жизни после брахитерапии, у 15% отмечено полное сохранение ЭФ через 4-5 лет наблюдения. 12% и 13% отмечали эректильную дисфункцию (ЭД) умеренной и легкой степени. 60% больных спустя 4-5 лет наблюдений отмечали развитие выраженной ЭД. При этом значимая корреляция в развитие ЭД отмечена у тех пациентов, которым применялся 1 тип источников с 1 активностью более 0,5 мКи. У таких пациентов ЭД тяжелой степени развивалась в 64% случаев. Однако у пациентов, которым применялись комбинации источников различной активности, частота развития ЭД тяжелой степени отмечена в 50% случаев.
Надо сказать, что применение андрогендепривационной терапии (АДТ) является важным фактором развития ЭД у пациентов, перенесших брахитерапию. Так, в нашем исследовании средний балл МИЭФ-5 через 4-5 лет после лечения у пациентов, которым не проводилась АДТ и которым проводилась в режиме максимальной андрогенной блокады, составлял 15,2 и 9,7 баллов соответственно (p=0,023).
ОБСУЖДЕНИЕ
Брахитерапия с применением радиоактивного 125 I во всем мире признана эффективным методом лечения локализованного РПЖ групп низкого и промежуточного рисков прогрессирования. Однако нужно понимать, что на сегодняшний день существующий объем диагностических данных не позволяет однозначно говорить об эффективности лечения у пациентов только низкого или только промежуточного рисков. Классическим примером является градация опухоли по шкале Глисона. С момента своего появления оценка по шкале Глисона является важным прогностическим фактором, определяющим результат лечения рака предстательной железы. Об этом свидетельствует тот факт, что почти каждая система стратификации риска рака предстательной железы и различные номограммы включают показатель Глисона в качестве прогностической переменной [7]. Тем не менее, в каждом отдельном подмножестве баллов по Глисону сохраняется степень неоднородности. Это особенно видно при анализе рака с индексом Глисона 7, где некоторые исследования показывают, что первичный паттерн Глисона 4 несет более высокий риск биохимического рецидива, чем первичный паттерн 3 [7,8]. Кроме того, такую же важную значимость имеют такие показатели как клиническая стадия опухолевого процесса и инициальный уровень ПСА.
Согласно полученным нами данным, независимыми факторами, значимо влияющими на РСВ, явились: клиническая стадия Т2с, индекс Глисона 7, особенно с преобладанием паттерна 4, инициальный уровень ПСА более 10 нг/мл. Так же мы определили, что периневральная инвазия является 4-м независимым предиктором развития прогрессирования. Это подтверждают и некоторые современные работы, акцентирующие внимание на наличие признаков периневральной инвазии при первичной диагностике РПЖ [9,10]. Важным фактором агрессивного поведения как РПЖ, так и любой другой опухоли является способность нарушать базальные мембраны и распространяться за пределы органа. Периневральная инвазия обсуждается как важный путь экстрапростатического распространения при РПЖ. Недавние исследования in vitro предположили сложный механизм нейроэпителиального взаимодействия. Присутствие очагов РПЖ приводило к значительному увеличению количества капсульных нервов и площади поверхности капсульных нервов по сравнению с секторами без опухолей [11,12]. Данный факт подтверждает результаты ранее проведенных исследований, позволяющие предположить, что наличие очагов РПЖ может привести к сложным нейроэпителиальным взаимодействиям, приводящим к росту нервов, вызванных РПЖ при инвазивном характере роста опухоли.
ЗАКЛЮЧЕНИЕ
По данным анализа пропорциональных рисков Кокса, независимыми факторами, влияющими на показатель РСВ у пациентов, получивших лечение в виде брахитерапии с использованием радиоизотопа 125I, явились клиническая стадия заболевания, индекс Глисона, инициальный уровень ПСА и наличие периневральной инвазии.
Надо отметить, что в нашем исследовании распространенность периневральной инвазии опухоли встречалась у 5% пациентов. Такой небольшой процент мог быть следствием разных тактик и схем биопсий, проведенных в различных учреждениях. По факту их могло быть гораздо больше, как и не диагностируемых стадий сТ3а, которые только после простатэктомии выявляются в среднем в 30% случаев. Это означает, что примерно такой же процент пациентов с Т3а будет и при брахитерапии. Тем не менее, наше исследование определило достоверную корреляцию развития рецидива и наличия периневральной инвазии, что позволяет нам определить его как независимый фактор, влияющий на РСВ у больных после проведения брахитерапии (р = 0,028).
В целом же надо отметить, что брахитерапия с использованием радиоизотопа 125I показала себя высокоэффективным методом лечения РПЖ с возможностью сохранения качества жизни пациентов на том уровне, которое было до начала лечения заболевания. Учитывая низкое количество осложнений со стороны мочеполовой системы, брахитерапию можно рассматривать как метод выбора у соматически отягощенных больных, а также у больных, для которых сохранение эректильной функции в послеоперационном периоде имеет немаловажное значение.
ЛИТЕРАТУРА
- Davis BJ, Pisansky TM, Wilson TM, Rothenberg HJ, Pacelli A, Hillman DW, et al. The radial distance of extraprostatic extension of prostate carcinoma: implications for prostate brachytherapy. Cancer 1999;85:2630-2637.
- Kattan MW, Skardino PT. Prediction of progression: normorams of clinical utility. Clin Prostate Cancer 2002;1(12): 90-96.
- BasiriA, de la Roosette JJ, Tabatabaei S, Woo H, Laguna M, Shemshaki H. Comparison of retropubic, laparoscopic and robotic radical prostatectomy: who is the winner? World J Urol 2018;36(4):609-62. doi: 10.1007/s00345-018-2174-1
- Зырянов А.В., Ощепков В.Н., Свиридов П.В., Баранов А.В., Бирюков В.А., Коротков В.А., и др. Рекомендации по лечению рака предстательной железы с помощью низкодозной перманентной внутритканевой лучевой терапии (брахитерапии). Экспертное совещание 4 октября 2014, Москва. Экспериментальная и клиническая урология 2015;(2):37-46.
- Fossati N, Karnes RJ, Cozzarini C, Fiorino C, Gandaglia G, Joniau S, Boorjian SA, Goldner G, et al. Assessing the Optimal Timing for Early Salvage Radiation Therapy in patients with prostate-specific antigen rise after radical prostatectomy. Eur Urol 2016;69(4):728-733. doi: 10.1016/j.eururo.2015.10.009.
- Clinical Practice Guidelines in Oncology. National Comprehensive Cancer Network (NCCN) 2018. URL: https://www.nccn.org/professionals/physician_gls/pdf/prostate.pdf
- Bittner N, Merrick GS, Butler WM, Galbreath RW, Adamovich E, Wallner KE. Gleason score 7 prostate cancertreatedwith interstitial brachytherapywith orwithout supplemental external beam radiation and androgen deprivation therapy: Is the primary pattern on needle biopsy prognostic? Brachytherapy 2013;12(1):14-18. doi: 10.1016/j.brachy.2012.05.002
- Uesugi T, Saika T, Edamura K, Nose H, Kobuke M, Ebara S, Abarzua F, et al. Primary Gleason grade 4 impact on biochemical recurrence aer permanent interstitial brachytherapy in Japanese patients with low- or intermediate-risk prostate cancer. Int J Radiat Oncol Biol Phys 2012;82(2):e219-23. doi: 10.1016/j.ijrobp.2011.04.018
- Zareba P, Flavin R, Isikbay M, Rider JR, Gerke TA, Finn S, et al. Perineural invasion and risk of lethal prostate cancer. Cancer Epidemiol Biomarkers Prev 2017;26(5): 719–726. doi: 10.1158/1055-9965.EPI-16-0237.
- Li-jin Zhang L, Wu B, Zha ZL, Qu W, Zhao H, Yuan J, Feng YJ. Perineural invasion as an independent predictor of biochemical recurrence in prostate cancer following radical prostatectomy or radiotherapy: a systematic review and metaanalysis. BMC Urol 2018;18(1):5. doi: 10.1186/s12894-018-0319-6
- BrundlJ, Schneider S, Weber F, Zeman F, Wieland WF, Ganzer R.Computerized quantification and planimetry of prostatic capsular nerves in relation to adjacent prostate cancer foci. Eur Urol 2014;65(4):802–808. doi: 10.1016/ j.eururo.2013.04.043
- Reeves F, Hovens CM, Harewood L, Battye S, Peters JS, Costello AJ. Corcoran NM. Does perineural invasion in a radical prostatectomy specimen predict biochemical recurrence in men with prostate cancer? Can Urol Assoc J 2015; 9(5-6): e252–e255. doi: 10.5489/cuaj.2619
Статья опубликована в журнале "Экспериментальная и клиническая урология" №2 2019 г., стр. 44-49









Комментарии