Журнал "Экспериментальная и клиническая урология" Выпуск №3 за 2015 год
Котов С.В.
Общепринятым ориентиром в выборе того или иного варианта уретропластики при стриктурах бульбозного отдела уретры является протяженность рубцового поражения. Так, при стриктурах бульбозного отдела протяженностью до 1-2 см наиболее часто применяется внутренняя оптическая уретротомия (ВОУТ). При поражении уретры до 2-3 см – операция Хольцова (иссечение стриктуры и прямой анастомоз/анастомотическая уретропластика конец в конец). При стриктурах данного отдела протяженностью более 34 см традиционно применяются аугментационные методы операции (аугментационный анастомоз и onlay техники) или заместительные (многоэтапные) методики. Анастомотическая уретропластика без пересечения спонгиозного тела является новым вариантом уретропластики при коротких стриктурах бульбозного отдела уретры. Но данная методика требует оценки отдаленных результатов для определения ее места в лечении стриктур мочеиспускательного канала у мужчин.
МАТЕРИАЛЫ И МЕТОДЫ
В период с июля 2012 по май 2015 г. в ГКБ № 1 им. Н.И. Пирогова анастомотическая уретропластика без пересечения спонгиозного тела была выполнена 20 пациентам. Показанием к операции явилась стриктура бульбозного отдела уретры, протяженностью менее 2,0 см и не имеющая посттравматического генеза.
Клиническая характеристика группы представлена в таблице 1. По этиологическому фактору преобладали стриктуры уретры ятрогенного происхождения (75%). При этом в 12 из 20 случаев формирование стриктуры было поздним осложнением трансуретральных вмешательств. В подавляющем большинстве случаев (95%) стриктура локализовалась в проксимальной части бульбозного отдела уретры. Это место типично для травмы мочеиспускательного канала во время трансуретрального введения инструментов. Пациентам с посттравматическими стриктурами подобные операции не выполнялись в связи с прогнозированием наличия в зоне стриктуры спонгиофиброза.
Во всех случая операция начиналась стандартно. Пациент укладывался в литотомическую позицию. Выполнялся срединный промежностный доступ с рассечением бульбоспонгиозной мышцы до бульбозного отдела уретры. Циркулярно мобилизировался весь бульбозный отдел уретры: дистально – до пеноскротального угла; проксимально – по дорзальной поверхности до мембранозного отдела, по вентральной поверхности – не доходя 2-3 см до бульбарных артерий, тем самым сохраняя их. Далее, ориентируясь на проведенный до стриктуры катетер Фолея № 20, уретра продольно рассекалась в проксимальном направлении по дорзальной поверхности в проекции стриктуры. Далее уретропластика выполнялась по одному из трех вариантов:
- при протяженности стриктуры до 1,0 см после продольного рассечения уретры над стриктурой производилось поперечное ушивание дефекта, т.е. реализовался «принцип Heineke-Mikulicz» (11 пациентов);
- при стриктурах протяженностью 1,0-2,0 см выполнялась «стриктуропластика по Mundy» (5 пациентов). В этом варианте пораженный рубцовым процессом участок слизистой циркулярно иссекался внутри просвета с сохранением подлежащего спонгиозного тела (рис. 1 А, Б). Далее по вентральной полуокружности накладывался анастомоз между здоровыми концами слизистой внутри просвета уретры (рис. 2). Продольный разрез уретры по дорзальной полуокружности ушивался поперечно по принципу HeinekeMikulicz;
- при наличии непротяженной облитерации проксимальной части бульбозного отдела уретры выполнялась «сосудосберегающая анастомотическая пластика по Jordan» (4 пациента). При данной методике пораженный сегмент слизистой уретры полностью резецировался с сохранением подлежащей вентральной части спонгиозного тела. Далее концы здоровой слизистой спатулировались и выполнялся циркулярный анастомоз (рис. 3А,Б).
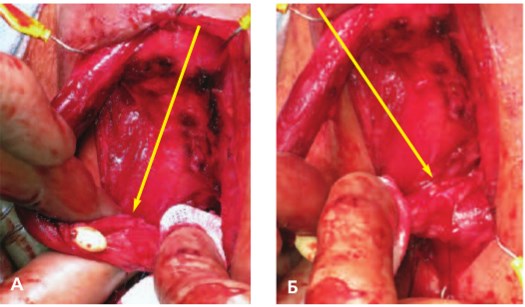
Рис. 1. Края неизмененной слизистой уретры (указаны стрелкой) после иссечения стриктуры: A – дистальный край, Б – проксимальный край
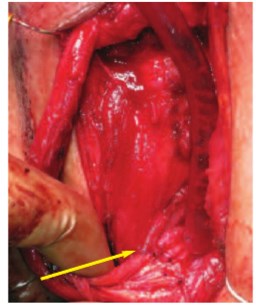
Рис. 2. Анастомоз между краями слизистой внутри уретры (указан стрелкой)
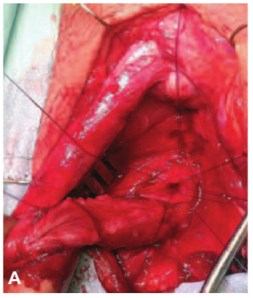
Рис. 3А. Модификация выполнения сосудосохраняющей анастомотической уретропластики по Jordan: А – резекция слизистой уретры со стриктурой
Таблица 1. Клиническая характеристика пациентов, перенесших анастомотическую уретропластику без пересечения спонгиозного тела
| Показатель | Значение |
|---|---|
| Количество пациентов | 20 |
| Медиана возраста (25 и 75 перцентиль), лет | 68,5 лет (41,5 ; 74,8) |
| Этиология стриктуры, кол-во пациентов (%) Воспалительная Ятрогенная: трансуретральные вмешательства чреспузырная аденомэктомия Идиопатическая |
1 (5,0%) 15 (75.0%) 12 (60,0%) 3 (15,0%) 4 (20,0%) |
| Локализация стриктуры бульбозный отдел проксимальный бульбозный отдел |
1 (5,0%) 19 (95,0%) |
| Медиана протяженности стриктуры (25 и 75 перцентиль) Min-max, см |
1,0 (0,86; 1,13) 0, – 2,0 |
| Наличие цистостомического дренажа, количество пациентов (%) | 4 (20,0%) |
| Медиана показателя максимальной скорости мочеиспускания, мл/с (25 и 75 перцентиль) |
4,5 мл/с (5,1; 8,5) |
| Предшествующее лечение Нет ВОУТ |
10 (50%) 10 (50%) |
| Средний показатель шкалы IPSS, баллы | 23,6 + 2,0 |
| Медиана QoL, (25 и 75 перцентиль), баллы | 4,5 (4,0; 5,0) |
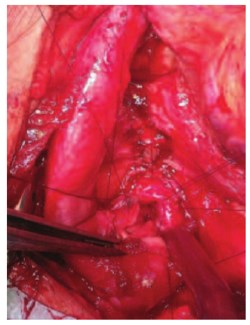
Рис. 3Б. Модификация выполнения сосудосохраняющей анастомотической уретропластики по Jordan: Б – прямой анастомоз уретры конец в конец.
С целью проверки герметичности швов ретроградно вводился раствор индигокармина. При определении места экстравазации жидкости накладывался дополнительный анастомотический шов. Мочевой пузырь дренировался силиконовым уретральным катетером № 14-16 Сh. Далее выполнялось восстановление целостности бульбоспонгиозной мышцы и послойное ушивание раны. Дренирование послеоперационной раны проводили по необходимости.
Все пациенты были активизированы вечером в день операции. Для купирования болевого симптома использовались нестероидные противовоспалительные средства. Антибактериальная терапия не назначалась. Время пребывания пациента после операции в стационаре составило 2-3 дня. Пациент выписывался из стационара с уретральным катетером. Амбулаторно в назначенный день выполнялась ретроградная перикатетерная уретрография (3-12 сутки). При отсутствии затека контрастного вещества удаление уретрального катетера совмещалось с выполнением микционной цистоуретрографии. В этот же или на следующий день пациенту выполнялась урофлоуметрия.
Таблица 2. Среднее значение показателя максимальной скорости мочеиспускания до и после операции у пациентов после анастомотической уретропластики без пересечения спонгиозного тела
| Показатель | До операции | После операции | 3 месяца | 6 месяцев | 12 месяцев |
|---|---|---|---|---|---|
| ср Q max, мл/с | 4,5 мл/с | 25,07±4,5 | 24,6±3,4 | 23,8±3,5 | 24,75±4,8 |
Медиана наблюдения составила 16 месяцев (от 3 до 35). Контрольное обследование в объеме урофлоуметрии выполнялось через 3, 6 и 12 месяцев после операции, ретроградная уретрография проводилась через 6 месяцев после операции. Рецидивом стриктуры считалось возникновение сужения мочеиспускательного канала, требующее инвазивного вмешательства (бужирование, внутренняя оптическая уретротомия – ВОУТ, повторная уретропластика).
РЕЗУЛЬТАТЫ
После удаления уретрального катетера самостоятельное мочеиспускание восстановилось у всех пациентов. В период наблюдения рецидив возник у трех пациентов, т.е. эффективность операции составила 85%. Если рассмотреть каждую методику отдельно, то рецидив после уретропластики по Heineke-Mikulicz отсутствовал у 9 из 11 пациентов (81,8%), после стриктуропластики по Mundy – у 4 из 5 пациентов (80%), после сосудосберегающей пластики по Jordan – у 4 из 4 (100%).
Результаты средних показателей максимальной скорости мочеиспускания и их динамика втечение периода наблюдения представлены в таблице 2.
Послеоперационные осложнения были зарегистрированы у трех пациентов. У двух больных на вторые сутки после операции была диагностирована незначительная гематома мягких тканей промежности и мошонки, не повлиявшая на изменение терапии в послеоперационном периоде. У одного пациента возник острый эпидидимит на 18-е сутки после операции, который был вылечен консервативно.
У всех пациентов с сохранной половой функцией никаких сексуальных дисфункций в виде снижения кровенаполнения, чувствительности головки полового члена, эректильной или эякуляторной дисфункции не было.
ОБСУЖДЕНИЕ
Короткая стриктура бульбозного отдела уретры является наиболее благоприятной формой, т.к. имеет наилучшие результаты лечения методом уретропластики. Так, традиционно «золотым стандартом» при стриктурах бульбозного отдела протяженностью до 2 см является анастомотическая уретропластика конец в конец, при которой положительный результат операции составляет 90-98% [1, 2]. Даже при наблюдении за пациентами в течение 15 лет эффективность анастомотической уретропластики остается высокой (86%) [3]. При коротких стриктурах (до 1 см) проксимальной части уретры, большинством урологов принимается решение о выполнении внутренней оптической уретротомии – метода более простого для исполнения врачом, обладающего меньшей инвазивностью для пациента и требующего в большинстве случаев более короткого периода дренирования мочевого пузыря катетером и, следовательно, более короткой госпитализации. При сравнении оптической уретротомии и анастомотической уретропластики, результаты последней по данным литературы значимо превышают таковые при эндоскопическом методе лечения, хотя специальных сравнительных рандомизированных исследований не проводилось. Альтернативным оперативным вмешательством может служить анастомотическая уретропластика без пересечения спонгиозного тела. Данная методика, независимо от применения одной из трех ее модификаций, позволяет сохранить антеградный кровоток в спонгиозном теле в пораженном отделе уретры [4, 5, 6]. Это особенно важно для пациентов с сохраненной сексуальной функцией или с тяжелой степенью стрессовой формы недержания мочи и необходимостью установки искусственного мочевого сфинктера, с множественным рубцовым поражением передней уретры или при сочетании стриктуры уретры и гипоспадии.
Принципиальным моментом в определении показаний к анастомотической уретропластике без пересечения спонгиозного тела является деление коротких стриктур бульбозного отдела по этиологическому принципу на посттавматические и нетравматические. При постравматических стриктурах развивающийся рубцовый процесс в спонгиозном теле на уровне травмы приводит к нарушению кровотока в этом отделе уретры, что делает бессмысленным сохранение пораженного участка спонгиозного тела, а также может увеличивать риски рецидива стриктуры.
Ни у одного из оперированных нами пациентов на этапах доступа и мобилизации бульбозного отдела уретры не было отмечено признаков спонгиофиброза в виде изменения цвета, уплотнения спонгиозного тела по вентральной поверхности, спаянности последнего с бульбоспонгиозной мышцей, рубцовых изменений периуретральных тканей. Это объясняется тем, что данная операция не выполнялась больным с травматическим генезом стриктуры и для данной операции были отобраны пациенты со стриктурами нетравматического генеза, т.е. с потенциально сохраненным кровотоком в спонгиозном теле и минимально выраженным спонгиофиброзом. Интраоперационно это подтверждалось обильным кровотечением из спонгиозного тела в просвет уретры после иссечения измененного участка слизистой.
Как видно, первые результаты нового метода уретропластики очень обнадеживающие. Согласно данным комплексного обследования эффективность операции составила 85%. При этом наилучшие результаты были при использовании модификации Jordana (100%). Вероятнее всего это обусловлено тем, что по данной методике пораженный участок слизистой иссекается полностью и анастомоз мнжду здоровыми участками уретры накладывается по всей окружности. Но вопрос о показаниях к данной методике пока остается открытым. Альтернативными вариантами лечения в такой ситуации могут служить внутренняя оптическая уретротомия или иссечение уретры с прямым анастомозом, т.е. анастомотическая пластика уретры. В настоящее время в литературе нет данных проспективных рандомизированных исследований сравнивающих новую методику уретропластики и уже зарекомендовавшие себя варианты лечения. Но при изучении отдаленных результатов операций (2007-2015 гг.) установлено, что положительные результаты анастомотической уретропластики без пересечения спонгиозного тела (90-100%) [5, 6, 7, 8] вполне сопоставимы с результатами стандартной методики анастомотической уретропластики (90,8 – 98,8%) [1, 2, 8] и значительно превышает результаты внутренней оптической уретротомии (8 – 42%) [9, 10].
Преимуществами новой анастомотической методики без пересечения спонгиозного тела над стандартной операцией Хольцова могут считаться следующие:
1. простота и небольшое время, необходимое для выполнения операции, т.к. не требуется выделения уретры по вентральной поверхности в области бульбарных артерий, что упрощает операцию. При коротких стриктурах (< 0,5 см) стриктуропластику, т.е. иссечение рубцовоизмененной слизистой можно не производить, что значимо укорачивает время операции и делает ее простой;
2. более быстрое заживление и, следовательно, более короткий срок дренирования мочевого пузыря уретральным катетером. Безусловно, это возможно только при правильном выполнении техники и контроле герметичности шва уретры в конце операции. С приобретением хирургом оперативного опыта, уретральный катетер можно будет удалять в течение первых трех-пяти дней, что значительно снизит риски инфекционных осложнений и затраты на лечение больного. Учитывая высокую эффективность операции по сравнению с внутренней оптической уретротомией и отсутствием необходимости повторять эндоскопические вмешательства общая стоимость лечения будет достоверно ниже;
3. сохранение антеградного кровотока по спонгиозному телу в зоне операции и дистальнее. Нарушение последнего может значимо и не влиять на частоту рецидива, особенно при хорошо выраженном ретроградном кровоснабжении уретры, но, вероятно, обуславливает развитие сексуальных нарушений в виде снижения кровенаполнения и чувства холода головки полового члена. Это может негативно сказываться на качестве сексуальной функции и жизни молодых сексуально активных пациентов. Подобные осложнения после стандартной операции по иссечению и прямому анастомозу при коротких стриктурах бульбозного отдела уретры могут достигать 23% [11].
ВЫВОДЫ
Новая методика анастомотической уретропластики без пересечения спонгиозного тела является малоинвазивной, простой, высокоэффективной, с коротким периодом послеоперационного дренирования мочевого пузыря, не нарушающая кровотока по спонгиозному телу.
Данная методика может служить альтернативой существующему «золотому стандарту» – анастомотической уретропластике у пациентов с короткими стриктурами бульбозного отдела уретры, за исключением стриктур посттравматического генеза, и вполне может заменить внутреннюю оптическую уретротомию в качестве первого варианта оперативного лечения у пациентов с протяженностью стриктуры менее 1 см.
ЛИТЕРАТУРА
1. Коган М.И., Красулин В.В., Митусов В.В., Шангичев А.В., Глухов В.П., Наранов С.В. Оперативное лечение стриктур и облитераций уретры. // Урология. 2015. N 2. C. 17-23.
2. Morey AF, Watkin N, Shenfeld O, Eltahawy E, Giudice C. SIU/ICUD Consultation on Urethral Strictures: Anterior urethra-primary anastomosis. // Urology. 2014. Vol. 83, Suppl.3. P. 23-26.
3. Andrich DE, Dunglison N, Greenwell TJ, Mundy AR. The long-term results of urethroplasty. // J Urol. 2003. Vol. 170, N 1. P. 90
4. Andrich DE, Mundy AR. Non-transecting anastomotic bulbar urethroplasty: a preliminary report. // BJU Int. 2012. Vol. 109, N 7. P. 1090-1094
5. Lumen N, Hoebeke P, Oosterlinck W. Ventral longitudinal stricturotomy and transversal closure: the Heineke-Mikulicz principle in urethroplasty. // Urology. 2010. Vol. 76, N 6. P. 1478-1482.
6. Jordan GH, Eltahawy EA, Virasoro R. The technique of vessel sparing excision and primary anastomosis for proximal bulbous urethral reconstruction. // J Urol. 2007. Vol. 177, N 5. P. 1799 – 1802.
7. Virasoro R, Zuckerman JM, McCammon KA, DeLong JM, Tonkin JB, Capiel L, Rovegno AR, Favre G, Giudice CR, Eltahawy EA, Gur U, Jordan GH. International multi-institutional experience with the vessel-sparing technique to reconstruct the proximal bulbar urethra: mid-term results. // World J Urol. 2015. Feb 18.
8. Глухов В.П. Резекция уретры с концевым анастомозом при осложненных структурах и облитерациях уретры у мужчин: Дисс. ...канд. мед. наук. РнД., 2010. 116с
9. Santucci R, Eisenberg L. Urethrotomy has much lower success rate than previously reported. // J Urol. 2010. Vol. 183, N 5. P. 1859-1862.
10. Pansadoro V, Emiliozzi P. Internal urethrotomy in the management of anterior urethral strictures: long-term followup. // J Urol. 1996. Vol. 156, N 1. P. 73–75.
11. Barbagli G, De Angelis M, Romano G, Lazzeri M: Long-term follow up of bulbar end-to-end anastomosis: a retrospective analysis of 153 patients in a single center experience. // J Urol. 2007. Vol. 178, N 6. P. 2470–2473.









Комментарии