Б.Г. Гулиев1,2, Б.К. Комяков2, Ж.П. Авазханов1,2
- 1 Кафедра урологии Северо-Западного государственного медицинского университет имени И.И. Мечникова, Санкт-Петербург, Россия
- 2 Центр урологии с робот-ассистированной хирургией Мариинской больницы, Санкт-Петербург, Россия
Хирургическое лечение протяженных стриктур мочеточника остается сложной проблемой в урологии [1]. При их локализации в тазовом отделе применяются такие хорошо апробированные операции, как уретероцистоанастомоз по Боари или Psoas hitch. Эти вмешательства активно выполняются, что связана с высокой частотой повреждения нижней трети мочеточника при хирургических, гинекологических и эндоурологических операциях [2]. Протяженные стриктуры проксимального отдела мочеточника отмечаются не так часто. В основном они бывают рецидивными и встречаются после эндоурологических и пластических операций на лоханочно-мочеточниковом сегменте (ЛМС) и верхней трети мочеточника. В этих случаях используются такие вмешательства, как мобилизация почки с низведением, операция Yang-Monti, тонкокишечная тубулярная пластика, замещение мочеточника червеобразным отростком [1,3].
Низведение почки позволяет заместить дефект мочеточника длиной около 4 см [4,5]. Однако рубцовые изменения паранефральной клетчатки после предыдущих вмешательств не всегда позволяют мобилизовать почку. Пластика тубулярным и реконфигурированным кишечным сегментом требует резекцию тонкой кишки с межкишечным анастомозом и выполнение дистального и проксимального анастомозов. Однако при илеоуретеропластике существуют различные хирургические и метаболические осложнения [3,6]. Поэтому продолжается поиск новых альтернативных методов реконструкции проксимального отдела мочеточника. В настоящее время среди них наиболее привлекательным является уретеропластика буккальным лоскутом [7–12].
МАТЕРИАЛЫ И МЕТОДЫ
Поиск проводился в следующих базах данных: Embase, Medline, Google Scholar, Scopus в период с 2010 по 2019 годы. Ключевыми словами для поиска были: ureter stricture, buccal ureteroplasty. Критериями включения были оригинальные статьи, описывающие результаты экспериментальных и клинических работ по пластике мочеточника лоскутом из слизистой щеки. В итоге было отобрано 94 статьи, из которых после изучения абстрактов в обзор вошли результаты 14 публикаций, удовлетворяющих критериям включения.
РЕЗУЛЬТАТЫ
В настоящее время слизистая щеки широко используется при пластике уретры [13–15]. Буккальный лоскут хорошо подходит для замещения мочевых путей, так как он легко доступен и трансплантат минимально подвержен к отторжению [13,16,17]. Он не имеет волосяных фолликул, резистентен к инфекции и устойчив во влажной среде [18]. Благодаря прочной собственной подслизистой пластинке, легко происходит сращение с мочеточником [13]. При уретеропластике лоскутом из слизистой щеки диссекция мочеточника проводится только в области сужения, что минимизирует нарушение кровоснабжения. Также в зависимости от протяженности дефекта мочеточника можно выкроить лоскут адекватной длины для обеспечения анастомоза без натяжения.
Первые экспериментальные работы по буккальной уретеропластике проводились еще в 1983 году [19]. У трех бабуинов вначале резецировали среднюю треть мочеточника на протяжении 3 см. Затем из лоскута слизистой щеки размером 3х2 см создавали трубку и замещали этот участок. Далее его окутывали сальником для дальнейшей васкуляризации. Урограммы через 8 и 10 недель демонстрировали хорошую проходимость лоскута с отсутствием данных за стриктуру. При патоморфологических исследованиях реконструированных мочеточников кровоснабжение лоскута было хорошим, признаков выраженной воспалительной инфильтрации или фиброзных изменений не было [20, 21]. Результаты этой работы были встречены урологами с вопросами относительно проходимости лоскута и его долговечности. Противники данного метода указывали, что реконструированный мочеточник с адинамическим участком из слизистой щеки может привести к нарушению уродинамики верхних мочевых путей (ВМП), так как в этой зоне будет отсутствует перистальтика, генерируемая гладкомышечными волокнами мочеточника [19,21]. Вопросы были также относительно приживляемости из-за недостаточного кровоснабжения стенки мочеточника, в особенности после неоднократных операций на нем. В связи с этим задача первоначальных работ по буккальной пластике заключалась в том, чтобы ответить на эти вопросы.
Удовлетворительные результаты экспериментальных работ на животных воодушевили J.H. Naude выполнить уретеропластику слизистой щеки у 6 пациентов. У 4 из них операция производилась по методике onlay, когда суженный участок мочеточника рассекали и пришивали буккальный лоскут. У 1 пациента выполнена аугментационная анастомотическая onlay буккальная уретеропластика. После резекции пораженного участка мочеточника анастомозировали близкие края здорового мочеточника, а остальную часть восстанавливали буккальным графтом. Один пациент подвергнут замещению мочеточника тубулярным лоскутом из слизистой щеки. Во всех случаях реконструированный мочеточник окутывался сальником. Эффективность операций оценивалась с помощью антеградной или ретроградной уретеропиелографии и экскреторной урографии. У всех пациентов наблюдалась умеренная дилатация в зоне вмешательства, но проходимость ВМП была адекватной. За средний период наблюдения 24 мес. (2 – 72 мес) не было рецидива сужения и дополнительные вмешательства не проводились [22]. Таким образом результаты экспериментальной и первых клинических работ позволили сделать заключение о том, что атоничность мочеточника не препятствует оттоку мочи, а окутывание реконструированного мочеточника сальником на ножке может помочь в васкуляризации.
Удовлетворительные результаты первоначальных работ привели к увеличению количества сторонников буккальной пластики мочеточника. Нарастающий опыт и усовершенствование техники позволили уточнить показания к этой операции [7, 20, 22]. Она, несомненно, является методом выбора при невозможности создания анастомоза «конец в конец» без натяжения. D. Kroepfl и соавт. у 6 пациентов со стриктурами средней и дистальной части мочеточника, не позволяющими выполнить уретеро-уретероанастомоз, провели уретеропластику по методике onlay (один пациент имели билатеральные стриктуры обоих мочеточников). Реконструированные мочеточники также были окутаны сальником. Средняя длина стриктуры была 7 см (3 – 11 см). За средний период наблюдения 18 мес (10 – 85 мес) у 5 (71,4%) больных обструкции ВМП не было. Двум пациентам с рецидивом стриктуры (через 17 и 30 мес) произведена пункционная нефростомия [23].
A.A. Badawy и соавт. 5 пациентам со сужениями проксимальной и средней трети мочеточника выполнили тубулярную буккальную уретеропластику. При резекции пораженного сегмента мочеточника его адвентицию оставили не тронутой, чтобы ее можно было использовать для дополнительной васкуляризации графта. Также все оперированные мочеточники были окутаны сальником. Средняя длина стриктуры составила 4,5 см (3,5 – 5 см). Хирургический успех регулярно оценивался с помощью ультразвукового исследования почек и экскреторной урографии. За период наблюдения 18 мес. (14 – 26 мес) у всех пациентов получена адекватная проходимость на урограммах [24]. O. Fahmy и соавт. замещали дефект проксимального участка мочеточника длиной 6 см. Перинефральный жир использовали для окутывания лоскута. За 9 месячный период наблюдения не было признаков рецидива стриктуры по данным ультразвукового исследования и сканирования почек [25]. Несмотря на ее обнадеживающие результаты тубулярной уретеропластики слизистой щеки, сообщаемые в литературе имеются разногласия по использованию этой техники, не всегда дающей хорошие результаты [24,25]. Так оnlay уретеропластика слизистой щеки ассоциируется с 11%, а тубулярная уретеропластика с 45% рецидивом сужения мочеточника, что связано с недостаточной васкуляризацей лоскута [26,27]. Однако не следует полностью отказываться от нее и в дальнейшем необходимо проведение работ, сравнивающих результаты тубулярной и onlay буккальной уретеропластики.
Некоторые авторы утверждают, что буккальная уретеропластика может быть более предпочтительной для замещения длинных мочеточниковых стриктур по сравнению с такими традиционными техниками, как илеоуретеропластика и аутотрансплантация почки, которые являются технически сложными и приводят к значительным осложнениям [8,9,23,24]. Забор лоскута слизистой щеки для урологической реконструкции ассоциируется с низкой морбидностью. M.R. Markiewic и соавт. анализировал результаты 27 работ, по данным которых наблюдались 4,0% осложнений [16]. В то время как замещение тонкой кишкой включает ее резекцию с реконструкцией и может ассоциироваться с кишечной непроходимостью, метаболическими нарушениями, инфекцией мочевых путей [28,29]. Аутотрансплантация почки требует достаточных технических навыков в трансплантации и после нее наблюдаются псевдоаневризмы и тромбоз почечной артерии [30-32]. Однако в опытных руках и с определенным отбором больных, обе операции (кишечная пластика и аутотрансплантация) ассоциируются с хорошими отдаленными результатами [30,33]. J.D. Roth и соавт. кишечную пластику выполнили 108 пациентам и отмечали невысокий процент осложнений по Клавьен >2 ст. (11,1%) и только у 3,7% развился гиперхлоремический метаболический ацидоз [33]. N.G Cowan. и соавт. выполнили 54 аутотрансплантации у 51 пациента, число ранних послеоперационных осложнений (>2 ст.) было 14,8% и у только 3,7% наблюдали отторжение трансплантированной почки и 1,9% развилась аневризма почечной артерии, потребовавшей выполнения нефрэктомии [30]. Однако илеоуретеропластику и аутотрансплантацию почки можно использовать для восстановления дефектов мочеточника, охватывающих ее большую или всю часть. Использование слизистой щеки для реконструкции таких стриктур является неправильным [8,9]. Кроме того, имеется ограниченная возможность выкраивания нескольких лоскутов, доступных для замещения тотальных стриктур мочеточника.
В литературе имеются лимитированные данные относительно эффективности буккальной пластики более протяженных сужениях мочеточника. D. Kroepfl и соавт. выполнили подобную операцию у пациента с мочеточниковой стриктурой длиной 11 см. Спустя 40 мес. после операции рецидива сужения не было [23]. Дальнейшие исследования необходимы для определения лимита уретеропластики относительно протяженности сужения и сравнения полученных результатов с таковыми при илеоуретеропластике и аутотрансплантации почки.
Буккальная уретеропластика является относительно показана пациентам с рецидивными стриктурами мочеточников [8,23,34]. Реконструкция мочеточника в зоне сужения представляется сложной ввиду рубцовых изменений в зоне диссекции и плохой васкуляризации мочеточника [8,35]. M. Etafy и соавт. провели ретроспективный анализ всех робот-ассистированных пиелопластик и отметили 83% успех при первичных и 70% при вторичных сужениях пиелоуретрального сегмента (ПУС) [36]. Буккальная уретеропластика считается хорошей опцией при рецидивных стриктурах, так как нет необходимости уретеролиза на большом протяжении, который минимизирует нарушение кровоснабжения мочеточника. При буккальной уретеропластике нужно выполнить диссекцию только суженного участка мочеточника для инцизии. У пациентов с частичной или полной облитерацией просвета измененную зону можно резецировать и выполнить аугментационную анастомотическую буккальную пластику [8].
В сообщении A. Pandey и соавт. два пациента из трех ранее были подвергнуты неуспешной пиелопластике и имели рецидивные мочеточниковые стриктуры. Один больной имел стриктуру длиной 6 см, и другой – 7 см. Хирургический успех оценивался с помощью экскреторной урографии. Оба пациента перенесли успешную буккальную оnlay уретеропластику и не было рецидива стриктуры за период наблюдения в 50 и 34 мес. [34]. Недавние сообщения касательно буккальной уретеропластики были не только фокусированы на оценке результатов, но и также направлены на усовершенствование хирургической техники. За последние годы появились работы по робот-ассистированной буккальной уретеропластике с хорошими результатами [8,9,37-39]. Роботическая система Да Винчи все чаще используется для реконструкции мочеточника, обеспечивая преимущества минимально инвазивной хирургии [7]. При этих операциях степень васкуляризации мочеточника можно оценить с помощью околоинфракрасной флуоресцентной визуализации (ИФВ) [40-42], которая доступна для Да Винчи Si и Xi.
В 2015 году в первом сообщении по роботической буккальной уретеропластике L.C. Zhao и соавт. описали технику операции у 4 пациентов с проксимальными мочеточниковыми стриктурами, средняя длина которых была 4 см (1,5–6 см). Проксимальные и дистальные края суженного участка определяли комбинацией гибкой уретероскопии с ИФВ. При невозможности проведения гибкого уретероскопа из-за облитерации мочеточника внутривенно вводился индоцианин зеленый. Под ИФВ хорошо – перфузируемая ткань мочеточника окрашивалась в зеленый цвет, а суженный участок оставался темным. 3 пациента подвергнуты onlay и один аугментационной анастомотической буккальной уретеропластике. У одного пациента зона операции была окутана перинефральным жиром, а у других – сальником. Эффективность оценивалась с помощью УЗИ и реносканирования. При среднем наблюдении 15,5 мес (10.7 – 18,6 мес.) данных за рецидив не получено [9]. S. Arora и соавт. аналогично использовали гибкую уретероскопию и ИФВ для определения дистального края стриктуры длиной 6 см у пациента, который ранее был подвергнут неуспешному робот-ассистированному уретеролизу. Реконструированный мочеточник был окутан сальником. За период наблюдения 6 мес. по данным сканирования почек рецидива сужения не было [37].
Таблица 1. Результаты буккальной пластики протяженных сужений мочеточника
Table 1. Results of buccal ureteroplasty of extented ureteral strictures
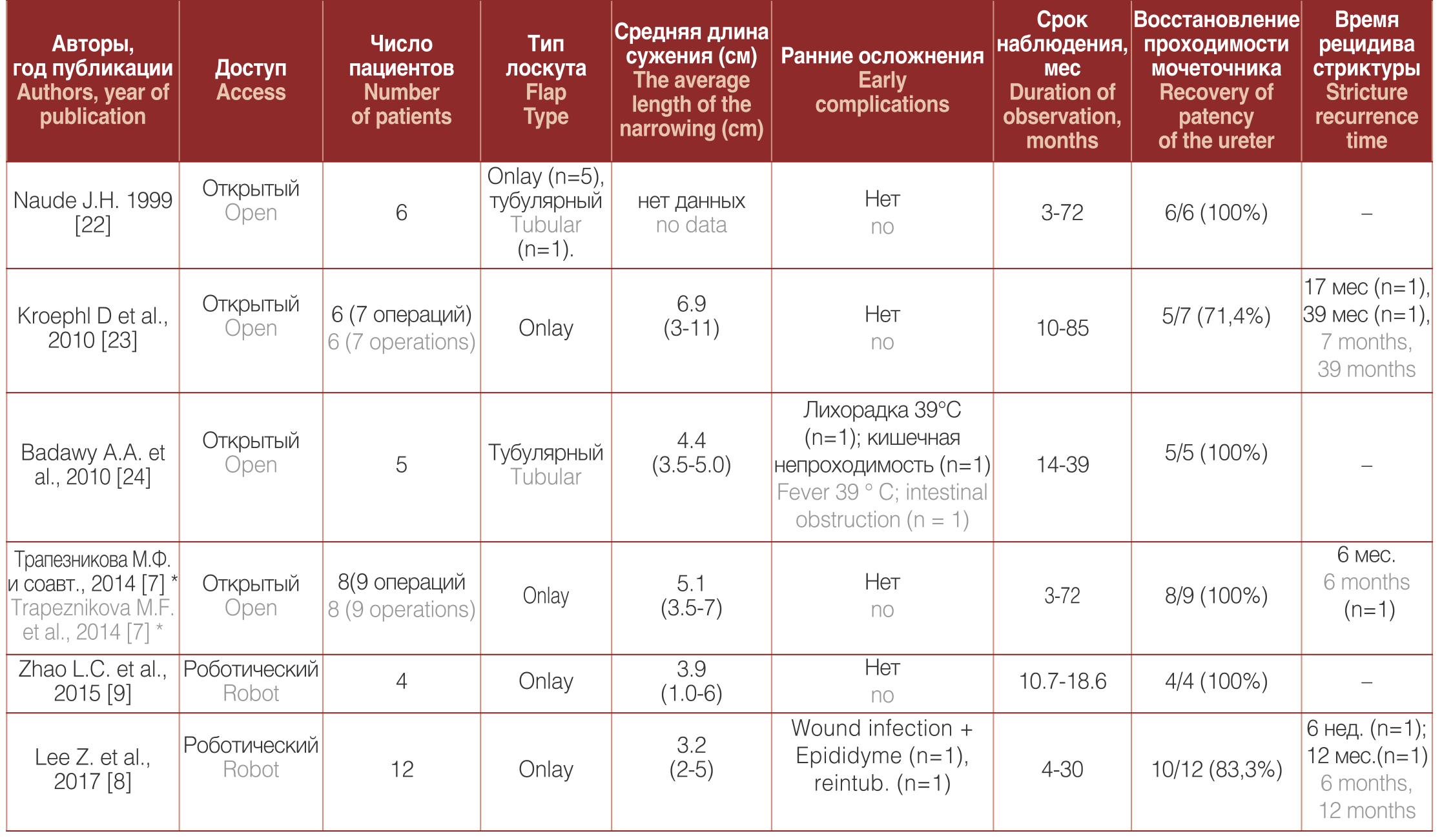
* Поздние осложнения: Лигатурный камень мочеточника (n=1). Вторично-сморщенная почка (n=1). *Late complications: Ligature ureteral stone (n = 1). Secondarily shriveled kidney (n = 1).
В широкой серии Z. Lee и соавт. описали робот-ассистированную уретеропластику у 12 пациентов с стриктурами проксимального и среднего отдела мочеточника Из них у 8 ранее выполнялась пластика мочеточника. Средняя длина мочеточника была 3 см (2–5 см). Проксимальные и дистальные края стриктуры определяли также с помощью ИФВ. Во всех случаях оперированный участок мочеточника окутывался сальником. Хирургический успех оценивался использованием ретроградной пиелографии, реносцинтиграфии, компьютерной томографии и наличия симптомов. При среднем сроке наблюдения 13 мес. результаты операции у 10 (83,3%) больных были клинически и радиологически успешными [8].
В мировой литературе имеется единственное наблюдение лапароскопической буккальной уретеропластики. Данная операция была проведена 42-летнему мужчине с ятрогенной (после контактной уретеролитотрипсии) стриктурой верхней трети мочеточника длиной 3 см, включая 1 см облитерированного участка [43].
Данные авторов с опытом буккальной пластики мочеточника более 4-5 больных приведены в таблице 1 Необходимо отметить, что большинство работ по буккальной уретропластике являются моно-институтскими с небольшой серией клинических случаев с короткими и средними периодами наблюдения. Оценка эффективности операций и количества осложнений является сложной для изучения из-за небольшого числа этих больных. Поэтому для решения этого вопроса необходимо совместные работы урологов из различных клиник.
ЗАКЛЮЧЕНИЕ
Буккальная уретеропластика может быть методом выбора у больных с протяженными сужениями проксимального отдела мочеточника, когда выполнение уретероуретероанастамоза и использование сегмента тонкой кишки технически невозможны. Данное вмешательство является привлекательным ввиду несложности выкраивания лоскута достаточной длины, отсутствия необходимости широкой мобилизации мочеточника, замещения суженного участка и высокой эффективности. Недостатком буккальной пластики мочеточника является ограниченный опыт единичных клиник, который, возможно, связан с небольшим количеством больных со стриктурами верхней трети мочеточника и негативным отношением большинства урологов к этой операции.
ЛИТЕРАТУРА
- Комяков Б.К., Гулиев Б.Г. Хирургия протяженных сужений мочеточников. СПб.: Невский диалект, 2005 257 с. [Komyakov B.K., Guliev B.G. Surgery of extended ureteral stricturess. SPb.: Nevskij dialect, 2005 257 s. (In Russian)]
- Wenske S, Olsson CA, Benson MC. Outcomes of distal ureteral reconstruction through reimplantation with psoas hitch, Boari flap, or ureteroneocystostomy for benign or malignant ureteral obstruction or injury. Urology 2013;82(1):231–236. doi: 10.1016/j.urology.2013.05.033.
- Комяков Б.К., Гулиев Б.Г., Очеленко В.А. Технические особенности кишечной пластики мочеточников. Часть 3: Лапароскопическая илеои аппендикулярная уретеропластика. Урология 2016;(4): 4 – 9 [Komyakov B.K., Guliev B.G., Ochelenko V.A. Technical features of intestinal plastics of the ureters. Part 3: Laparoscopic ileoand appendicular ureteroplasty. Urologiya=Urology 2016; (4): 4 9 (In Russian)]
- Lee Z, Llukani E, Reilly CE, Mydlo JH, Lee DI, Eun DD. Single surgeon experience with robot-assisted ureteroureterostomy for pathologies at the proximal, middle, and distal ureter in adults. J Endourol 2013;27(8):994–999. doi: 10.1089/end.2013.0075.
- Hofer MD, Aguilar-Cruz HJ, Singla N, Cordon BH, Scott JM, Morey AF. Expanding applications of renal mobilization and down ward nephropexy in ureteral reconstruction. Urology 2016;94: 232–236. doi: 10.1016/j.urology.2016.04.008.
- Ghosh B, Jain P, Pal DK. Managing mid and lower ureteral benign strictures: the laparoscopic way. J Laparoendosc Adv Surg Tech A 2018;28(1):25–32. doi: 10.1089/lap.2017.0256.
- Трапезникова М.Ф., Базаев В.В., Шибаев А.Н., и соавт. Заместительная пластика протяженных стриктур мочеточника аутотрансплантатом буккальной слизистой. Урология 2014;(2):16–19. [Trapeznikova M.F., Bazaev V.V., Shibaev A.N., Zamestitel’naya plastika protyazhennyh strictur mochetochnika autotransplantatom bukkal’noy slizistoj. Urologiya=Urology 2014;(2):16–19 (In Russian)]
- Lee Z, Waldorf BT, Cho EY, Liu JC, Metro MJ, Eun DD. Robotic ureteroplasty with buccal mucosa graft for the management of complex ureteral strictures. J Urol 2017;198(6):1430–1435. doi: 10.1016/j.juro.2017.06.097.
- Zhao LC, Yamaguchi Y, Bryk DJ, Adelstein SA, Stifelman MD. Robot-assisted ureteral reconstruction using buccal mucosa. Urology 2015;86(3):634–638. doi: 10.1016/j.urology.2015.06.006.
- Катибов М.И., Поляков Н.В., Кешишев Н.Г. и соавт. Использование буккального графта при стриктурах мочеточника. Урология 2018;(1):138-142. doi: https://dx.doi.org/10.18565/urology.2018.1.138-142 [Katibov M.I., Polyakov N.V., Keshishev N.G. et al. The use of buccal graft for ureteral strictures. Urologiya=Urology 2018; (1): 138-142. doi: https://dx.doi.org/10.18565/urology.2018.1.138-142 (In Russian)]
- Lee Z, Keehn AY, Sterling ME. A review of buccal mucosa graft ureteroplasty. Curr Urol Rep 2018; 19(4): 23 doi: 10.1007/s11934-018-0772-5
- Del Pozo Jiménez G. Castillón-Vela I, Carballido Rodríguez J. Buccal mucosa graft for the treatment of long ureteral stenosis: Bibliographic review. Arch Esp Urol 2017;70(4):445–453.
- Bhargava S, Chapple CR. Buccal mucosal urethroplasty: is it the new gold standard? BJU Int 2004;93(9):1191–1193. doi: 10.1111/j.1464-410X.2003.04860.x
- Patterson JM, Chapple CR. Surgical techniques in substitution urethroplasty using buccal mucosa for the treatment of anterior urethral strictures. Eur Urol 2008;53(6):1162–1171. doi: 10.1016/eururo.2007.10.011
- Hudak SJ, Lubarn JD, Kulkarni S, Morey AF. Single-stage reconstruction of complex anterior urethral strictures using overlapping dorsal and ventral buccal mucosal grafts. BJU Int 2012;110(4):592–596. doi: 10.1111/j.1464-410X.2011.10787.x
- Markiewicz MR, DeSantis JL, Margarone JE, Pogrel MA, Chuang SK. Morbidity associated with oral mucosa harvest for urological reconstruction: an overview. J Oral Maxillofac. Surg 2008;66(4):739–744. doi: 10.1016/j.joms.2007.11.023
- Bryk DJ, Yamaguchi Y, Zhao LC. Tissue transfer techniques in reconstructive urology. Korean J Urol 2015;56(7):478–486. doi: 10.4111/kju.2015.56.7.478
- Barbagli G. Lazzeri M. Urethral reconstruction. Curr Opin Urol 2006;16(6):391–395. doi: 10.1097/01.mou.0000250277.44990.ab
- Naude JH. The natural history of ureteric bilharzia. Br J Urol 1984;56(6):599–601. doi: 10.1111/j.1464-410x.1984.tb06125.x
- Somerville JJ, Naude JH. Segmental ureteric replacement: an animal study using a free non-pedicled graft. Urol Res 1984;12(2):115–119. doi: 10.1007/bf00257176
- Powell SJ, Engelbrecht HE, Welchman JM. Hydronephrosis and urinary tract bilharziasis. A radiological and necropsy survey. Trans Royal Soc Trop 1968;62(2):231–237. doi: 10.1016/0035-9203(68)90162-4
- Naude JH. Buccal mucosal grafts in the treatment of ureteric lesions. BJU Int 1999; 83(7):751–754. doi: 10.1046/j.1464-410x.1999.00019.x
- Kroepfl D, Loewen H, Klevecka V, Musch M. Treatment of long ureteric strictures with buccal mucosal grafts. BJU Int 2010;105(10):1452–1455. doi: 10.1111/j.1464-410X.2009.08994.x
- Badawy AA, Abolyosr A, Saleem M.M Abuzeid AM. Buccal mucosa graft for ureteral stricture substitution: initial experience. Urology 2010;76(4):971–975. doi: 10.1016/j.urology.2010.03.095.
- Fahmy O, Schubert T, Khairul-Asri MG, Stenzl A, Gakis G. Total proximal ureter substitution using buccal mucosa. Int J Urol 2017;24(4):320–323. doi: 10.1111/iju.13307
- Andrich DE, Mundy AR. Substitution urethroplasty with buccal mucosal-free grafts. J Urol 2001;165(4):1131–1133. doi: 10.1016/S0022-5347(05)66447-6
- Patterson JM, Chapple CR. Surgical techniques in substitution urethroplasty using buccal mucosa for the treatment of anterior urethral strictures. Eur Urol 2008;53(6):1162–1171. doi: 10.1016/j.eururo.2007.10.011
- Armatys SA, Mellon MJ, Beck SD, Koch MO, Foster RS, Bihrle R. Use of ileum as ureteral replacement in urological reconstruction. J Urol 2009;181(1):177–181. doi: 10.1016/j.juro.2008.09.019
- Chung BI, Hamawy KJ, Zinman LN, Libertino JA. The use of bowel for ureteral replacement for complex ureteral reconstruction: long-term results. J Urol 2006; 175(1):179–183. doi: 10.1016/S0022-5347(05)00061-3
- Cowan NG, Banerji JS, Johnston RB, Duty BD, Bakken B, Hedges JC. Renal autotransplantation: 27-year experience at 2 institutions. J Urol 2015;194(5):1357–1361. doi: 10.1016/j.juro.2015.05.088
- Eisenberg ML, Lee KL, Zumrutbas AE, Meng MV, Freise CE, Stoller ML. Long-term outcomes and late complications of laparoscopic nephrectomy with renal autotransplantation. J Urol 2008;179(1):240–243. doi: 10.1016/ j.juro.2007.08.135
- Tran G, Ramaswamy K. Chi T, Meng M. Freise C, Stoller ML. Laparoscopic nephrectomy with autotransplantation: safety, efficacy and long-term durability. J Urol 2015;194(3):738–743. doi: 10.1016/j.juro.2015.03.089
- Roth JD, Monn MF, Szymanski KM, Bihrle R, Mellon MJ. Ureteral reconstruction with ileum: long-term follow-up of renal function. Urology 2017;104:225–229. doi: 10.1016/j.urology.2017.02.026
- Pandey A, Dican R, Beier J, Keller H. Buccal mucosal graft in reconstructive urology: uses beyond urethral stricture. Int J Urol 2014;21(7):732–734. doi: 10.1111/iju.12403
- Ambani SN, Yang DY, Wolf JS Jr. Matched comparison of primary versus salvage laparoscopic pyeloplasty. World J Urol 2017;35(6):951–956. doi: 10.1007/s00345-016-1951-y
- Etafy M, Pick D, Said S, Hsueh T, Kerbl D, Mucksavage P, et al. Robotic pyeloplasty: the University of California-Irvine experience. J Urol 2011;185(6):2196–2200. doi: 10.1016/j.juro.2011.02.054
- Arora S, Campbell L, Tourojman M, Pucheril D, Jones LR, Rogers C. Robotic buccal mucosal graft ureteroplasty for complex ureteral stricture. Urology 2017;110:257–258. doi: 10.1016/j.urology.2017.06.037
- Zampini AM, Nelson R. Zhang JJ, Reese J, Angermeier KW, Haber GP. Robotic salvage pyeloplasty with buccal mucosal onlay graft: video demonstration of technique and outcomes. Urology 2017;110: 253–256. doi: 10.1016/ j.urology.2017.07.023
- Ganpule AP, Singh AG, Islam MR, Sonawane P, Sabnis RB, Desai MR. Robotic buccal mucosa graft ureteroplasty (inlay and onlay) for upper ureteric stricture: Point of technique. J Minim Access Surg 2018;14(4): 357–361. doi: 10.4103/jmas.JMAS_188_17
- Bjurlin MA, Gan M, McClintock TR, Volpe A, Borofsky MS, Montrie A, Stifelman MD. Near-infrared fluorescence imaging: emerging applications in robotic upper urinary tract surgery. Eur Urol 2014;65(4):793–801. doi: 10.1016/j.eururo.2013.09.023
- Hockenberry MS, Smith ZL, Mucksavage P. A novel use of near-infrared fluorescence imaging during robotic surgery without contrast agents. J Endourol 2014;28(5):509–512. doi: 10.1089/end.2013.0606
- Lee Z, Moore B, Giusto L, Eun DD. Use of indocyanine green during robotassisted ureteral reconstructions Eur Urol 2015;67(2):291–298. doi: 10.1016/ j.eururo.2014.08.057
- Li B, Xu Y, Hai B, Liu B, Xiang Y, Hua X, Hou T. Laparoscopic onlay lingual mucosal graft ureteroplasty for proximal ureteral stricture: initial experience and 9-month follow-up. Int Urol Nephrol 2016;48(8):1275–1279. doi: 10.1007/ s11255-016-289-9.
Статья опубликована в журнале "Экспериментальная и клиническая урология" №4 2019, стр. 86-91









Комментарии