Е.А. Ефремов, М.Н. Коршунов, О.В. Золотухин, Ю.Ю. Мадыкин, С.С. Красняк
Всемирная организация здравоохранения (ВОЗ) определяет бесплодие как «неспособность достичь клинической беременности через 12 месяцев или более при регулярной незащищенной половой жизни» [1]. Уровни бесплодия в 2010 году были аналогичны уровням 1990 года в большинстве стран мира, кроме снижения этого показателя в странах Африки к югу от Сахары и в Южной Азии [2]. Пара, которая безуспешно пыталась зачать год или больше, считается субфертильной или менее фертильной, чем типичная здоровая пара [3].
От 40 до 50% случаев бесплодия обусловлены женским фактором. Они включают: овуляторную недостаточность, повреждение фаллопиевых труб, эндометриоз, эндокринные нарушения, инфекционно-воспалительные заболевания органов малого таза, низкое качество яйцеклеток – как вариант овуляторной недостаточности и необъяснимую субфертильность. Считается, что в мире до 25% пар, которые пытаются зачать ребенка, испытывают трудности с деторождением [4,5]. Чтобы преодолеть проблемы с фертильностью, многие пары прибегают к лечению методами вспомогательных репродуктивных технологий (ВРТ). К ним относятся индукция овуляции, внутриматочная инсеминация спермой мужа или донора (ИОСМ/ИОСД), экстракорпоральное оплодотворение (ЭКО) и интрацитоплазматическая инъекция сперматозоида (ИКСИ).
Как женщины, так и мужчины нередко используют антиоксидантные добавки для подготовки к процедурам ВРТ и/или одновременно с лечением иными средствами, а некоторые пары используют только антиоксиданты без применения ВРТ в попытке улучшить свою фертильность. Антиоксиданты – это биологические и химические соединения, которые уменьшают окислительный стресс (дисбаланс между образованием активных форм кислорода и способностью организма к детоксикации). Они представляют собой группу органических нутриентов, которые включают витамины, минералы, активные ингредиенты растительного происхождения, и используются в виде моноили комбинированной терапии. Исчерпывающий мета-анализ показал, что применение антиоксидантов при бесплодии более чем в 2 раза повышает вероятность зачатия [6].
Цинк является мощным антиоксидантным средством и основным компонентом системы антиоксидантной защиты организма, состоящей из активных ферментов, таких, как супероксиддисмутаза, каталаза. Кроме того, цинк в качестве катализатора может предотвращать перекисное окисление липидов путем перемещения или переноса металлов, включая железо и медь [7].
В одном из исследований подопытные, получавшие диету с дефицитом цинка, демонстрировали снижение потенциала антиоксидантной защиты и одновременное увеличение перекисного окисления липидов в ткани яичка [8]. Нужно отметить, что у мужчин цинк играет важную роль в регуляции сывороточного уровня тестостерона [9].
L-карнитин – витаминоподобное вещество, которое повышает уровень клеточной энергии в митохондриях, защищает мембраны клеток и структуру ДНК от индуцированного активными формами кислорода апоптоза [10,11]. L-карнитин присуствует в придатке яичка и семенной плазме, обусловливая поддержку подвижности сперматозоидов и их дозревания [12].
Астаксантин – еще один мощнейший антиоксидант – Астаксантин – каротиноид, имеющий по сравнению с бета-каротином два дополнительных атома кислорода на каждом из шестичленных колец. Астаксантин является наиболее мощным из всех известных антиоксидантов. Его сила как антиоксиданта в 75 раз больше, чем у альфа-липоевой кислоты, приблизительно в 550 раз больше, чем у катехинов зеленого чая и витамина Е, в 800 раз больше, чем у коэнзима Q10, и приблизительно в 6000 раз больше, чем витамина С [13]. Кроме того, последние исследования также показали, что астаксантин восстанавливает стероидогенез в клетках Лейдига за счет снижения образования активных форм кислорода. В группе терапии достоверно повышается и длительно поддерживается уровень прогестерона и тестостерона [14].
Мака перуанская (Lepidium meyenii, Клоповник Мейена) представляет собой травянистое двухлетнее растение семейства крестоцветных, произрастающее в высокогорных районах Анд в Перу. В дополнение к сахарам и белкам корень Маки содержит уридин, глюкозинолаты, яблочную кислоту и ее бензоильные производные, также содержит глюкотропеолин и м-метокси глюкотропеолин [15]. Метаноловый экстракт корня маки также содержит (1R, 3S)1-метил-тетрагидро-карболин-3-карбоновую кислоту – молекула, которая, оказывает множество воздействий на центральную нервную систему [16]. Мака содержит химическое вещество под названием p-метоксибензилизотиоцианат, который, по общему мнению, обладает свойствами афродизиака. Многие из активных компонентов Маки перуанской могут быть разрушены или инактивированы кислым содержимым желудка, поэтому лекарственная форма в виде кишечно-растворимой капсулы позволяет доставить все действующие вещества в кишечник, исключая воздействие желудочного сока. Экстракт Маки перуанской показал способность увеличивать выработку фолликулостимулирующего гормона в гипофизе, что позволяет активизировать клетки Сертоли в яичках [17]. Кроме того, водно-спиртовой экстракт Маки увеличивает уровень тестостерона путем активизации клеток Лейдига [18]. Также было доказано, что применением Маки позволяет улучшить подвижность сперматозоидов и их концентрацию, как в экспериментальных, так и клинических исследованиях [19,20].
МАТЕРИАЛЫ И МЕТОДЫ
Проведена мультицентровая оценка эффективности и безопасности применения биологически активной добавки к пище (БАД) «Мираксант»® умужчин с идиопатическим бесплодием. Целью исследования было оценить динамику параметров спермограммы (концентрация, подвижность, морфология, жизнеспособность) и уровня гормонов (общий тестостерон,глобулин, связывающий половые гормоны – ГСПГ, фолликулостимулирующий гормон – ФСГ, лютеинизирующий гормон – ЛГ, ингибин В) на фоне терапии препаратом «Мираксант»®.
В исследовании приняли участие 86 мужчин, проходящих обследование и лечение по поводу бесплодия в браке. Средний возраст наблюдаемых составил 31,6±5,8 года (19-45 лет). Средняя продолжительность бесплодного брака – 14,2±6,9 мес. Спермиологическое исследование проводилось и оценивалось в соответствии с Руководством ВОЗ 5-го пересмотра (2010). Критерии исключения: инфекционно-воспалительные заболевания урогенитального тракта, варикоцеле, генетические нарушения, эндокринные нарушения, аутоиммунное бесплодие.
Таким образом, исследуемую группу составили бесплодные мужчины с идиопатической патоспермией. Пациенты получали препарат «Мираксант»® на регулярной основе по одной капсуле (400 мг) 2 раза в день. Длительность лечения составляла 90 дней. Кроме медикаментозного лечения все пациенты получили рекомендации по изменению образа жизни и избавлению от вредных привычек.
В состав препарата «Мираксант»® входят: L-карнитин – 150 мг, Маки перуанской (Lepidium meyenii) корней сухой экстракт 10:1 – 165 мг, одноклеточной водоросли Hematococcus pluvialis сухой экстракт, содержащий Астаксантин – 60 мг, цинка цитрат – 50 мг (в пересчете на цинк – 17,05 мг).
Проверка достоверности изменения показателей относительно исходного уровня выполнялась для количественных переменных с использованием парного критерия Стьюдента (paired t-test), либо знаковым критерием Вилкоксона (Wilcoxon signed test) в случае ненормальности распределения признака.
РЕЗУЛЬТАТЫ
Исследование гормонального статуса
В ходе оценки гормонального статуса было выявлено незначительное, но достоверное увеличение уровня тестостерона. Уровень общего тестостерона до начала приема «Мираксанта»® и 3-хмесячного курса составил 17,57±5,08 и 17,86±4,9, соответственно (р=0,017) (рис. 1).
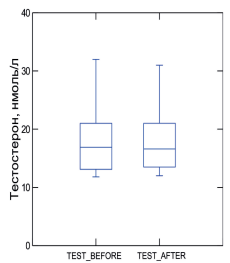
Рис. 1. Динамика уровня общего тестостерона при приеме «Мираксанта»
Уровень лютеинизирующего гормона до и после приема «Мираксанта»® практически не изменялся и составил 4,52±1,24 и 4,49±1,29 мМЕд/мл соответственно (р=0,642) (рис. 2).
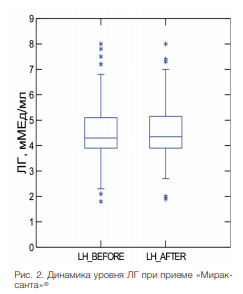
Рис. 2. Динамика уровня ЛГ при приеме «Мираксанта»®
Уровень фолликулостимулирющего гормона после приема «Мираксанта»® незначительно, но достоверно снижался с 5,71±2,96 до 5,24± 2,13 мМЕд/мл (р=0,045) (рис. 3).
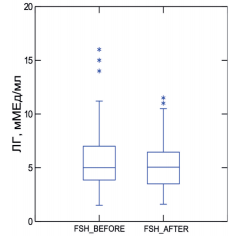
Рис. 3. Динамика уровня ФСГ при приеме «Мираксанта»®
Уровень пролактина в ходе исследования достоверно не изменился и составил 180,4±56,1 и 180,1±52,1 мЕд/л до и после лечения, соответственно (р=0,86). Уровень глобулина, связывающего половые гормоны, также достоверно не изменился. Показатель ингибина В в ходе исследования достоверно не менялся, но показал тенденцию к увеличению. Средний уровень ингибина В до и после применения препарата «Мираксант»® составил 127,6±17,3 и 139,5±28,8 пг/мл, соответственно.
Изменение параметров эякулята
Средняя концентрация сперматозоидов в эякуляте после 3 месяцев приема «Мираксанта»® достоверно увеличилась с 14,4±7,9•106 /мл до 15,8± 8,6 106/млн, (р=0,0001). Прирост показателя составил 9,7% (рис. 4).
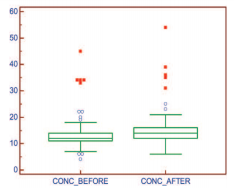
Рис. 4. Динамика средней концентрации сперматозоидов эякуляте, млн/мл
Общая подвижность сперматозоидов на фоне приема «Мираксанта»® достоверно и выраженно увеличилась (на 22,5%). Средний процент подвижных сперматозоидов до и после приема «Мираксанта»® составил 32,5±8,0% и 39,91±7,9%, соответственно (р<0,0001) (рис. 5).
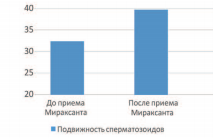
Рис. 5. Динамика показателя общей подвижности сперматозоидов в%
Морфология сперматозоидов по строгим критериям Крюгера достоверно не изменилась, но показала тенденцию к улучшению. Доля морфологически нормальных сперматозоидов увеличилась с 3,87±2,93% до 4,02±3,03% после приема «Мираксанта»® (р=0,25).
Общее количество сперматозоидов в эякуляте достоверно не изменилось.
В результате применения препарата «Мираксант»® отмечается выраженное и достоверное увеличение жизнеспособности сперматозоидов. Средняя величина показателя жизнеспособности до и после лечения составила 54,4±13,4% и 60,9±11,7% (р<0,0001). Средний прирост жизнеспособности относительно исходного значения составил 11,7% (рис. 6).
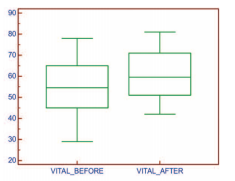
Рис. 6. Динамика жизнеспособности сперматозоидов на фоне приема «Мираксанта»® в%
Таким образом, после лечения у пациентов были отмечены следующие эффекты:
- Достоверное выраженное увеличение подвижности сперматозоидов на 22,5% к третьему месяцу лечения;
- Достоверное повышение жизнеспособности сперматозоидов на 11,7% после приема «Мираксанта»;
- Увеличение концентрации сперматозоидов на 9,7%;
- Хороший эффект от лечения достигнут у 20% пациентов. Удовлетворительный эффект – в 36,7% случаев. Таким образом, суммарный положительный эффект от приёма препарата составил 56,7%;
- Уровень общего тестостерона, ФСГ, ЛГ, пролактина и ГСПГ в ходе лечения не претерпел существенных изменений;
Каких-либо нежелательных или побочных эффектов, в ходе лечения (изменение А/Д, ЧСС, аритмии, приступы бессонницы и т.д.) зарегистрировано не было. Безопасность применения препарата «Мираксант»® так же подтверждена отсутствием динамики параметров функционирования жизненно важных органов и систем и какимилибо изменениями основных лабораторных показателей (клинический анализ крови, мочи, биохимический анализ крови).
ЗАКЛЮЧЕНИЕ
Данное проспективное несравнительное клиническое исследование по изучению препарата «Мираксант»® продемонстрировало его клиническую эффективность у 56,7% мужчин и безопасность применения при идиопатическом бесплодии. Являясь натуральным биологически активным комплексом препарат «Мираксант»® способствовал, в ряде случаев, достоверному увеличению концентрации, подвижности и жизнеспособности сперматозоидов, без развития каких-либо нежелательных побочных эффектов.
Результаты проведённого исследования позволяют рекомендовать использовать биологически активный комплекс «Мираксант»® в комплексной терапии бесплодных мужчин с идиопатической патоспермией.
ЛИТЕРАТУРА
1. Agarwal A, Nallella KP, Allamaneni SSR, Said TM. Role of antioxidants in treatment of male infertility: An overview of the literature. Reprod Biomed Online. 2004. doi:10.1016/S1472-6483(10)61641-0
2. Bagchi D. Oxygen free radical scavenging abilities of vitamins C, E, b-carotene, pycnogenol, Grape seed proanthocyanidin extract and astaxanthins in vitro 2001. Creighton University School of Health Sciences 2500 California Plaza. URL: https://www.cyanotech.com/ pdfs/bioastin/batl06.pdf
3. Boivin J, Bunting L, Collins JA, Nygren KG. International estimates of infertility prevalence and treatment-seeking: Potential need and demand for infertility medical care. Hum Reprod 2007;22(6), 1506–1512. doi:10.1093/humrep/dem046
4. Bray TM, Bettger WJ. The physiological role of zinc as an antioxidant. Free Radic Biol Med 1990:8(3), 281–291. doi:10.1016/0891-5849 (90)90076-U
5. Costa M, Canale D, Filicori M, D’lddio S, Lenzi A. L‐ carnitine in idiopathic asthenozoospermia: a multicenter study. Andrologia, 1994;26(3), 155–159. doi:10.1111/j.1439-0272.1994.tb00780.x
6. Evers JLH. Female subfertility. Lancet 2002;360:151–159. doi:10.1016/S0140-6736(02)09417-5
7. Gasco M, Villegas L, Yucra S, Rubio J, Gonzales GF. Dose-response effect of Red Maca (Lepidium meyenii) on benign prostatic hyperplasia induced by testosterone enanthate. Phytomedicine 2007;14(7–8), 460–464. doi:10.1016/j.phymed.2006.12.003
8. Gonzales C, Rubio J, Gasco M, Nieto J, Yucra S, Gonzales G. Effect of short-term and long-term treatments with three ecotypes of Lepidium meyenii (MACA) on spermatogenesis in rats. J Ethnopharmacol 2006;103(3), 448–454.
9. Gonzales GF, Cordova A, Gonzales C, Chung A, Vega K, Villena A. Improved sperm count after administration of Lepidium meyenii (maca) in adult men. Asian J Andrology 2001;3(4), 301–304. doi:10.1016/j.cell.2014.09.029
10. Hart R. Unexplained infertility, endometriosis, and fibroids. BMJ 2006;327(7417), 721–724. doi:10.1136/bmj.327.7417.721
11. Mascarenhas MN, Flaxman SR, Boerma T, Vanderpoel S, Stevens GA. National, Regional, and Global Trends in Infertility Prevalence Since 1990: A Systematic Analysis of 277 Health Surveys. PLoS Medicine 2012;9(12). doi:10.1371/journal.pmed.1001356
12. Moncada ML, Vicari E, Cimino C, Calogero AE, Mongioì A, D’Agata R. Effect of acetylcarnitine treatment in oligoasthenospermic patients. Acta Eur Fertil 1992;23(5), 221–4.
13. Ohta Y, Yoshida K, Kamiya S, Kawate N, Takahashi M, Inaba T, et al. Feeding hydroalcoholic extract powder of Lepidium meyenii (maca) increases serum testosterone concentration and enhances steroidogenic ability of Leydig cells in male rats. Andrologia, 2016;48(3), 347–354. doi:10.1111/and.12453
14. Özkan KU, Boran Ç, Kilinç M, Garipardiç M, Kurutaş EB. The Effect of Zinc Aspartate Pretreatment on Ischemia-Reperfusion Injury and Early Changes of Blood and Tissue Antioxidant Enzyme Activities after Unilateral Testicular Torsion-Detorsion. J Pediatr Surg 2004;39(1), 91–95. doi:10.1016/j.jpedsurg.2003.09.013
15. Piacente S, Carbone V, Plaza A, Zampelli A, Pizza C. Investigation of the tuber constituents of maca (Lepidium meyenii Walp.). J Agric Food Chem. 2002;50(20), 5621–5625. doi:10.1021/jf020280x
16. Prasad AS, Mantzoros CS, Beck FWJ, Hess JW, Brewer GJ. Zinc status and serum testosterone levels of healthy adults. Nutrition 1996;12(5), 344–348. doi:10.1016/S0899-9007(96)80058-X
17. Showell MG, Mackenzie-Proctor R, Jordan V, Hart RJ. Antioxidants for female subfertility. Cochrane Database of Systematic Reviews, 7, 2017;CD007807. doi:10.1002/14651858.CD007807.pub3
18. Uchiyama F, Jikyo T, Takeda R, Ogata M. Lepidium meyenii (Maca) enhances the serum levels of luteinising hormone in female rats. J Ethnopharmacol 2014;151(2), 897–902. doi:10.1016/ j.jep.2013.11.058
19. Wang JY, Lee YJ, Chou MC, Chang R, Chiu CH, Liang YJ, Wu LS. Astaxanthin protects steroidogenesis from hydrogen peroxide-induced oxidative stress in mouse Leydig cells. Marine Drugs 2015;13(3), 1375–1388. doi:10.3390/md13031375
20. Zegers-Hochschild F, Adamson GD, de Mouzon J, Ishihara O, Mansour R, Nygren K, et al. International Committee for Monitoring Assisted Reproductive Technology (ICMART) and the World Health Organization (WHO) revised glossary of ART terminology. Fertil Steril 2009;92(5), 1520–1524. doi:10.1016/j.fertnstert.2009.09.009
Статья опубликована в журнале "Экспериментальная и клиническая урология". Номер №1/2018 стр. 100-105











Комментарии