Р.О. Бегляров
Азербайджанский медицинский университет, г. Баку, Азербайджан
Гематурический хронический гломерулонефрит является одним из самых распространенных в детском возрасте и в то же время наименее изученным заболеванием почек. По данным литературы гематурическая форма в структуре хронического гломерулонефрита (ХГН) встречается у 22,1- 24,1% детей [1,2]. В настоящее время выявлено, что через 13,5 лет от начала гематурической ХГН у 13,6% детей отмечается развитие хронической почечной недостаточности І стадии, а по другим данным, через 15 лет течения заболевания у 11,0-15,5% детей развивается терминальная стадия хронической почечной недостаточности [1,3,4]. Ранее прогноз данной формы ХГН рассматривался как благоприятный [5,6].
Одним из ведущих механизмов развития заболеваний в целом, и ХГН в частности, является оксидативный стресс, в основе которого лежит избыточная, неконтролируемая выработка активных форм кислорода [7,8].
В настоящее время изучению свободнорадикальных процессов, которые объективно отражают тяжесть течения заболевания, придается большое значение. Одним из важных звеньев неспецифической резистентности организма является состояние антиоксидантной системы (АОС) и прооксидантной системы, находящей свое отражение в показателях перекисного окисления липидов (ПОЛ). Установлено, что с течением процесса происходит истощение пула эндогенных антиоксидантов, что имеет существенное значение для дальнейшей активации процессов ПОЛ [6,9]. Исследования показали, что у детей ПОЛ и состояние АОС в крови могут меняться в зависимости от реактивности организма и влияния различных средовых факторов. В норме у здоровых детей поддерживается сбалансированное соотношение между ними [6,9]. Недостаточная изученность активности патологического процесса гематурического ХГН, противоречивость имеющихся данных определяет актуальность этой проблемы.
Целью исследования явилось исследование интенсивности ПОЛ и состояние АОС у детей с гематурическойформой хронического гломерулонефрита.
МАТЕРИАЛЫ И МЕТОДЫ
Обследовано 126 детей. Основную группу составили 96 детей с гематурической формой ХГН, контрольную группу – 30 детей без ХГН. В группе с ХГН мальчиков было 58 (60,4%), девочек – 38 (39,6%). Возраст детей колебался от 7 до 15 лет, средний возраст – 12,06±2,14 лет. В возрасте 7-10 лет было 44 (45,8%), 11-15 лет – 52 (54,2%) детей. Длительность заболевания в среднем составила 4,12±1,77 лет. В контрольной группе мальчиков было 19 (63,3%), девочек – 11 (36,7%), средний возраст – 10,7±5,11 лет.
Стадия клинической ремиссии отмечалась у 53 (55,2%), обострение ХГН наблюдалось у 43 (44,8%) пациентов.
Применены общеклинические, биохимические и инструментальные (ультразвуковые – УЗИ) методы исследования. Выраженность гематурии определяли проведением пробы по Нечипоренко. Число эритроцитов не более 10х106/л считали незначительной гематурией, количество эритроцитов в диапазоне от 10х106/л до 60х106/л – считали умеренной гематурией, количество эритроцитов более 60х106 /л – выраженной гематурией.
Интенсивность ПОЛ оценена по уровню продуктов: первичных – диеновых конъюгатов (ДК) и вторичных – малонового диальдегида (МДА). Определение ДК проводили в гексановых экстрактах сыворотки крови с помощью спектрофотометрии [10]; МДА – в тесте с тиобарбитуровой кислотой [11]. Состояние АОС определяли по активности каталазы, по уровню восстановленного глутатиона (GSH), активности глутатионпероксидазы (ГПО) и – глутатионредуктазы (ГР). Активность каталазы определяли по образованию перекиси водорода с молибдатом аммония [12]; концентрацию GSH – по изменению оптической плотности по методике G.L. Ellman [13]; ГПО – по методу А.Р. Гавриловой [14]; ГР – по B.C. Асатиани [15]. Показатели АОС определяли в плазме крови и эритроцитах.
Для выделения эритроцитов венозную кровь с гепарином центрифугировали 20 мин при 3000 об/мин, после чего отбирали плазму, а оставшуюся эритроцитарную массу промывали физиологическим раствором трижды и центрифугировали по 15 минут при 3000 об/мин. Супернатант отделяли. Для более плотной упаковки клеток последнее центрифугирование проводили в течение 20 мин. Активность ГПО и ГР оценивали по снижению экстинкции за 1 мин при λ=340 нм, что соответствовало снижению концентрации кофермента НАДФН. Активность всех ферментов пересчитывали на концентрацию белка в пробе (Б). Концентрацию белка оценивали на фотоколориметре при λ=600 нм. Расчет активности фермента производился по формуле:
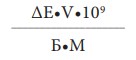
где: ΔЕ – изменение экстинкции за 1 минуту; V – объем кюветы (2 мл для ГР и 1 мл для ГПО); Б – концентрация белка в пробе; М – коэффициент молярной экстинкции (М=для ГПО и для ГТ).
Статистическую обработку результатов осуществляли путем использования стандартных пакетов программы Statistica version 6,0 (США). Рассчитывали среднее значение (M), стандартную ошибку (m) и стандартное отклонение (δ). Средние значения представлены в виде М±m. Использованы параметрический критерий признаков t Стьюдента и непараметрический – U-критерий Манна-Уитни. Критический уровень значимости при проверке статистических гипотез принимался р<0,05.
РЕЗУЛЬТАТЫ
Результаты исследования показали, что у 52 (54,2%) пациентов имелась отягощенная наследственность по заболеваниям органов мочевой системы. По данным анамнеза дети часто болели ОРВИ (60,4%), ангиной (28,1%),гриппом (11,5%). У 34 (35,4%) пациентов ХГН сопровождалась аллергическими заболеваниями, у 18 (18,8%) – заболеваниями желудочно-кишечного тракта, у 10 (10,4%) – глистными инвазиями.
По данным УЗИ почек у 70 (72,9%) пациентов изменений в почках не визуализировалось, у 16 (16,7%) – отмечалась гиперэхогенность коркового вещества и у 10 (10,4%) больных – увеличение размеров почек. Характерными изменениями в общем анализе крови был низкий гемоглобин – у 57,2%; в общем анализе мочи – эритроцитурия у всех (100%), протеинурия – у 86,4%, кристаллурия – у 84,4%, лейкоцитурия – у 47,9%, цилиндрурия – у 30,2% пациентов. В пробе по Нечипоренко незначительная эритроцитурия отмечалась у 18 (18,7%), умеренная – у 20 (20,8%), выраженная – у 58 (60,4%) больных, незначительная лейкоцитурия выявлена у 37 (38,5%), умеренная – у 8 (8,3%), выраженная – у 1 (1,0%) пациента.
Дети основной группы с обострением гематурического ХГН на момент обследования отмечали боли в животе (20,8%) и в пояснице (19,8%), макрогематурию (32,3%), астению (36,4%). У больных в стадии ремиссии отмечались боли в животе (16,7%) и пояснице (10,4%). У пациентов в стадии обострения эритроцитурия в среднем составила 181,6±33,8 в п/зр, в стадии ремиссии – 42,8±10,4 в п/зр (р<0,01). У всех 43 пациентов с обострением ХГН в разовых порциях мочи определялся белок, у пациентов в стадии ремиссии протеинурия наблюдалась в 39,6% случаев.
Исходя из современных представлений о сущности патологических процессов, которые основываются на признании ведущей роли повреждения клеточных мембран, нами изучено содержание продуктов ПОЛ, представляющих информацию о протекающих свободно-радикальных реакциях, поддерживаемых специализированными системами. Результаты изучения содержания продуктов ПОЛ в плазме и эритроцитах приведены в таблице 1.
Таблица 1. Уровень диеновых конъюгатов и малонового диальдегида в крови у обследованных детей
| Показатель | Основная группа (n=96) | Контрольная группа (n=30) | |
|---|---|---|---|
| ДК, мкмоль/мл | плазма | 0,83±0,22 | 0,80±0,11 |
| эритроциты | 0,72±0,16 | 0,68±0,06 | |
| МДА, мкмоль/л | плазма | 2,83±0,61* | 1,60±0,34 |
| эритроциты | 2,39±0,55* | 1,51±0,08 | |
*статистическая достоверность различий между группами (р<0,05)
Как видно из таблицы 1, содержание ДК, являющегося первичным продуктом ПОЛ, в плазме крови и в эритроцитах пациентов практически не отличалось от контрольного. Напротив, концентрация вторичного продукта ПОЛ – МДА и в плазме, и в эритроцитах превышала контрольный уровень в среднем на 76,9% (р<0,01) и 58,3% (р<0,05) соответственно. При этом, более высокие значения МДА отмечались у пациентов с активной фазой процесса (рис. 1).
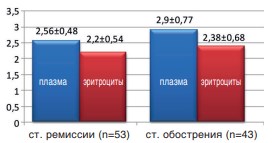
Рис.1. Средний уровень МДА (мкмоль/л) в плазме и в эритроцитах у детей с гематурической ХГН при обострении (n=43) и в стадии ремиссии (n=53)
Как видно из таблицы 2, активность каталазы в сравнении с контрольной величиной была незначительно снижена в плазме (на 7,9%) и достоверно – в эритроцитах (на 40,4%, р<0,05). Также выявлялось снижение активности глутатионовых ферментов. Наиболее выраженная разница относительно контрольного уровня отмечалась в отношении фермента глутатионредуктазы (ГР). Активность этого фермента в плазме в среднем была снижена на 42,9% (р<0,05), в эритроцитах – на 48,1% (р<0,05). Активность другого фермента данной редокс-системы– глутатионпероксидаза (ГПО) в сравнении с контрольным показателем была снижена в плазме и в эритроцитах почти одинаково – в среднем на 32,5% (р<0,05) и на 32,1% (р<0,05) соответственно. Уровень восстановленного глутатиона (GSH) в сравнении с контрольным уровнем был ниже на 26,5% (р<0,05) и на 43,9% (р<0,05) соответственно в плазме и в эритроцитах.
Таблица 2. Показатели АОС у детей с гематурической формой ХГН
| Показатели | Группы | ||
|---|---|---|---|
| Основная группа (n=96) | Контрольная группа (n=30) | ||
| Каталаза, ед/мл | плазма эритроциты |
51,2±1,38 1217,4±22,44* |
55,6±1,90 2043,1±12,5 |
| GSH, нмоль/мл мкмоль/мл | плазма эритроциты |
13,3±1,22* 0,87±0,11* |
18,1±1,84 1,55±0,10 |
| ГПО, нмоль/мин на 1 мг белка | плазма эритроциты |
1,31±0,08* 5,08±0,57* |
1,94±0,04 7,48±0,47 |
| ГР, нмоль/мин на 1 мг белка | плазма эритроциты |
0,24±0,06* 1,10±0,31* |
0,42±0,03 2,12±0,14 |
При сравнительном анализе величин показателей АОС у пациентов в стадии клинической ремиссии и обострения патологического процесса выявлено более выраженное снижение показателей этой системы у последних (табл. 3).
Таблица 3. Показатели АОС у больных с гематурической формой ХГН на фоне ремиссии и обострения
| Показатели | Основная группа (n=96) | Контрольная группа (n=30) | ||
|---|---|---|---|---|
| в стадии ремиссии (n=53) | в стадии обострения (n=43) | |||
| Каталаза, ед/мл | плазма эритроциты |
53,0±2,04 1407,2±38,8* |
51,26±1,07 1212,8±29,6* |
55,6±1,90 2043,1±12,5 |
| GSH, нмоль/мл мкмоль/мл | плазма эритроциты |
13,8±1,46* 0,88±0,17* |
12,8±1,38* 0,84±0,16* |
18,1±1,84 1,55±0,10 |
| ГПО, нмоль/мин на 1 мг белка | плазма эритроциты |
1,31±0,04* 5,12±0,82* |
1,30±0,07* 5,04±0,66* |
1,94±0,04 7,48±0,47 |
| ГР, нмоль/мин на 1 мг белка | плазма эритроциты |
0,25±0,04* 1,12±0,34* |
0,22±0,06* 1,08±0,27* |
0,42±0,03 2,12±0,14 |
*статистическая достоверность различий между группами больных и контрольной группой (р<0,05)
При анализе полученных данных выявлено, что активность каталазы в плазме крови при обостренном и необостренном процессе существенно не отличалась и была незначительно ниже контрольной группы. В тоже время в эритроцитах активность данного фермента у пациентов с клинической ремиссией относительно пациентов с обострением была выше на 16,0% и ниже контрольной величины на 31,1% (р<0,05). Средняя активность фермента в эритроцитах у пациентов с обострением ХГН была также ниже контрольного показателя на 40,6% (р<0,05). Максимальное содержание восстановленного глутатиона в плазме и эритроцитах отмечалось у детей с клинической ремиссией и минимальное – с обострением ХГН и в обеих группах уровень GSH было достоверно ниже, чем в контрольной группе. Активность плазменного и эритроцитарного ГПО при активном и неактивном течение ХГН практически не различались, но были достоверно ниже контрольной (р<0,05). Аналогичная ситуация наблюдалась и в отношении уровня ГР. Активность этого фермента в плазме и в эритроцитах при клинической ремиссии и обострении ХГН между собой существенно не различались, но достоверно снижены (p<0,05) относительно контрольных показателей.
Следовательно, у детей с обострением ХГН гематурической формы из исследованных ферментов наиболее существенное различие наблюдалось в отношении ГПО и ГР. Активность этих ферментов по сравнению с контрольным уровнем была снижена, соответственно, на 33,0 и 52,4% (р<0,05) в плазме и на 32,6 и 49,1% в эритроцитах (р<0,05). При этом, плазменная активность ГПО и ГР была ниже эритроцитарной. Содержание GSH в эритроцитах было более сниженным (на 49,1%, р<0,05), чем в плазме (на 29,3%, р<0,05).
ОБСУЖДЕНИЕ
Таким образом, результаты проведенного исследования указывают на выраженное развитие окислительного стресса при гематурической форме ХГН, о чем свидетельствуют процессы ПОЛ и истощение пула антиоксидантной системы защиты. Отметим, что данные литературы подтверждают важную роль процессов ПОЛ и АОС в повреждении почечных структур. Исследование процесса свободнорадикального окисления ведется и в педиатрической нефрологии, в том числе и при ГН [7]. В литературе приводятся сведения о том, что повышение уровня показателей ПОЛ может служить предиктором прогрессирования заболеваний почек, поэтому определение показателей прооксидантно-антиоксидантного состояния является важным фактором, влияющим на течение и прогрессирование ГН [8]. Полученные нами результаты согласуются с этими доводами. Об этом свидетельствовала разница концентрации МДА, которая в плазме и в эритроцитах у детей с обострением была выше величин вне обострения. Следует отметить, что МДА – это вторичный продукт ПОЛ, увеличение которого провоцирует синдром интоксикации [6]. Повышение уровня МДА свидетельствует об усилении ПОЛ, что способствует изменениям в функциях мембраны клетки, а также структурной дезорганизации ДНК клетки [6,7]. При этом возрастание уровня МДА и ДК в эритроцитах происходит на фоне снижения активности системы глутатиона. Сравнительный анализ показателей контрольной группы и группы с обострением позволил получить достоверные результаты, подтверждающие наличие прооксидантно-антиоксидантного дисбаланса у детей с гематурической формой ХГН. Анализируя полученные результаты, можно наблюдать, что высокая интенсивность ПОЛ не может быть остановлена сниженными компонентами АОС, что не позволяет поддерживать состояние мембран и соответственно мембранзависимых компонентов на нужном уровне, поскольку избыточное накопление первичных и особенно вторичных продуктов ПОЛ, имеющее место при ХГН, которые вызывают нарушение проницаемости структур и функции биомембран, повреждение липидов, белков, нуклеиновых кислот, изменение биоэнергетики и т.д. [7,8]. Результаты исследования и литературные данные свидетельствуют о том, что в большинстве случаев одним из механизмов развития патологического процесса и его хронизации является дисбаланс в системе перекисного каскада с ослаблением АОС.
Содержание МДА в плазме крови и эритроцитах, а также показатели активности АОС являются дополнительными компонентами в комплексном обследовании детей с ХГН, характеризующими степень патологического процесса.
Таким образом, у детей с гематурической формой ГН отмечается повышение вторичного продукта ПОЛ – МДА и снижение глутатионового звена АОС, особенно выраженное при обостренном течение заболевания.
ЛИТЕРАТУРА
- Лоскутова С.А., Чупрова А.В., Мовчан Е.А. Выживаемость больных первичным гломерулонефритом, дебютировавшем в детском возрасте. Педиатрия 2005;(4):29-33.
- Ни А., Лучанинова В.Н. Результаты катамнестического наблюдения детей, перенесших гломерулонефрит. Педиатрия 2009;87(3):39-42.
- Swaminathan S, Shah SV. Novel approaches targeted toward oxidative stress for the treatment of chronic kidney disease. Cur Opin Nephr Hypertens 2008;2(17): 143-148.
- Yata N, Nakanishi K, Shima Y, Togawa H, Obana M, Sako M, et al. Improved renal survival in Japanese children with IgA nephropathy. Pediatr nephrol 2008;23(6):905-912.
- Герасименко О.Н. Хронический гломерулонефрит (гематурическая форма) в детском возрасте: клинико-морфологические особенности и прогностические факторы. Здоровье ребенка 2011;(4):22-26.
- Игнатова М.С. Гломерулопатии у детей. Педиатрия 2011;90(3):125-127.
- Конюшевская А.А. Состояние перекисного окисления липидов и антиоксидантной защиты при остром гломерулонефрите у детей, проживающих в экологически неблагополучном регионе. Здоровье ребенка 2011;(3):23-27.
- Hastings MC, Wyatt RJ, Santos NM. Renal survival in pediatric patients with IgA nephropathy. Pediatr nephrol 2007;22 (2):317-318.
- Лучанинова В.Н. Актуальные вопросы детской нефрологии. Владивосток: Медицина ДВ. 2012.
- Каган В.Е., Орлов В.Н., Прилипко Л.Л. Проблема анализа эндогенных продуктов перекисного окисления липидов. М.: Наука. 1986.
- Андреева Л.И., Кожемякин Л.А., Кишкун А.А. Модификация метода определения перекисей липидов в тесте с тиобарбитуровой кислотой. Лабораторно дело 1988;(11):41-43.
- Королюк М.А., Иванова Л.И., Майорова И.Г. Метод определения активности каталазы. Лабораторное дело 1988;(1):16-17.
- Ellman G.L. Tissue sulfhydryl groups. Arch Biochem Biophys 1959;82(l):70-77.
- Гаврилова А.Р., Хмара Н.Ф. Определение активности глутатионпероксидазы эритроцитов при насыщающих концентрациях субстратов. Лабораторное дело 1986;(12):21-24.
- Асатиани В.С. Ферментные методы анализа. М.: Наука. 1969.
Статья опубликована в журнале"Экспериментальная и клиническая урология" №2 2018, стр.130-133









Комментарии