Мартов А.Г., Турин Д.Е., Ергаков Д.В., Андронов А.С., Камалов А.А.
Сведения об авторах:
- Мартов А.Г. – д.м.н., профессор, заведующий кафедрой урологии и андрологии ИППО ФГБУ ГНЦ ФМБЦ имени А.И. Бурназяна ФМБА РФ, заведующий урологическим отделением, ГБУЗ ГКБ имени Д.Д. Плетнева, martovalex@mail.ru, AuthorID 788667
- Ергаков Д.В. – к.м.н., доцент кафедры урологии и андрологии ИППО ФГБУ ГНЦ ФМБЦ имени А.И. Бурназяна ФМБА РФ, врач-уролог урологического отделения, ГБУЗ ГКБ имени Д.Д. Плетнева, dergakov@mail.ru
- Турин Д.Е. – аспирант кафедры урологии и андрологии ИППО ФГБУ ГНЦ ФМБЦ имени А.И. Бурназяна ФМБА РФ, врач ФГБУ «12 КДЦ» Минобороны РФ, dmit.turin2013@yandex.ru
- Андронов А.С. – к.м.н., ассистент кафедры урологии и андрологии ИППО ФГБУ ГНЦ ФМБЦ имени А.И. Бурназяна ФМБА РФ, врач урологического отделения, ГБУЗ ГКБ имени Д.Д. Плетнева, dr.andronov@mail.ru
- Камалов А.А. – д.м.н., профессор, академик РАН, директор МНОЦ МГУ им. М.В. Ломоносова, roo.rusmh@gmail.com, AuthorID 759356
Консервативное и оперативное лечение пациентов с симптомами нарушения функции нижних мочевых путей (СНМП) вследствие доброкачественной гиперплазии предстательной железы (ДГПЖ) является одной из распространенных и актуальных проблем урологии [1]. За последние два десятилетия был достигнут значительный прогресс как в понимании причин развития СНМП, так и в их терапии [2]. Так, было показано, что ДГПЖ не является более единственной причиной возникновения СНМП у мужчин. Было выявлено, что нарушение функции мочевого пузыря, а также целый ряд урологических (мочекаменная болезнь, онкоурологические заболевания) и экстрагенитальных заболеваний (болезнь Паркинсона, рассеянный склероз, сахарный диабет и др.) могут лежать в основе клинических проявлений, которые урологи и врачи общей практики традиционно связывают с имеющейся у большинства мужчин пожилого и старческого возраста ДГПЖ [3]. Естественно, что результаты оперативного лечения у этой категории пациентов, весьма вероятно, будут далеки от удовлетворительных (снижение показателей по шкале I-PSS, повышение индекса качества жизни, отсутствие недержания мочи и ургентности, уменьшение частоты дневных и ночных мочеиспусканий, возрастание максимальной и средней скорости потока мочи, увеличение среднего объема микции) [4]. Комплексное уродинамическое исследование (КУДИ) и определение показателя «давление-поток» является «золотым» стандартом диагностики состояния детрузора и позволяет заподозрить иные причины, кроме ДГПЖ в качестве причины расстройств мочеиспускания [5]. Вследствие инвазивности КУДИ, возможности возникновения инфекционно-воспалительных осложнений частота его предоперационного применения не превышает 5-10% [6]. В этой связи представляется весьма актуальным выявление прогностических факторов персистирования ирритативных симптомов после операции, на основании которых пациент может быть заранее проинформирован о возможной неэффективности или лишь о частичном улучшении СНМП после операции [7].
С другой стороны, в результате большого многоцентрового исследования EpiLUTS было показано, что СНМП вследствие ДГПЖ более чем у половины пациентов представляют из себя комбинацию обструктивных (вялая струя мочи, долгое время мочеиспускание, ощущение неполного опорожнения мочевого пузыря) и ирритативных жалоб (позывы на мочеиспускания, учащенное мочеиспускание днем и ночью, малый объем микции) [8]. Учитывая сочетанный характер расстройств мочеиспускания, комбинированная терапия М-холиноблокаторами и альфа-адреноблокаторами становится все более и более популярной, хотя все еще значительно уступает по частоте использования монотерапии альфа-адреноблокаторами [9]. Тем не менее, все чаще на прием к врачу-урологу обращаются пациенты, которые до операции получают комбинированную терапию [10]. Данные о функциональных результатах оперативного лечения у этой категории пациентов пока также отсутствуют, что является основанием для проведения собственных исследований. Третьим аспектом этой темы является большая разнородность данных различных исследований по функциональным результатам после проведенного оперативного лечения, так как во многих исследованиях результаты получены на азиатских когортах пациентов, у которых отмечена более высокая частота встречаемости гиперактивности детрузора и более высокая аффинность альфа1А-адренорецепторов [11].
Неоднородность данных отмечается еще и вследствие того, что под единым термином «трансуретральная резекция предстательной железы» подразумеваются различные электрохирургические, а иногда и лазерные методы лечения (инцизия, вапоризация, энуклеация и т.д.) ДГПЖ, функциональные результаты, которых не могут быть одинаковыми [12].
Последним, но не менее важным нюансом данной темы является объем предстательной железы (ПЖ) и количество удаленной ткани. В большинстве исследований по результатам оперативного лечения средний объем ПЖ не превышает 50 см3, а количество удаленной ткани – 20 см3, все это служит обоснованием для отдельного изучения СНМП после операции у пациентов с большими (более 80 см3 ) железами для детальной оценки послеоперационных изменений [13].
В нашей клинике проводится комбинированная терапия расстройств мочеиспускания после трансуретральной резекции ПЖ больших размеров с использованием альфа-адреноблокаторов и м-холиноблокаторов. Однако раздельное применение двух препаратов неудобно пациентам, которые принимают несколько препаратов, дозировка М-холиноблокатора требует титрования дозы, поэтому появление фиксированной комбинации тамсулозина 0,4 мг и солифенацина 6 мг открывает новые возможности в терапии расстройств мочеиспускания у пациентов после трансуретральной резекции ПЖ больших размеров.
В связи с вышеизложенными фактами нами проведено самостоятельное проспективное рандомизированное исследование по изучению сравнительной эффективности и безопасности использования фиксированной комбинации альфа-адреноблокатора и М-холиноблокатора и монотерапии альфа-адреноблокаторами у пациентов после трансуретральной резекции ПЖ разного объема. Целью данного исследования являлась оценка динамики СНМП после операции в зависимости от исходного объема ПЖ.
МАТЕРИАЛЫ И МЕТОДЫ
С января 2017 г. по февраль 2018 г. в отделении урологии ГКБ имени Д.Д. Плетнева выполнено 288 трансуретральных резекций ПЖ по поводу СНМП вследствие ДГПЖ различного размера. Всем пациентам было проведено комплексное клинико-лабораторное обследование, в результате которого из исследования исключались пациенты с возможной нарушенной функцией мочевого пузыря (гипотония детрузора, нейрогенный мочевой пузырь, гиперактивный мочевой пузырь). У 27 пациентов были выявлены критерии исключения: наличие цистостомического дренажа (5 пациентов) или уретрального катетера (2), камни мочевого пузыря (6), неврологические заболевания (4), инсулинопотребный сахарный диабет (3), колостома (1), количество остаточной мочи более 150 мл и/или дивертикулы мочевого пузыря (6) (табл. 1).
Таблица 1. Причина исключения пациентов из исследования
| Причина | Количество пациентов |
|---|---|
| Цистостомический дренаж | 5 |
| Уретральный катетер | 2 |
| Неврологические заболевания (б-знь Паркинсона, состояние после ОНМК и др) | 4 |
| Инсулинопотребный сахарный диабет | 3 |
| Колостома | 1 |
| Камни мочевого пузыря | 6 |
| Остаточная моча до операции выше 150 мл, наличие крупных дивертикулов МП | 6 |
| Всего | 27 |
Таблица 2. Результаты предоперационного обследования пациентов в группах с различным обьемом ПЖ
| Показатель | Группа 1 (п=93) объем ПЖ <40 см3 |
Группа 2 (п = 102) объем ПЖ 41-80 см3 |
Группа 3 (п=66) объем ПЖ >80 см3 |
|---|---|---|---|
| IPSS, балл | 23,8 ± 3,4 | 24,3 ± 3,3 | 24,4 ± 3,5 |
| Обструктивный IPSS, балл | 12,3 ±2,6 | 12,2 ±2,5 | 12,2 ±2,6 |
| Ирритативный IPSS, балл | 11,5 ±2,4 | 11,1 ±2,3 | 11,2 ±2,4 |
| ВАШ, балл | 48 ±24 | 42 ±22 | 41 ±20 |
| QoL, балл | 4,3 ±1,5 | 4,5 ± 1,6 | 4,4 ± 1,5 |
| Объем предстательной железы, см3 | 35 ± 14 | 66 ± 16* | 108 ± 21**,*** |
| Qmax, мл/сек | 8,9 ± 1,5 | 7,7 ± 1,3 | 6,3 ±1,2 |
| Остаточная моча, мл | 82 ±23 | 108 ±28 | 103 ±24 |
| Объем микции, мл | 230 ± 23 | 200 ± 20 | 180 ± 15 |
Всего в исследование был включен 261 пациент. На этапе включения в исследование субъективные жалобы оценивались по опросникам IPSS/QoL, заполнялась визуальная аналоговая шкала (ВАШ) (0 – плохо, 100 – хорошо). Всем пациентам проводилось стандартное объективное обследование, оценивался урологический статус, проводилось пальцевое ректальное исследование ПЖ. Объективное обследование включало в себя трансректальное ультразвуковое исследование с определением остаточной мочи, ультразвуковое исследование мочевого пузыря и почек, урофлоуметрию. Целью лабораторного обследования была оценка стандартных показателей крови и мочи, необходимых для выполнения планового оперативного лечения, исключение инфекции мочевых путей и выявление подозрений на рак ПЖ. В таблице 2 приведены результаты предоперационного обследования пациентов в трех группах в зависимости от объема ПЖ.
Дооперационная терапия СНМП включала в себя у 162 (66%) пациентов монотерапию альфа-адреноблокаторами, у 99 пациентов проводилась комбинированная терапия, из них комбинированный прием альфа-адреноблокатора и М-холинолитика – у 31 (12%) пациента.
В зависимости от исходного объема ПЖ пациенты были разделены на три группы: 1 группа – объем ПЖ до 40 см3 (n = 93), 2-я – от 41 до 80 см3 (n = 102), 3-я – более 81 см3 (n = 66).
Все пациенты были оперированы по поводу СНМП вследствие ДГПЖ в течение 30 дней после включения в исследование. Всем пациентам выполнена биполярная трансуретральная резекция ПЖ. После удаления уретрального катетера на 2-3-и сутки после операции в зависимости от проводимой послеоперационной терапии каждая группа была разделена на три равные подгруппы: по 31 (1 группа), 34 (2 группа) и 22 (3 группа) пациента в каждой из групп соответственно: I подгруппа получала антибактериальный препарат и нестероидные противовоспалительные свечи 7 дней, II подгруппа – дополнительно назначался тамсулозин с пролонгированным высвобождением на срок 3 месяца, III подгруппа – дополнительно к тамсулозину с пролонгированным высвобождением солифенацин в дозировке 6 мг в составе комбинированного препарата также в течение 3 месяца. До операции и спустя 1 и 3 месяца после операции отслеживались следующие показатели: ВАШ, индекс IPSS, QoL, объем остаточной мочи, урофлоуметрия, средний объем микции. Статистическая обработка проводилась с использованием программы Статистика 6.0. Достоверным считалось отличие при показателе Фишера p<0,05 при сравнении дооперационных показателей с показателями спустя 1 и 3 месяца от момента операции в пределах одной подгруппы.
В послеоперационном периоде все больные отмечали вышеописанные СНМП, выраженные в различной степени. Данные сроки и дизайн исследования был выбран исходя из дизайна предыдущих исследований по этой теме, в том числе и проведенных клиникой ранее [4,13]. Исследование было одобрено локальным этическим комитетом. На рисунке 1 представлен дизайн исследования.
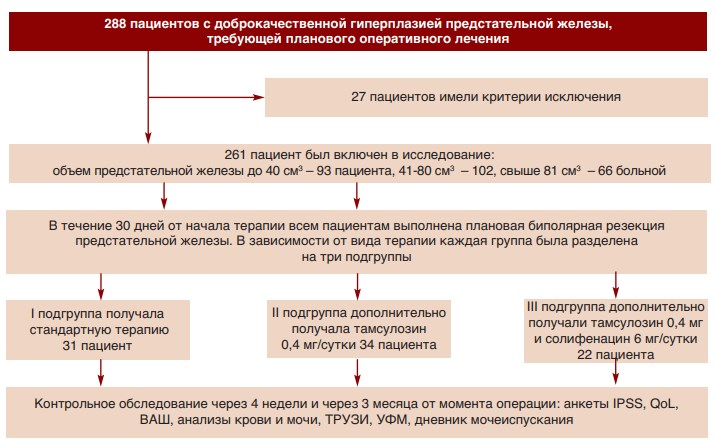
Рис. 1. Дизайн исследования по сравнительной оценке эффективности фиксированной комбинации м-холиноблокатора и альфа-адреноблокатора и монотерапии альфа-адреноблокаторами у пациентов с дизурией после биполярной трансуретральной резекции по поводу ДГПЖ в зависимости от ее размеров.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Предоперационное обследование пациентов показало, что за исключением объема ПЖ остальные показатели были одинаковыми и отражали наиболее часто встречающиеся данные у пациентов с показаниями для проведения оперативного лечения (табл. 2). Характерно, что у данной группы пациентов не было исходного преобладания обструктивных или ирритативных симптомов. Средний объем мочеиспускания варьировал от 180 до 230 мл, при показателях остаточной мочи от 82 до 108 мл. В группе пациентов с малым (до 40 см3) объемом ПЖ было удалено в среднем 25 грамм ткани, в группе со средними размерами (средний объем – 66 см3 ) – 52 грамма и в случаях наличия ПЖ большого объема (108 см3 ) – 85 грамм. Остальные показатели интра- и послеоперационного периода так же зависили от объема ПЖ: то есть чем больше исходный размер ПЖ, тем больше было время операции, дольше сроки стояния уретрального катетера и дольше сроки госпитализации (табл. 3).
Таблица 3. Результаты основных интра- и послеоперационных показателей пациентов исследуемых групп
| Показатель | Г руппа 1 (п=93) | Группа 2 (п = 102) | Группа 3 (п=66) |
|---|---|---|---|
| Вес удаленной ткани, г | 25,5 ± 5,3 | 52,4 ± 8,6* | 85,4 ± 12,3**,*** |
| Время операции, мин | 35,5 ±12,6 | 52,2 ± 13,5 | 67,7 ± 18,3** |
| Сроки стояния уретрального катетера, часы | 38,5 ± 3,4 | 48,2 ±6,2* | 60,4 ± 7,1** |
| Послеоперационный койко-день | 2,2 ± 1,2 | 3,4 ± 1,3 | 4,1 ± 1,5** |
Примечание: * р1-2< 0,05, ** р1-3< 0,05, *** р2-3< 0,05
Показатель ВАШ (табл. 4) является интегральным субъективным показателем, когда пациент описывает общее самочувствие. Во всех трех группах отмечается сходная тенденция, дооперационный показатель (41-48 баллов) повышается после операции, достигая через 1 месяц в первых подгруппах каждой из групп показателя 57-63 балла, во вторых подгруппах – 65-78 баллов и в третьих подгруппах – 84- 91 балл. Спустя 3 месяца аналогичные показатели были 72-81 балл, 80-85 баллов и 90-93 балла, соответственно. Наиболее выраженное улучшение было отмечено в подгруппах комбинированной терапии и в подгруппах, где после операции применялся тамсулозин, выраженное улучшение наступало уже к концу 1 месяца и сохранялось на протяжении всего срока наблюдения. В первых подгруппах даже к концу третьего месяца наблюдения показатели ВАШ не достигли показателей, которые были в третьих подгруппах уже к концу первого месяца терапии.
Таблица 4. Динамика показателей визуальной аналоговой шкалы (в баллах) до операции и спустя 1 и 3 месяца после операции
| Подгруппа | До операции | Спустя 1 месяц | Спустя 3 месяца |
|---|---|---|---|
| Группа 1 (n = 93) | |||
| Подгруппа I | 48 ±24 | 63 ± 16 | 81 ± 17** |
| Подгруппа II | 48 ±24 | 78 ± 15 | 85 ± 13** |
| Подгруппа III | 48 ±24 | 91 ±4’ | 93 ± 6** |
| Группа 2 (п = 102) | |||
| Подгруппа I | 42 ±22 | 59 ± 15 | 75 ± 16 |
| Подгруппа II | 42 ±22 | 71 ± 14 | 80 ± 14** |
| Подгруппа III | 42 ±22 | 88 ±10* | 91 ± 6** |
| Группа 3 (n = 66) | |||
| Подгруппа I | 41 ±20 | 57 ± 17 | 72 ± 15 |
| Подгруппа II | 41 ±20 | 65 ± 16 | 81 ± 13** |
| Подгруппа III | 41 ±20 | 84 ±9’ | 90 ± 5**, *** |
Примечание: * р1-2< 0,05, ** р1-3< 0,05, *** р2-3< 0,05
Таблица 5. Динамика показателей шкалы IPSS (в баллах) до операции и спустя 1 и 3 месяца после операции
| Подгруппа | До операции | Спустя 1 месяц | Спустя 3 месяца |
|---|---|---|---|
| Группа 1 (n = 93) | |||
| Подгруппа I | 23,8 ± 3,6 | 16,5 ± 3,2* | 12,2 ±2,1** |
| Подгруппа II | 23,8 ± 3,6 | 14 ± 2,9* | 11,6 ±2** |
| Подгруппа III | 23,8 ± 3,6 | 11,9 ±2,8* | 10,2 ± 1,8** |
| Группа 2 (n = 102) | |||
| Подгруппа I | 24,3 ± 3,5 | 17,3 ±3,1* | 13,4 ±2,2** |
| Подгруппа II | 24,3 ± 3,5 | 13,9 ±3* | 12,1 ±2** |
| Подгруппа III | 24,3 ± 3,5 | 12,6 ±2,8* | 10,6 ± 1,7** |
| Группа 3 (n = 66) | |||
| Подгруппа I | 24,4 ± 3,4 | 17,5 ±2,9* | 13,7 ±2** |
| Подгруппа II | 24,4 ± 3,4 | 14,7 ±2,7* | 12,4 ± 1,8** |
| Подгруппа III | 24,4 ± 3,4 | 12,9 ±2,6* | 10,8 ± 1,5** |
Примечание: * р1-2< 0,05, ** р1-3< 0,05, *** р2-3< 0,05
В таблице 5 приведена динамика показателей шкалы IPSS в зависимости от исходного размера ПЖ. Исходный уровень IPSS соответствовал показателям СНМП сильной степени выраженности во всех группах (23,8-24,4), спустя 1 месяц после операции во всех девяти подгруппах зарегистрировано статистически достоверное снижение суммарного балла по шкале IPSS до уровня СНМП средней степени выраженности (11,9–17,5 баллов), а через 3 месяца отмечено дальнейшее снижение (10,2-13,7 баллов). Наиболее выраженное улучшение было отмечено в третьих подгруппах каждой из групп, т.е. у пациентов, получавших комбинацию альфа-адреноблокатора и м-холинолитика. Менее выраженное улучшение было отмечено в подгруппах, принимавших дополнительно альфа-адреноблокатор. В подгруппах, где использовалась дополнительная терапия, улучшение наступало уже к концу первого месяца и сохранялось на протяжении всего периода наблюдения. Уровень IPSS зависил от исходного объема ПЖ, так как суммарный уровень симптомов был более выражен в третьей группе по сравнению с первой группой пациентов.
Показатели изменения шкалы качества жизни приведены в таблице 6. Предоперационный показатель QoL колебался от 4,3 до 4,5 баллов, во всех группах снижался через 1 месяц до уровня 2,2-3 балла и через 3 месяца оставался на прежнем уровне 2,2-2,4 балла. Во всех группах отмечено улучшение качества жизни пациента, данное улучшение было стойким, т.е. сохранялось спустя 3 месяца после операции. Большая вариабельность исходного показателя качества жизни не позволила выявить статистическую достоверность пред- и послеоперационных отличий. С другой стороны, полученные данные свидетельствуют о том, что использование ВАШ лучше позволяет оценить качество жизни пациента по сравнению с индексом QoL шкалы IPSS.
Таблица 6. Динамика показателей шкалы QoL (в баллах) до операции и спустя 1 и 3 месяца после операции
| Подгруппа | До операции | Спустя 1 месяц | Спустя 3 месяца |
|---|---|---|---|
| Группа 1 (n = 93) | |||
| Подгруппа I | 4,3 ± 1,7 | 2,6 ± 1,9 | 2,3 ±1,5 |
| Подгруппа II | 4,3 ±1,7 | 2,5 ±1,8 | 2,1 ± 1,4 |
| Подгруппа III | 4,3 ±1,7 | 3 ±1,4 | 2,4 ± 1,4 |
| Группа 2 (n = 102) | |||
| Подгруппа I | 4,5 ± 1,6 | 2,4 ± 1,6 | 2,2 ± 1,2 |
| Подгруппа II | 4,5 ± 1,6 | 2,3 ± 1,5 | 2,1 ± 1 |
| Подгруппа III | 4,5 ± 1,6 | 2,6 ±1,4 | 2,3 ± 1,2 |
| Группа 3(n =36) | |||
| Подгруппа I | 4,4 ± 1,5 | 2,5 ±1,2 | 2,4 ± 1,1 |
| Подгруппа II | 4,4 ± 1,5 | 2,2 ± 1 | 2,1 ± 1 |
| Подгруппа III | 4,4 ± 1,5 | 2,6 ±1 | 2,2 ± 1 |
Динамика количества остаточной мочи приведена в таблице 7. До операции средний показатель количества остаточной мочи был от 82 мл в группе малых желез до 103- 108 мл в группах со средними и большими размерами ПЖ. Спустя 1 месяц во всех подгруппах количество мочи было клинически незначимым и варьировало от 20 до 40 мл, данные изменения сохранялись в течение всех трех месяцев послеоперационной терапии. Нами не было выявлено зависимости количества остаточной мочи от исходного объема ПЖ. Также мы не получили увеличения объема остаточной мочи во всех трех подгруппах, когда использовалась комбинированная терапия с использованием мхолиноблокатора
Таблица 7. Динамика показателей количества остаточной мочи (мл) до операции и спустя 1 и 3 месяца после операции
| Подгруппа | До операции | Спустя 1 месяц | Спустя 3 месяца |
|---|---|---|---|
| Группа 1 (п = 93) | |||
| Подгруппа I | 82 ±23 | 30 ± 10* | 22 ± 8** |
| Подгруппа II | 82 ±23 | 20 ± 12* | 18 ± 10** |
| Подгруппа III | 82 ±23 | 25 ±14* | 23 ± 10** |
| Группа 2 (п = 102) | |||
| Подгруппа I | 108 ±28 | 35 ± 12* | 25 ± 8** |
| Подгруппа II | 108 ±28 | 22 ± 12* | 20 ± 10’* |
| Подгруппа III | 108 ±28 | 25 ±14* | 24 ± 8** |
| Группа 3 (п =66) | |||
| Подгруппа I | 103 ±24 | 40 ± 14* | 27 ± 8** |
| Подгруппа II | 103 ±24 | 25 ± 12* | 23 ± 9** |
| Подгруппа III | 103 ±24 | 30 ±11* | 26 ± 8** |
Примечание: * р1-2< 0,05, ** р1-3< 0,05, *** р2-3< 0,05
Изменение максимальной объемной скорости мочеиспускания до и после операции в зависимости от исходного объема ПЖ показано в таблице 8. До операции все пациенты имели обструктивный тип кривой мочеиспускания с максимальной объемной скоростью от 6,3 мл/сек в группе больших желез до 8,9 мл/сек у пациентов с малым объемом ПЖ. Несмотря на отсутствие статистической достоверности отличий, отмечается тенденция по снижению максимальной скорости мочеиспускания при увеличении объема железы. Проведенное оперативное лечение во всех случаях приводило к выраженному возрастанию максимальной объемной скорости мочеиспускания через 1 месяц до 17,4-22,5 мл/сек и через 3 месяца – до 18,6-23 мл/сек. Во вторых и третьих подгруппах, т.е. там, где применялся тамсулозин было отмечено незначительное возрастание максимальной скорости мочеиспускания, хотя и не носящее статистически достоверных отличий.
Таблица 8. Динамика показателей максимальной объемной скорости (мл/сек) мочеиспускания до операции и спустя 1 и 3 месяца после операции
| Подгруппа | До операции | Спустя 1 месяц | Спустя 3 месяца |
|---|---|---|---|
| Группа 1 (п = 93) | |||
| Подгруппа I | 8,9 ± 1,5 | 19,7 ± 2,4* | 20,1 ±2** |
| Подгруппа II | 8,9 ± 1.5 | 21,3 ±2,5* | 21,5 ±2,1** |
| Подгруппа III | 8,9 ± 1,5 | 22,5 ± 2,5* | 23 ± 2,2** |
| Г руппа 2 (п = 102) | |||
| Подгруппа I ( | 7,7 ± 1,3 | 18,8 ± 2,3* | 19,2 ±2** |
| Подгруппа II | 7,7 ± 1,3 | 20,4 ± 2* | 20,8 ±2,1** |
| Подгруппа III | 7,7 ± 1,3 | 21,3 ±2,1* | 22,4 ± 2,3** |
| Группа 3 (п = 66) | |||
| Подгруппа | 6,3 ± 1,2 | 17,4 ±2* | 18,6 ± 1,9** |
| Подгруппа II | 6,3 ± 1,2 | 19,3 ±2,1* | 20,5 ± 2’* |
| Подгруппа III | 6,3 ± 1,2 | 20,1 ±2,2* | 21,3 ±2,1** |
Примечание: * р1-2< 0,05, ** р1-3< 0,05, *** р2-3< 0,05
Таблица 9. Динамика показателей среднего объема микции (мл) до операции и спустя 1 и 3 месяца после операции
| Подгруппа | До операции | Спустя 1 месяц | Спустя 3 месяца |
|---|---|---|---|
| Группа 1 (n = 93) | |||
| Подгруппа I | 230 ± 23 | 180 ± 25*,*** | 260 ±20 |
| Подгруппа II | 230 ± 23 | 200 ± 30 | 280 ± 20**,*** |
| Подгруппа III | 230 ± 23 | 280 ±35 | 300 ± 20** |
| Группа 2 (n = 102) | |||
| Подгруппа I | 200 ± 20 | 160 ±25 | 265 ± 20**,*** |
| Подгруппа II | 200 ± 20 | 180 ±30 | 290 ± 25**,*** |
| Подгруппа | 200 ± 20 | 260 ±30* | 305 ± 20**,*** |
| Группа 3 (п = 66) | |||
| Подгруппа I | 180 ± 15 | 140 ±20* | 250 ± 25**,*** |
| Подгруппа II | 180 ± 15 | 150 ±30 | 270 ± 20**,*** |
| Подгруппа III | 180 ± 15 | 240 ±40* | 290 ± 20**,*** |
Примечание: * р1-2< 0,05, ** р1-3< 0,05, *** р2-3< 0,05
Средний объем микции является показателем, определяющим во многом качество жизни пациента после операции, его динамика представлена в таблице 9. Средний объем микции до операции составлял 180-230 мл, т.е. был сохранен, несмотря на наличие выраженной инфравезикальной обструкции. В третьей группе предоперационные показатели количества остаточной мочи были статистически достоверно ниже, чем в первой группе. Спустя 1 месяц после операции в первой подгруппе при небольших размерах желез объем микции практически не изменился по отношению с дооперационными показателями и только к третьему месяцу статистически достоверно увеличился до 260 мл. При использовании альфа-адреноблокаторов и комбинированной терапии эти различия отличия стали носить статистически достоверный характер к третьему месяцу терапии, достигнув значений – 280 и 300 мл, соответственно.
Во второй и третьих группах были отмечены схожие тенденции: в первых подгруппах средний объем микции спустя 1 месяц уменьшался до 160 и 140 мл соответственно, а к третьему месяцу увеличивался до 265 и 250 мл. При использовании альфа-адреноблокаторов и комбинации альфа-блокатора снижение среднего объема микции через 1 месяц после операции не носило статистически достоверный характер, к третьему месяцу средний объем микции увеличивался до 290 и 270 мл. соответственно. В третьих подгруппах как при операциях на ПЖ средних размеров, так и больших размерах, средний объем микции уже к первому месяцу был статистически значимо выше как аналогичных дооперационных показателей, так и при их сравнении с показателями первых подгрупп. К третьему месяцу терапии эти изменения оставались стабильными.
ОБСУЖДЕНИЕ
Наше исследование носило проспективный, рандомизированный характер. Сроки его проведения были достаточны для определения эффективности проводимой терапии в зависимости от исходных объемов ПЖ. Выбранная когорта пациентов отражала стандартного больного с СНМП вследствие ДГПЖ и была однородной по степени тяжести симптомов, уродинамическим показателям, количеству остаточной мочи. В зависимости от размеров ПЖ и послеоперационной терапии пациенты проспективно были разделены на 9 подгрупп с одинаковым количеством пациентов в рамках каждой группы для проведения статистически корректного сравнения.
Вторым преимуществом проведенной работы была единая методика оперативного вмешательства, выполненная в одной операционной одним оперирующим врачом (А.Г. Мартов), что позволило нам исключить влияния многих дополнительных факторов на результаты исследования.
Основанием для подразделения пациентов в зависимости от характера проводимой послеоперационной терапии послужили наши предыдущие публикации по данной проблеме [4,13], предварительно показавшие эффективность дополнительного назначения альфа-адреноблокаторов в виде монотерапии, так и в виде комбинации с м-холинолитиками. Ранее мы не проводили исследования зависимости выраженности СНМП и исходного объема ПЖ, что обуславливает новизну и актуальность данной работы.
К возможным недостаткам проведенного исследования следует отнести отсутствие группы плацебоконтроля и открытый характер исследования (пациенты и исследователи были осведомленыо характере проводимого лечения). Вторым серьезным недостатком является отсутствие детализированного анализа изменений обструктивных и ирритативных симптомов в каждой группе. На основании ранее проведенных нами исследований [4,13], мы предполагали, что обструктивные жалобы должны снижаться в большей степени, а ирритативные симптомы в меньшей. Еще одним возможным недостатком является отсутствие выполнения цистометрии наполнения у пациентов до- и после операции, что не позволяет установить состояниефункции детрузора. Однако на основании предоперационных данных (объем микции, количество остаточной мочи, данные урофлоуметрии) и имеющихся сведений из литературных источников, можно говорить о сохранной функции детрузора у пациентов в нашем исследовании. Пациенты с подозрением на исходно компрометированную функцию детрузора были исключены из исследования на этапе включения в исследование.
Оценка качества жизни пациентов до и после операции показала, что показатель ВАШ лучше отражает изменения самочувствия пациентов по сравнению с использованием индекса качества жизни QoL.
Анализ оценки ВАШ показал, что проводимое оперативное лечение улучшает качество жизни пациентов вне зависимости от исходных размеров ПЖ, однако, чем больше размер железы, тем хуже были исходные показатели качества жизни пациентов. Улучшение показателя качества жизни имело схожие тенденции для всех размеров ПЖ. При дополнительном назначении комбинированной терапии показатели ВАШ достигли пиковых показателей и оставались стабильными на протяжении всего исследования. Данные визуальной аналоговой шкалы в первых подгруппах, т.е. у пациентов, получавших только антибактериальную и противовоспалительную терапию, не достигли тех показателей в абсолютных цифрах, которые были определены в подгруппах комбинированной терапии.
Значения показателей оценки симптомов нижних мочевых путей по шкале IPSS в зависимости от исходного объема ПЖ носили прямо пропорциональный характер, т.е. чем больше был объем железы, тем более высокие показатели IPSS были у пациентов, несмотря на считающуюся независимость данных значений. Тем не менее, во всех трех группах пациенты отмечалиСНМП сильной степени выраженности. Интересным представляется факт, что спустя 1 и 3 месяца после операции во всех подгруппах пациентов ни в одном случае уровень симптомов не снизился ниже 8, чтобы соответствовать уровню симптомов слабой степени выраженности, когда показано лишь динамическое наблюдение.
Проводимая дополнительно медикаментозная терапия как альфаадреноблокаторами, так и комбинированное назначение м-холинолитиков и альфа-адреноблокаторов, приводила к снижению абсолютных признаков СНМП, однако ни в одном из межгрупповых сравнений не было продемонстрировано статистически достоверных отличий. Данный феномен уже изучался нами в предыдущей публикации по данному вопросу и связан по-видимому с тем, что оценка симптомов IPSS проводилась нами в целом, без разделения на обструктивные и ирритативные [14]. При детализированной оценке симптомов нами ранее было получено свидетельство того, что сумма обструктивных симптомов одинакова во всех группах, так как операция хорошо устраняет обструктивную симптоматику. Отличия в сумме ирритативных симптомов носили статистически достоверный характер и были максимально выраженыпри использовании комбинированной терапии после операции.
Важным обоснованием целесообразности дополнительного назначения тех или иных препаратов после операции является не только улучшение объективных симптомов, но и их положительное влияния на объективные показатели, такие как средний объем микции, что косвенно определяет и частоту мочеиспускания днем и ночью, уродинамические показатели [14]. В нашем исследовании не было выявлено влияния проводимой комбинированной терапии на количество остаточной мочи у пациентов после операции, во всех случаях не было статистически значимых отличий. Схожие тенденции были и при оценке максимальной объемной скорости мочеиспускания, однако при использовании альфа-адреноблокаторов и комбинированной терапии во всех подгруппах были получены лучшие показатели в абсолютных цифрах, без статистически достоверных межгрупповых отличий.
Главным преимуществом комбинированной терапии после операций на ПЖ является статистически значимое увеличение среднего объема микции, что также продемонстрировано и при монотерапии альфа-адреноблокаторами. Небезынтересной представляется выявленная закономерность, заключающаяся в уменьшении среднего объема микции спустя 1 месяц в первых подгруппах всех групп. Т.е. появление временной нестабильности мочевого пузыря в результате проведенного лечения является одним из результатов оперативного лечения. Только комбинированная терапия, но не монотерапия альфа-адреноблокаторами, позволяет увеличить данный показатель по сравнению с предоперационными показателями. Данное влияние не зависит от исходных размеров ПЖ.
В результате проведенного исследования была выявлена большая эффективность комбинированной терапии по сравнению со стандартным лечением послеоперационных расстройств мочеиспускания у мужчин после оперативного лечения ДГПЖ. Большая эффективность терапии заключается в комбинированном воздействии на детрузор и шейку мочевого пузыря. Данная терапия, по нашему мнению, должна являться непременной частью социальной реабилитации пациента после операции. Комбинированная терапия тамсулозином 0,4 мг с модифицированным высвобождением и солифенацином 6 мг показала свою целесообразность при всех объемах ПЖ.
Обоснованием проведения комбинированной терапии альфа-адреноблокаторами и М-холиноблокаторами у пациентов после операций по поводу ДГПЖ является сложный механизм развития послеоперационных расстройств мочеиспускания. Развитие ирритативных жалоб возможно связано с тем, что послеоперационная рана располагается ниже шейки мочевого пузыря, и после выполнения операции попадающая на раневую поверхность моча, является триггером для сокращения детрузора на фоне небольшого наполнения мочевого пузыря [15]. Данные симптомы развиваются у подавляющего большинства пациентов после операции независимо от наличия гиперактивности мочевого пузыря до операции. При подозрении на наличие гиперактивности детрузора до операции оправдано предоперационное использование комбинированной терапии. По данным диссертации М.Р. Тангриберганова результатылечения описанных выше симптомов гиперактивного мочевого пузыря на фоне ДГПЖ в два раза лучше с использованием М-холиноблокаторов по сравнению с предоперационной терапией альфа-адреноблокаторами. В течение месяца по мере заживления послеоперационной раныданные явления стихают, однако размер послеоперационной раны имеет значение и назначение комбинированной терапии альфа-адреноблокаторами и М-холиноблокаторами позволяет улучшить качество жизни подобных пациентов [17].
Важным обоснованием целесообразности проведения комбинированной терапии является свидетельства выявления гиперактивности детрузора, имеющиеся почти у 47% пациентов до и после операций на ПЖ. По данным З.К. Гаджиевой [18] наиболее частымиформами являются гиперактивность и низкий комплаенс детрузора. Таким образом, применение комбинированной терапии обосновано еще и патогенетически. В нашей работе мы показали ее эффективность при разных объемах ПЖ и сроки ее использования в течение трех месяцев, хотя в отдельных случаях целесообразно и более длительное ее проведение. Мы не проводили изучение дальнейшей динамики СНМП у пациентов, однако очевидна ее польза при персистировании симптомов нижних мочевых путей средней степени выраженности.
ЗАКЛЮЧЕНИЕ
Наше исследование показало, что назначение комбинированной терапии после трансуретральных операций на ПЖ позволяет уже с первого месяца после операции достичь субъективного улучшения симптомов вне зависимости от исходного объема ПЖ. Объективное улучшение достигается за счет раннего увеличения среднего объема мочеиспускания по сравнению с назначением стандартной послеоперационной терапии. В процессе комбинированной терапии нами не было отмечено ни нарастания остаточной мочи, ни влияния на максимальную скорость мочеиспускания. На основании проведенного исследования мы считаем целесообразным назначение комбинированной терапии в послеоперационном периоде на срок 3 месяца от момента операции.
ЛИТЕРАТУРА
- Roberts RO, Jacobsen SJ, Jacobson DJ, Reilly WT, Talley NJ, Lieber MM. Natural history of prostatism: high American urological association symptom scores among community-dwelling men and women with urinary incontinence. Urology 1998;51(2):213–219.
- Wasson JH, Reda DJ, Bruskewitz RC, Elinson J, Keller AM, Henderson WG. A comparison of transurethralsurgerywithwatchfulwaiting for moderate symptoms of benign prostatic hyperplasia. The Veterans Affairs Cooperative Study Group on transurethral resection of the prostate. N Engl J Med 1995;332(2):75–79. doi: 10.1056/NEJM199501123320202
- Han HH, Ko WJ, Yoo TK, Oh TH, Kim DY, Kwon DD, et al. Factors associated with continuing medical therapy aer transurethral resection of prostate. Urology 2014; 84(3):675–680. doi: 10.1016/j.urology.2014.04.027.
- Мартов А.Г., Гущин Б.Л., Ергаков Д.В., Ощепков В.Н. Улучшение результатов оперативного лечения больных с доброкачественной гиперплазией предстательной железы посредством применения альфа1-адреноблокаторов в послеоперационном периоде. Урология 2002;( 5):23-37.
- Rassweiler J, Teber D, Kuntz R, Hofmann R. Complications of transurethral r esection of the prostate (TURP) – incidence, management, and prevention. Eur Urol 2006;50(5):969–980. doi: 10.1016/j.eururo.2005.12.042
- Athanasopoulos A, Chapple C, Fowler C, Gratzke C, Kaplan S, Stief C, Tubaro A. The role of antimuscarinicsin the management of men with symptoms of overactive bladder associated with concomitant bladder outlet obstruction: an update. Eur Urol 2011;60(1):94–105. doi: 10.1016/j.eururo.2011.03.054.
- Gravas S, Bach T, BachmannA, Drake M, Gacci M, GratzkeC. et al. Management of Non-Neurogenic Male Lower Urinary Tract Symptoms (LUTS), incl. Benign Prostatic Obstruction (BPO). URL: http://www.uroweb.org/guideline/treatment-of-non-neurogenic-male-luts/.
- Coyne KS, Sexton CC, Thompson CL et al. The prevalence of lower urinary tract symptoms (LUTS) in the USA, the UK and Sweden: results from the Epidemiology of LUTS (EpiLUTS) study. BJU Int 2009;104(3):352-60. doi: 10.1111/j.1464-410X.2009.08427.x
- Kang YJ, Kim KH, Seo Y, Lee KS. Effect of transurethralresection of the prostate on storage symptoms in patients with benign prostatic hyperplasia of less than 30 ml. World J Mens Health 2013;31(1):64–9. doi: 10.5534/wjmh.2013.31.1.
- Chapple CR, Smith D. The pathophysiological changes in the bladder obstructed by benign prostatic hyperplasia. Br J Urol 1994;73(2):117–123.
- Li MC, Wang ZY, Yang J, Guo XL, Wang T1, Wang SG, et al. Efficacy and safety ofsolifenacin plustamsulosin oral controlled absorption system in menwith lower urinary tract symptoms: a meta-analysis. Asian J Androl 2015;17(1): 124–134. doi: 10.4103/1008-682X.137685.
- Hao N, Tian Y, Liu W, Wazir R, Wang J, Liu L, et al.Antimuscarinics and alphablockers or alpha-blockers monotherapy on lower urinary tract symptoms – a metaanalysis. Urology 2014;83:556–62. doi: 10.1016/j.urology.2013.10.034
- Ергаков Д.В., Мартов А.Г.. Комбинированная терапия расстройств мочеиспускания после трансуретральной резекции предстательной железы. Урология. 2018;(1):62-70.
- Johnson TM 2nd, Markland AD, Goode PS, Vaughan CP, Colli JL, Ouslander JG, et al. Efficacy of adding behavioural treatment or antimuscarinic drug therapy to alpha-blocker therapy in men with nocturia. BJU Int 2013;112:100–108. doi: 10.1111/j.1464-410X.2012.11736.x.
- Kaplan SA, Roehrborn CG, Abrams P, Chapple CR, Bavendam T, Guan Z. Antimuscarinics for treatment of storage lower urinary tract symptoms in men: a systematic review. Int J Clin Pract 2011;65(4):487–507. doi: 10.1111/j.1742-1241.2010.02611.x.
- Xin Z, Huang Y, Lu J, Zhang Q, Chen C. Addition of antimuscarinics to alphablockers for treatment of lower urinary tract symptoms in men: a meta-analysis. Urology 2013;82(2):270–7. doi: 10.1016/j.urology.2013.04.045.
- Тангриберганов М.Р. Особенности лечения доброкачественной гиперплазии предстательной железы в сочетании с клиническими симптомами гиперактивного мочевого пузыря. Автореф. дисс. … к.м.н. Москва, 2012. 25 c.
- Гаджиева З.К. Уродинамические методы исследования в диагностике и лечении нарушений мочеиспускания: Дисс. … д.м.н., Москва, 2009. 374 с
Статья опубликована в журнале "Экспериментальная и клиническая урология" №2 2019 г., стр. 70-79









Комментарии