Бессимптомная бактериурия: междисциплинарный обзор доказательной базы
Автор обзора: Шадеркина В.А., уролог, CEO Uroweb.ru
План обзора
- 1. От эрадикации к комменсализму
- 2. Диагностика и верификация ББ
- 3. Микробиологический пейзаж и протективные штаммы
- 4. Эпидемиология в особых популяциях
- 5. Ситуации, требующие терапии
- 6. Канефрон Н: Фармакологическая модуляция и профилактика
- 7. Стратегии в управлении ББ
- 8. Скрининг бессимптомной бактериурии
- Таблица 4. Сводная таблица на основании протоколов EAU 2025, IDSA и USPSTF ((United States Preventive Services Task Force)) по скринингу ББ
- 9. Сравнительный анализ российских и международных гайдлайнов
- 10. Заключение
1. От эрадикации к комменсализму
Бессимптомная бактериурия (ББ) определяется как присутствие одного или нескольких видов бактерий в моче в диагностически значимом количестве при полном отсутствии клинических признаков и симптомов, характерных для инфекции мочевыводящих путей (ИМП), таких как дизурия, поллакиурия или боли в надлобковой области [1, 2].
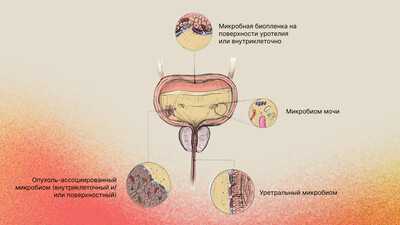
В последние пять лет в урологии и терапии произошел фундаментальный сдвиг в понимании микробиологии мочи. Традиционный взгляд на мочу как на стерильную среду был опровергнут открытием мочевого микробиома. Бессимптомная бактериурия теперь рассматривается не как патология, требующая обязательного лечения, а как форма комменсальной колонизации, которая во многих случаях защищает макроорганизм от инвазии вирулентных патогенов [1, 2, 3].
Глобальные данные подтверждают, что необоснованное назначение антибиотиков при ББ является мощным драйвером селекции полирезистентных штаммов и повышает риск развития тяжелых побочных эффектов, включая инфекцию Clostridioides difficile [2, 4–6].
2. Диагностика и верификация ББ
Согласно критериям EAU (2025) и IDSA, для постановки диагноза ББ необходимо наличие бактерий в моче в значимом титре при полном отсутствии симптомов, которые можно было бы отнести к инфекции мочевыводящих путей (ИМП) [1, 2].
2.1. Количественные показатели
- Женщины. Выделение одного и того же штамма бактерий в титре 105 КОЕ/мл и более в двух последовательных пробах мочи (интервал до 2 недель) [1].
- Мужчины. Однократное выделение одного вида бактерий в титре 105 и более КОЕ/мл в одной пробе средней порции мочи [1].
- Катетеризированные пациенты. Титр 102 и более КОЕ/мл в образце, полученном путем асептической пункции или прямой катетеризации [1].
Наличие пиурии (лейкоцитурии) при отсутствии симптомов не является поводом для изменения диагноза на «симптоматическую ИМП» и не служит показанием к антибиотикотерапии [7, 8].
Диагностические критерии ББ строго стандартизированы, чтобы отделить истинную бактериурию от контаминации образца мочи.
2.2. Интервал между сбором образцов
Интервал между сбором образцов не должен превышать 14 дней. При получении мочи путем катетеризации мочевого пузыря диагностически значимым считается титр ≥102 КОЕ/мл в однократно взятом образце.
2.3. Особый случай — стрептококк группы B
Для стрептококка группы B (Streptococcus agalactiae, СГВ) установлен более низкий диагностический порог. Бактериурия, вызванная СГВ, в титре ≥104 КОЕ/мл в одном образце мочи считается клинически значимой. Такой подход обусловлен тем, что бактериурия СГВ является маркером массивной колонизации влагалища и прямой кишки. Это, в свою очередь, является основным фактором риска развития у беременных неонатального сепсиса с ранним началом. Таким образом, диагностический критерий в данном случае является инструментом стратификации не урологического, а неонатального риска, что требует обязательного проведения интранатальной антибиотикопрофилактики.
3. Микробиологический пейзаж и протективные штаммы
Escherichia coli остается доминирующим изолятом (55–75%) [1]. Согласно российскому многоцентровому исследованию RESOURCE-2 (2022–2024), структура возбудителей в РФ совпадает с мировыми трендами – E. coli выявляется у 69,5% женщин с колонизацией мочевых путей [9].
Штаммы E. coli, вызывающие ББ, часто характеризуются редуктивной эволюцией — утратой генов вирулентности. Исследования штамма E. coli 83972 показали, что такая колонизация может предотвращать инфицирование более агрессивными уропатогенными штаммами (UPEC) за счет конкуренции за нутриенты и места адгезии на уротелии [11, 12].
4. Эпидемиология в особых популяциях
Распространенность ББ коррелирует с возрастом и сопутствующей патологией.
4.1. Сахарный диабет
Частота ББ у пациентов с диабетом составляет 12,2% (против 4,5% в контроле), достигая 27% у женщин. Риск развития ББ напрямую зависит от длительности заболевания и наличия автономной нейропатии мочевого пузыря [13, 14].
4.2 Пожилой возраст
В домах престарелых ББ выявляется у 25–50% женщин и 15–35% мужчин [15]. Исследования 2024 года подтверждают, что у этой категории пациентов наличие ББ не влияет на выживаемость и не должно лечиться антибиотиками даже при неспецифических симптомах, таких как падения или спутанность сознания [16].
4.3 Реципиенты почечного трансплантата
У реципиентов почечного трансплантата лечение бессимптомной бактериурии за пределами раннего послеоперационного периода не демонстрирует клинической пользы. Современные метаанализы 2023–2024 гг. показали, что антибактериальная терапия ББ не снижает риск острого отторжения, утраты трансплантата, ухудшения функции почечного аллотрансплантата или летальности в течение первого года после трансплантации. При этом рандомизированные контролируемые исследования у пациентов ≥2 месяцев после трансплантации убедительно продемонстрировали, что назначение антибиотиков при ББ ассоциировано с достоверным увеличением частоты последующих эпизодов бактериурии, вызванных антибиотикорезистентными, в том числе клинически значимыми мультирезистентными, уропатогенами, без снижения риска симптомной инфекции мочевых путей. Таким образом, рутинная стратегия «screen-and-treat» ББ у стабильных реципиентов почечного трансплантата должна рассматриваться как фактор антимикробного ущерба, а не как средство улучшения трансплантационных исходов [17-19].
5. Ситуации, требующие терапии
Клинические рекомендации 2024–2025 гг. ограничивают круг пациентов для обязательного лечения ББ двумя группами.
5.1. Беременные женщины
5.1.1. Распространенность
ББ у беременных варьирует в широких пределах, что зависит от географических, социально-экономических и демографических факторов.
- В развитых странах: В популяциях Европы и Северной Америки распространенность ББ составляет от 2% до 10% [20].
- Российские данные в целом соответствуют этим показателям, составляя в среднем 5–6% [21]. В большинстве случаев ББ выявляется уже в первом триместре беременности (до 75% случаев) и реже – во II и III триместрах беременности (в 25%). [22].
- В развивающихся странах: Наблюдается значительно более высокая распространенность. Исследования в странах Азии и Африки демонстрируют показатели от 15% до 25%, а в отдельных локальных отчетах, например из Нигерии, — до 86% [23, 24].
Эта выраженная разница ставит под сомнение универсальную применимость клинических рекомендаций, разработанных на основе данных из популяций с низкой распространенностью. Соотношение пользы и вреда от универсального скрининга, рассчитанное для западных стран, может быть совершенно иным в регионах с высокой эндемичностью, где абсолютная польза от предотвращения осложнений может быть значительно выше.
5.1.2. Диагностика ББ у беременных
ББ является фактором риска гестационного пиелонефрита (до 2% случаев), преждевременных родов и низкой массы плода [25, 26]. USPSTF (2024) сохраняет рекомендацию (Grade B) по обязательному скринингу ББ при первом визите в женскую консультацию (табл. 1) [27].
Таблица 1. Диагностические критерии бессимптомной бактериурии у беременных
| Метод сбора мочи | Критерии для большинства уропатогенов | Критерии для Стрептококка группы B (СГВ) | Источники рекомендаций |
|---|---|---|---|
| Средняя порция мочи («clean-catch») | ≥105 КОЕ/мл одного и того же возбудителя в двух последовательных пробах | ≥104 КОЕ/мл в одной пробе | IDSA, ACOG, КР Минздрава РФ |
| Катетеризация мочевого пузыря | ≥102 КОЕ/мл в одной пробе | Не стандартизировано, применяется общий порог | IDSA |
5.1.3. Цели терапии ББ у беременных и доказательная база
Эффективность антибактериальной терапии бессимптомной бактериурии у беременных подтверждена рандомизированными исследованиями и метаанализами, демонстрирующими достоверное снижение риска острого пиелонефрита на 70–80%, а также благоприятное влияние на акушерские исходы (табл. 2).
Табл. 2. Цели терапии ББ у беременных
| Исследование / источник | Дизайн и популяция | Основные эффекты терапии ББ | Ключевые выводы |
|---|---|---|---|
| Kass EH, 1960 [28] | Проспективное наблюдательное исследование; беременные с ББ | Без лечения: пиелонефрит у ~30–40% | Впервые доказана клиническая значимость ББ у беременных |
| Smaill F, Vazquez JC. Cochrane Review, 2019 (обновление) [29] | Систематический обзор и метаанализ РКИ; >2000 беременных | ↓ риск пиелонефрита на 70–80%; ↓ преждевременных родов | Лечение ББ эффективно и оправдано |
| Nicolle LE et al., IDSA 2019 [30] | Гайдлайн, анализ РКИ и когорт | Значимое снижение пиелонефрита; польза превышает риск АБТ | Беременные — единственная группа, где лечение ББ обязательно |
| EAU Guidelines on Urological Infections, 2024 [1] | Систематический анализ доказательств | ↓ пиелонефрита; ↓ госпитализаций | Рекомендован скрининг и лечение ББ при беременности |
| ACOG Practice Bulletin, 2023 [31] | Экспертный консенсус + систематический обзор | ↓ пиелонефрита, ↓ акушерских осложнений | Скрининг + лечение ББ — стандарт акушерской помощи |
| WHO Recommendations on Antenatal Care, 2016 (актуализированы) [32] | Глобальные данные, метаанализы | Улучшение материнских и перинатальных исходов | Рекомендовано лечение подтверждённой ББ |
| Hill JB et al., 2005 [33] | РКИ, беременные с ББ | ↓ пиелонефрита с 24% до 3% | Подтверждена эффективность АБТ |
5.1.4. Терапия ББ у беременных
Бессимптомная бактериурия при беременности является единственной «классической» ситуацией, когда скрининг и лечение бактериурии без симптомов рекомендованы. Это связано с тем, что антибактериальная терапия у беременных с ББ снижает риск острого пиелонефрита и может уменьшать риск неблагоприятных акушерских исходов (преждевременные роды, низкая масса тела новорождённого) несмотря на то, что качество доказательств по перинатальным исходам оценивается как низкое/умеренное из-за «старости» большинства РКИ. EAU также указывает, что лечение ББ у беременных по данным метаанализа приносит пользу, хотя подчёркивает, что большинство исследований — старые.
При выявлении ББ необходимо назначить антибиотикотерапию 4–7 дней (предпочитая наиболее короткий эффективный курс конкретного препарата). При этом доказательств, чтобы рекомендовать повторный рутинный скрининг при отрицательном исходном посеве или обязательный повторный скрининг после лечения, недостаточно (вопрос остаётся на усмотрение клинициста/локальных протоколов).
Принципы рационального использования антибиотиков полностью применимы и к ведению беременных с ББ. Однако здесь они имеют свою специфику. Если в общей популяции рациональная терапия означает отказ от лечения ББ, то у беременных этот принцип трансформируется в задачу «лечить правильно» (табл. 3).
Табл. 3. Лечение ББ у беременных
| Препарат | Стандартная дозировка | Длительность | Триместр-ограничения | Основные противопоказания / ограничения | Контрольный посев |
|---|---|---|---|---|---|
| Нитрофурантоин | 100 мг 2 р/сут (MR) или 50 мг 4 р/сут | 5–7 дней | ✔ I–II триместр ⚠ Избегать в конце III триместра / перед родами | Дефицит G6PD; eGFR <30 мл/мин; риск неонатального гемолиза при приёме «на сроке» | Рекомендуется через 1–2 недели после лечения |
| Амоксициллин | 500 мг 3 р/сут | 5–7 дней | ✔ Все триместры | Только при подтверждённой чувствительности (высокая резистентность E. coli); аллергия к β-лактамам | Рекомендуется |
| Амоксициллин/клавуланат | 500/125 мг 3 р/сут | 5–7 дней | ✔ Все триместры | Аллергия к β-лактамам; риск антибиотик-ассоциированной диареи | Рекомендуется |
| Цефалексин | 500 мг 2 р/сут | 5–7 дней | ✔ Все триместры | Аллергия на цефалоспорины (относительная) | Рекомендуется |
| Цефуроксим аксетил | 250–500 мг 2 р/сут | 5–7 дней | ✔ Все триместры | Аллергия к β-лактамам | Рекомендуется |
| Фосфомицин трометамол | 3 г однократно (per os) | 1 доза | ✔ Все триместры | Ограниченные данные при повторных курсах; не для пиелонефрита | Желателен (через 1–2 недели) |
| Триметоприм/сульфаметоксазол | 160/800 мг 2 р/сут | 3–5 дней | ❌ I триместр (антагонизм фолатам) ⚠ III триместр (риск гипербили-рубинемии) | Дефицит G6PD; гипербили-рубинемия плода; фолатный дефицит | Рекомендуется (если применён вынужденно) |
| Фторхинолоны | — | — | ❌ Запрещены | Токсичность для хрящевой ткани плода | ❌ Не применяются |
| Тетрациклины | — | — | ❌ Запрещены | Нарушение формирования костей и зубов плода | ❌ Не применяются |
Это подразумевает:
- Строгое соблюдение диагностических критериев. Лечение назначается только после подтверждения диагноза двумя положительными посевами (для большинства патогенов), чтобы избежать необоснованной терапии при контаминации образца.
- Выбор препарата с узким спектром. По возможности следует отдавать предпочтение препаратам с узким спектром действия (например, нитрофурантоин), а не цефалоспоринам широкого спектра.
- Использование кратчайших эффективных курсов. Придерживаться рекомендованной длительности терапии 4–7 дней, избегая необоснованного продления курсов.
- Опора на микробиологические данные. Эмпирическая терапия должна быть как можно скорее переведена в этиотропную на основании результатов посева и антибиотикограммы.
При подтверждённой бессимптомной бактериурии у беременных показана антибактериальная терапия препаратами с доказанной безопасностью для плода (фосфомицин, нитрофурантоин, β-лактамы) с последующим контрольным посевом мочи через 1–2 недели после лечения.
5.2. Пациенты перед инвазивными урологическими операциями
Если ожидается травматизация слизистой (например, ТУР простаты), эрадикация бактерий обязательна для профилактики уросепсиса [1, 2, 34, 35].
6. Канефрон Н: Фармакологическая модуляция и профилактика
В условиях необходимости сокращения антибиотикотерапии, препарат Канефрон Н (BNO 1045) выступает в качестве научно обоснованной альтернативы для управления здоровьем мочевыводящих путей.
6.1. Молекулярные механизмы (данные 2024–2025 гг.)
Исследование Milosevic et al. (2024) раскрыло новые мишени действия препарата [36]:
6.1.1. Блокада оси IKK-NF-кB
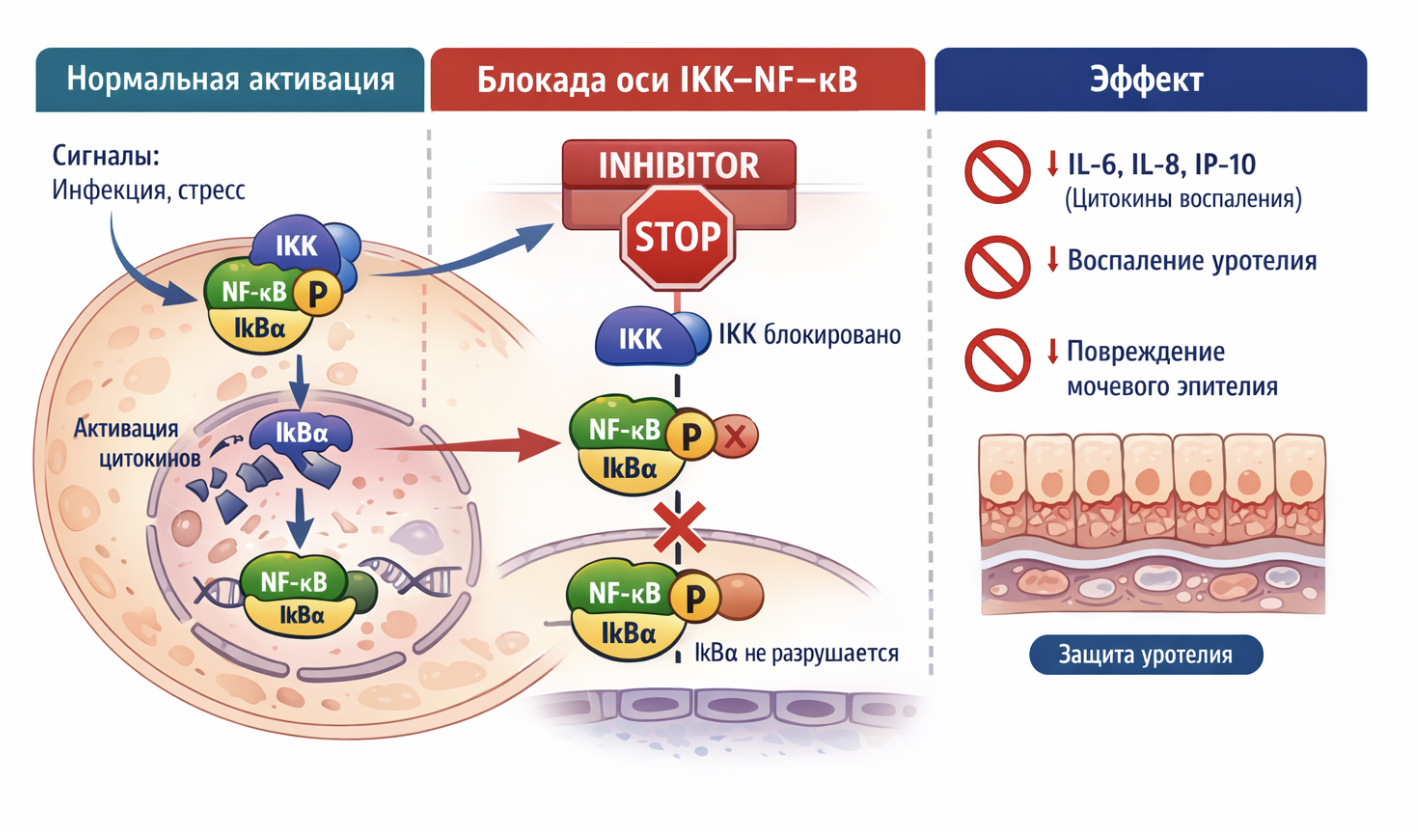
Препарат предотвращает фосфорилирование и деградацию белка ядерного фактора усилителя гена легкого полипептида каппа в ингибиторе В-клеток альфа (IκBα), блокируя транслокацию p65 в ядро. Это ведет к подавлению синтеза провоспалительных цитокинов (IL-6, IL-8, IP-10), уменьшая повреждение уротелия (рис. 1).
Рис. 1. Блокада оси IKK–NF-κB
6.1.2. Защита оси p38-MK2-RIPK1
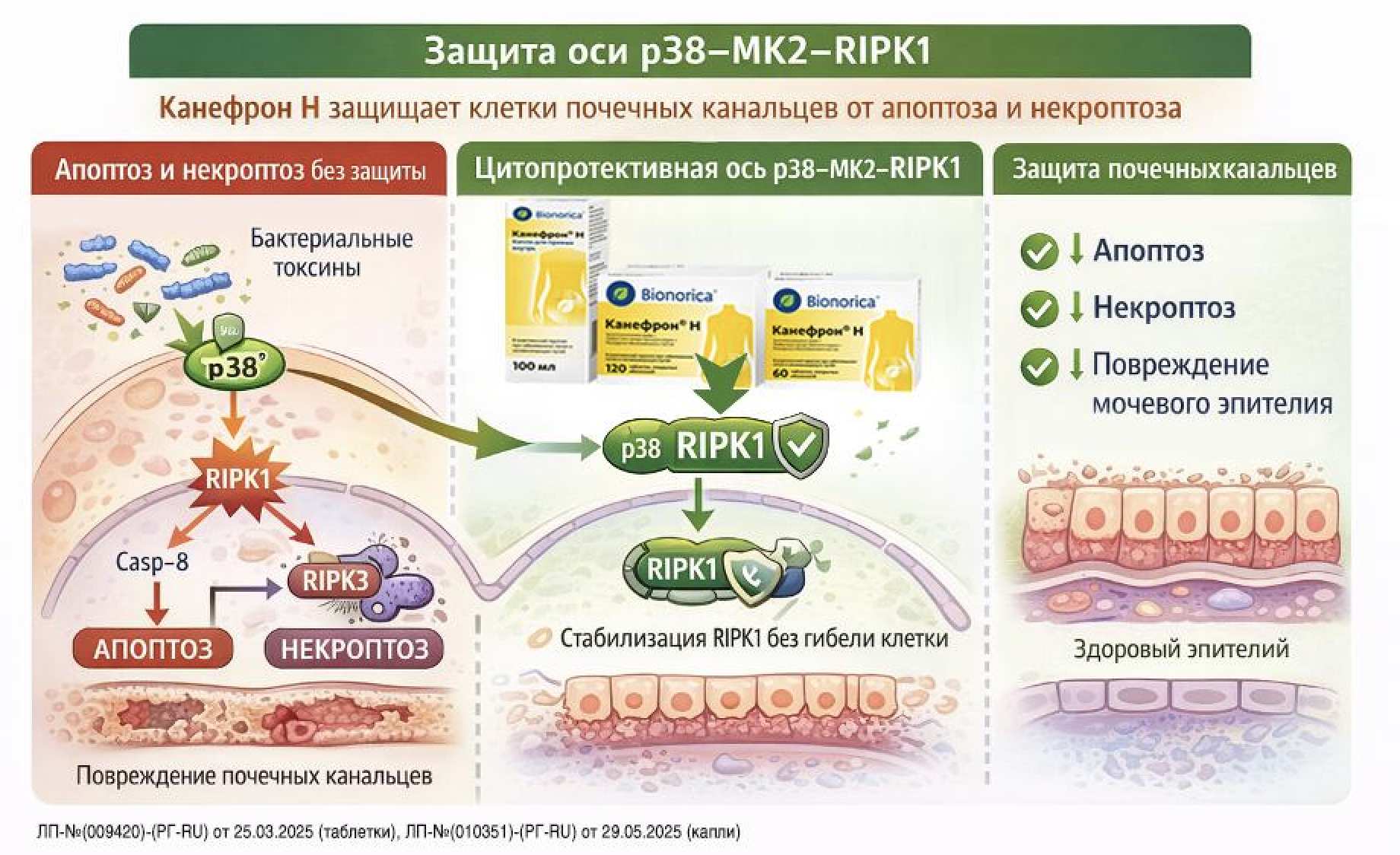
Активация цитопротективной оси p38–MK2–RIPK1 способствует предотвращению апоптоза и некроптоза эпителиальных клеток почечных канальцев в условиях бактериального стресса, обеспечивая сохранение тубулоинтерстициальной целостности.
Канефрон Н активирует цитопротективный сигнальный путь, блокируя запуск апоптоза и некроптоза клеток почечных канальцев в ответ на бактериальные токсины (рис. 2).
Рис. 2. Защита оси p38-MK2-RIPK1
6.1.3. Антиадгезивный эффект
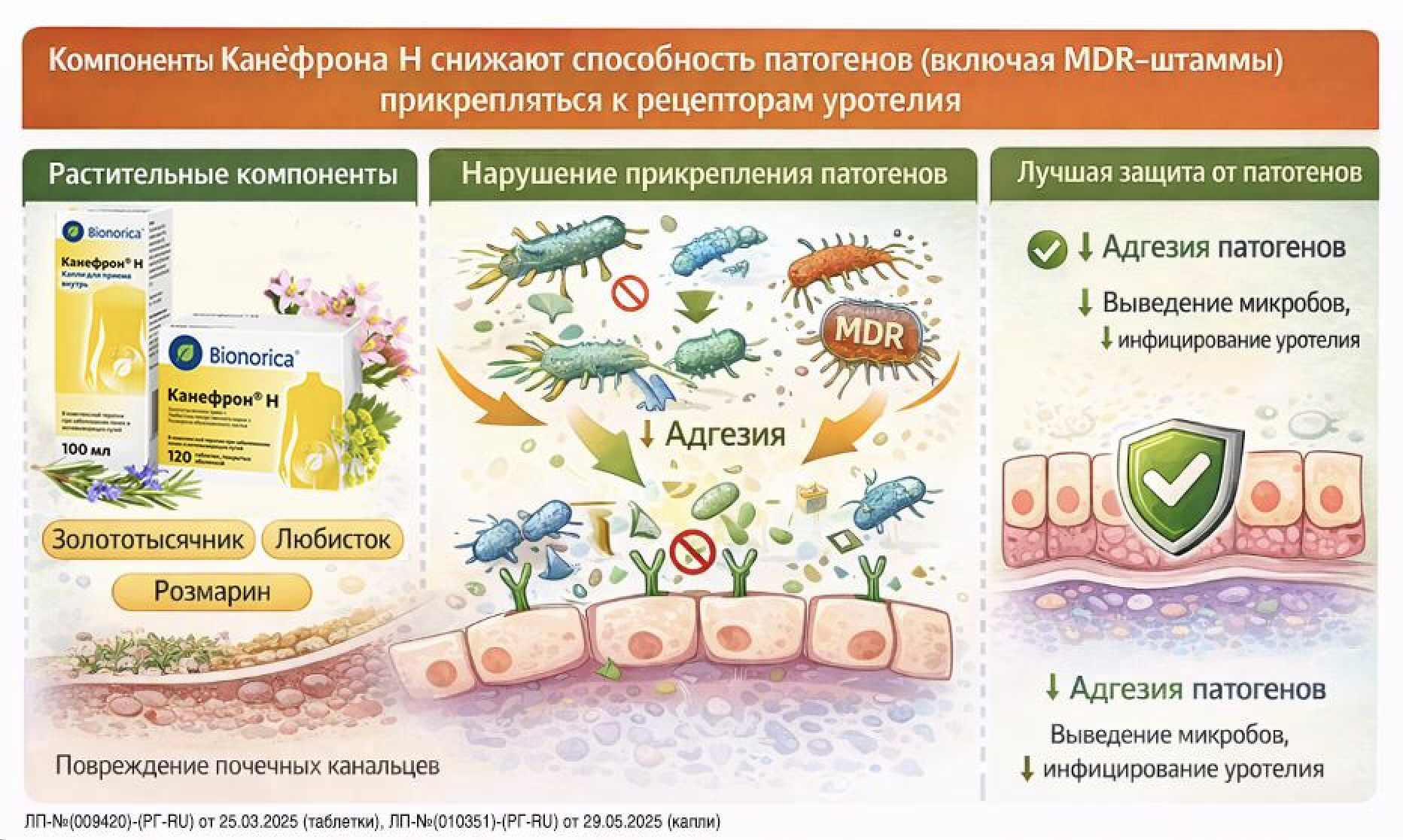
Компоненты препарата Канефрон Н снижают способность патогенов (включая MDR-штаммы) прикрепляться к рецепторам уротелия (рис. 3).
Рис. 3. Антиадгезивный эффект Канефрона Н.
6.2. Клиническая эффективность
Беременные с ББ
Ретроспективный анализ терапии ББ у 60 беременных женщин показал, что Канефрон Н не уступал антибиотикам по эффективности предотвращения симптомных инфекций, при этом частота рецидивов бессимптомной бактериурии была в 5 раз ниже в группе фитотерапии (10,7% против 53,1%, p=0,0006) [37].
Профилактика рецидивов
В российском многоцентровом исследовании добавление Канефрона Н к схеме лечения острого цистита снизило частоту рецидивов ИМП более чем в 2,5 раза через 12 месяцев (13,9% против 38,7%) [38].
Данные реальной клинической практики/real world data (IQVIA)
Анализ базы данных, включавший 160 000 амбулаторных пациентов с острым циститом в Германии подтвердил снижение риска повторных эпизодов при приеме Канефрона на 39% по сравнению со стандартной антибиотикотерапией [38, 39].
7. Стратегии в управлении ББ
Исследования 2024–2025 гг. в отделениях экстренной помощи (ED) показали, что внедрение образовательных программ для врачей и пациентов позволяет снизить потребность в антибиотиках [40]. После внедрения программы по обучению персонала экстренных отделений с ежедневным аудитом/обратной связью потребление антибиотиков снизилось: цефалоспоринов – на 21%, карбапенемов – на 24%, при этом клинические исходы не ухудшились [40].
В рандомизированном он-лайн исследовании взрослые лица 65 лет и старше, прочитав разработанный образовательный буклет, стали более комфортно относиться к отказу от антибиотиков в ситуации бессимптомной бактериурии по сравнению с теми, кто буклет не получал. Исследование измеряло готовность избегать прием антибиотиков без клинических показаний, возникающую после прочтения буклета, а также знание о ИМП/ББ. В результате было показано, что у людей, ознакомившихся с буклетом, снижалась склонность к необоснованному употреблению антибиотиков и улучшались знания о вышеперечисленных заболеваниях [41].
8. Скрининг бессимптомной бактериурии
Скрининг ББ является одной из наиболее обсуждаемых тем в современной урологии и инфектологии, так как рекомендации за последние годы существенно изменились в сторону ограничения использования антибиотиков (табл. 4).
Табл. 4. Сводная таблица на основании протоколов EAU 2025, IDSA и USPSTF ((United States Preventive Services Task Force)) по скринингу ББ.
| Группа пациентов | Рекомендация по скринингу | Уровень доказательности | Обоснование и тактика |
|---|---|---|---|
| Беременные женщины | Обязателен | Высокий(Grade A/1A) | Снижение риска пиелонефрита у матери и преждевременных родов. Скрининг на 12–16 неделе. |
| Перед инвазивными урологическими процедурами | Обязателен | Высокий(Grade A/1A) | Снижение риска уросепсиса. Проводится за 7–10 дней до вмешательства (с нарушением слизистой). |
| Пациенты с сахарным диабетом | Не рекомендуется | Высокий (Strong) | Лечение не снижает риск осложнений и не улучшает гликемический контроль. |
| Женщины в постменопаузе | Не рекомендуется | Высокий (Strong) | Терапия не влияет на частоту последующих симптоматических ИМП. |
| Пожилые люди (в т.ч. в стационарах) | Не рекомендуется | Высокий (Strong) | Высокая распространенность ББ; антибиотики повышают риск Cl. difficile и резистентности. |
| Пациенты с травмой спинного мозга | Не рекомендуется | Средний | Хроническая колонизация неизбежна; лечение не снижает риски. |
| Пациенты с катетером (длительным) | Не рекомендуется | Высокий | Лечение не предотвращает лихорадку, но вызывает селекцию резистентных штаммов. |
| Перед операцией по эндопротезированию суставов | Не рекомендуется | Средний | Современные мета-анализы не подтвердили связь ББ с инфекцией протеза. |
| Пациенты после трансплантации почки | Не рекомендуется | Низкий/Средний | После 1–2 месяцев после операции скрининг и лечение ББ обычно не требуются (согласно EAU 2024/25). |
9. Сравнительный анализ российских и международных гайдлайнов
Российские клинические рекомендации («Инфекция мочевых путей при беременности» 2025, «Цистит у женщин» 2024) полностью гармонизированы с EAU и IDSA [1, 2, 4]. Растительные препараты на основе золототысячника, любистока и розмарина (Канефрон Н) официально включены в российские протоколы как средства для лечения и профилактики рецидивирующих инфекций [4].
10. Заключение
Ведение бессимптомной бактериурии в 2025 году требует осознанного ухода от агрессивной антибиотикотерапии.
Внедрение стандартизированной фитотерапии (Канефрон Н) позволяет эффективно контролировать состояние мочевыводящих путей, снижать риск рецидивов и сохранять защитный микробиом, что является ключевым элементом современного подхода к здоровью пациента.
Литература
- EAU Guidelines on Urological Infections, https://uroweb.org/guidelines/urological-infections/chapter/the-guideline
- Lindsay E Nicolle, Kalpana Gupta, Suzanne F Bradley, Richard Colgan, Gregory P DeMuri, Dimitri Drekonja, Linda O Eckert, Suzanne E Geerlings, Béla Köves, Thomas M Hooton, Manisha Juthani-Mehta, Shandra L Knight, Sanjay Saint, Anthony J Schaeffer, Barbara Trautner, Bjorn Wullt, Reed Siemieniuk, Clinical Practice Guideline for the Management of Asymptomatic Bacteriuria: 2019 Update by the Infectious Diseases Society of America, Clinical Infectious Diseases, Volume 68, Issue 10, 15 May 2019, Pages e83–e110, https://doi.org/10.1093/cid/ciy1121
- Jazayeri SB, Balaji KC. Re: Antibiotic Prophylaxis for the Prevention of Infectious Complications following Prostate Biopsy: A Systematic Review and Meta-AnalysisA. Pilatz, K. Dimitropoulos, R. Veeratterapillay, Y. Yuan, M. I. Omar, S. MacLennan, T. Cai, F. Bruyère, R. Bartoletti, B. Köves, F. Wagenlehner, G. Bonkat and B. Pradere J Urol 2020; 204: 224-230. J Urol. 2020 Dec;204(6):1349-1350. doi: 10.1097/JU.0000000000001332. Epub 2020 Aug 24. PMID: 32830995.
- Инфекции мочевых путей при беременности (РОУ, РОАГ), 2025 https://nokpc53.gosuslugi.ru/netcat_files/8/9/Infektsiya_mochevyh_putey_pri_beremennosti.pdf
- Nicolle LE, Gupta K, Bradley SF, et al. Clinical Practice Guideline for the Management of Asymptomatic Bacteriuria: 2019 Update by the Infectious Diseases Society of America. Clin Infect Dis. 2019;68(10):e83-e110.
- Cai T, Nesi G, Mazzoli S, et al. Asymptomatic bacteriuria treatment is associated with a higher prevalence of antibiotic-resistant strains in women with urinary tract infections. Clin Infect Dis. 2015;61(11):1655–1661. doi:10.1093/cid/civ696.
- Givler DN, Givler A. Asymptomatic Bacteriuria. [Updated 2023 Jul 17]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2025 Jan-. Available from: https://www.ncbi.nlm.nih.gov/sites/books/NBK441848/
- Cliodna McNulty, Managing asymptomatic bacteriuria in the elderly, Practice Nursing, Volume 25, Number 1, https://doi.org/10.12968/pnur.2014.25.1.11
- Andreeva EM, Zakharova AV, Izotova AA, et al. Structure of community-acquired urinary tract infection pathogens in the Russian Federation in 2022–2024: results of the RESOURCE-2 study. Urologiia. 2025;(5):5-17.
- Roos V. ABU 83972 competition and growth repression of UPEC in human urine. PMC. 2025.
- Roos V, Ulett GC, Schembri MA, Klemm P. The asymptomatic bacteriuria Escherichia coli strain 83972 outcompetes uropathogenic E. coli strains in human urine. Infect Immun. 2006 Jan;74(1):615-24. doi: 10.1128/IAI.74.1.615-624.2006. PMID: 16369018; PMCID: PMC1346649.
- George I, et al. Competitive fitness of asymptomatic bacteriuria E. coli strain 83972 against uropathogens in human urine. Infect Immun. 2024; (in press). DOI:10.1128/iai.00173-24.
- Renko M, Tapanainen P, Tossavainen P, Pokka T, Uhari M. Meta-analysis of the significance of asymptomatic bacteriuria in diabetes. Diabetes Care. 2011 Jan;34(1):230-5. doi: 10.2337/dc10-0421. Epub 2010 Oct 11. PMID: 20937688; PMCID: PMC3005460.
- Mitra A, Ray S, Baidya A, et al. A study to estimate the prevalence of Asymptomatic Bacteriuria (ASB) in type 2 diabetes mellitus. CME Geriatric Med. 2025;03:1114.
- Journal of UTI. Prevalence of Asymptomatic Bacteriuria in Older Adults - A Narrative Review. UTI Journal. 2024;12(1):12.
- Everitt KA, Baldwin M, Tinker N, Stuhr K, Morris DS, Veillette JJ. Outcomes associated with asymptomatic bacteriuria management in elderly patients hospitalized with a ground-level fall. Antimicrob Steward Healthc Epidemiol. 2025 Mar 3;5(1):e72. doi: 10.1017/ash.2024.493. PMID: 40109917; PMCID: PMC11920912.
- Rao Z, Wang Z, Tang M, Shen L, Zhang K. Treatment of asymptomatic bacteriuria after kidney transplantation: a systematic review and meta-analysis of randomized controlled trials. Medicina (Kaunas). 2023;59(9):1606. doi:10.3390/medicina59091606.
- Medina-Polo J, Gómez Dos Santos V, Domínguez-Rodríguez S, et al. Systematic review and meta-analysis provide no guidance on management of asymptomatic bacteriuria within the first year after kidney transplantation. Antibiotics (Basel). 2024;13(5):442. doi:10.3390/antibiotics13050442.
- Coussement J, Kamar N, Matignon M, et al. Antibiotics versus no therapy in kidney transplant recipients with asymptomatic bacteriuria (BiRT): a pragmatic, multicentre, randomized, controlled trial. Clin Microbiol Infect. 2021;27(3):398–405. doi:10.1016/j.cmi.2020.08.016.
- Guideline for the Management of Bacteriuria in Pregnancy - Right Decisions, https://rightdecisions.scot.nhs.uk/media/2399/bacteriuria-in-pregnancy-aug-2023.pdf
- Л.А. Синякова, И.В. Косова. Инфекции мочевых путей у беременных. Современные подходы к лечению. «ЭФФЕКТИВНАЯ ФАРМАКОТЕРАПИЯ. Акушерство и Гинекология» №1. 2008
- Тютюнник В.Л., Кан Н.Е., Михайлова О.И., Мирзабекова Д.Д. Алгоритм диагностики и лечения бессимптомной бактериурии при беременности - Журнал «Акушерство и Гинекология», 2022, №12
- Odindo DA, Ochieng B, Onduru F, Ouma C, Onguru D, Awandu SS. Etiology of asymptomatic bacteriuria, antimicrobial susceptibility patterns and associated risk factors among pregnant women attending antenatal clinic in western Kenya. PLOS Glob Public Health. 2025 Mar 20;5(3):e0004347. doi: 10.1371/journal.pgph.0004347. PMID: 40112276; PMCID: PMC11925459
- Muneeba Sadaf, Afshan Zaman, Fatima Bibi, Maria Tariq. Frequency of Asymptomatic Bacteriuria in Pregnant Women. DOI: https://doi.org/10.53350/pjmhs2115103520
- ResearchGate. Systematic Review and Meta-Analysis: Global Prevalence and Antimicrobial Resistance Patterns of ASB in Pregnant Women (2000-2024). 2026.
- World Health Organization (WHO). The Global Crisis of Antimicrobial Resistance (AMR) in Maternal Health. ResearchGate. 2025.
- USPSTF. Screening for Asymptomatic Bacteriuria in Adults: US Preventive Services Task Force Recommendation. USPSTF. 2024.
- Kass EH. Bacteriuria and pyelonephritis of pregnancy. Arch Intern Med. 1960;105:194–198. doi:10.1001/archinte.1960.03840020016004.
- Smaill FM, Vazquez JC. Antibiotics for asymptomatic bacteriuria in pregnancy. Cochrane Database Syst Rev. 2019;11(11):CD000490. doi:10.1002/14651858.CD000490.pub4.
- Nicolle LE, Gupta K, Bradley SF, et al. Clinical practice guideline for the management of asymptomatic bacteriuria: 2019 update by the Infectious Diseases Society of America. Clin Infect Dis. 2019;68(10):e83–e110. doi:10.1093/cid/ciy1121.
- American College of Obstetricians and Gynecologists. Urinary tract infections in pregnant individuals. ACOG Practice Bulletin No. 230. Obstet Gynecol. 2023;142(2):e63–e80. doi:10.1097/AOG.0000000000005220.
- World Health Organization. WHO recommendations on antenatal care for a positive pregnancy experience. Geneva: WHO; 2016. https://www.who.int/publications/i/item/9789241549912
- Hill JB, Sheffield JS, McIntire DD, Wendel GD Jr. Acute pyelonephritis in pregnancy. Obstet Gynecol. 2005;105(1):18–23. doi:10.1097/01.AOG.0000149154.96285.32.
- Alsaywid BS, Smith GH. Antibiotic prophylaxis for transurethral urological surgeries: systematic review. Can J Urol. 2013;20(6):6606–6614.
- Summary of the 2024 Guidelines. Eur Urol. 2024.
- Milosevic M, Magnutzki A, Braun T, et al. Anti-inflammatory and cytoprotective polypharmacology of Canephron N reveals targeting of the IKK-NF-κB and p38-MK2-RIPK1 axes. Biomed Pharmacother. 2024;182(3):117747.
- Lokshin KL. [Comparative effectivenesss of standard antibiotic therapy and Canephron N asymptomatic bacteriuria in pregnant women]. Urologiia. 2018 Jul;(3):54-57. Russian. PMID: 30035419.
- Amdiy RE, Bayguzin RR, Darienko RO, et al. Efficacy and safety of Canephron N in preventing recurrences of uncomplicated lower urinary tract infection in women. Urologiia. 2025;(5):24-31.
- Siahlou B, et al. Effectiveness of Canephron® N in the Treatment of Acute Cystitis and Prevention of Recurrences: IQVIA Database Analysis. Antibiotics. 2021;10(6):685.
- Monje, A.; Escolà-Vergé, L.; Rivera, A.; Herrera, S.; Plaza, A.; Duch-Llorach, P.; Pomar, V.; Roch, N.; Rouras, L.; López-Contreras, J.; Ramos, J.R. Targeting Overtreatment of Asymptomatic Bacteriuria in the Emergency Department: Results from a Quasi-Experimental Clinical Pharmacist-Led Program Based on Education and Audit. Antibiotics 2025, 14, 1261.
- Impact of an Educational Leaflet About Asymptomatic Bacteriuria and Urinary Tract Infection on Antibiotic Preferences Among US Adults ≥65 Years: An Online Randomized Controlled Survey Experiment (2025). Open Forum Infectious Diseases, PMCID: PMC12703713.
erid: 2W5zFK2uQwT ООО «Бионорика» ИНН 7729590470







 Скачать
Скачать Скачать текст
Скачать текст Смотреть видео
Смотреть видео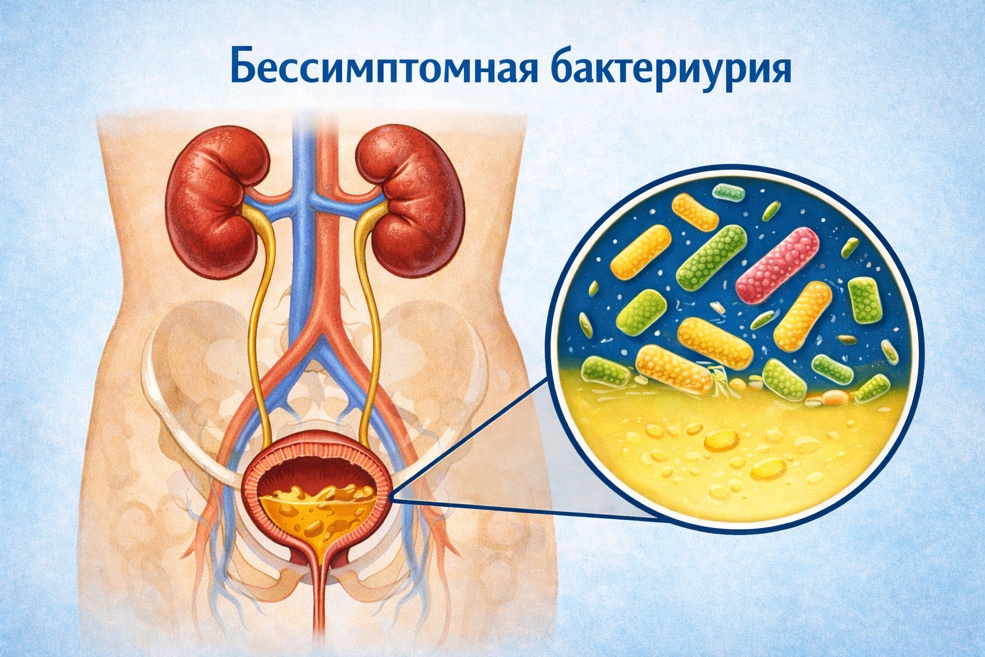










Комментарии