Эндотелиальная дисфункция как центральный патофизиологический механизм эректильной дисфункции: фундаментальные и клинические аспекты
Автор обзора: Шадеркина В.А., уролог, CEO Uroweb.ru
План обзора
- 1. Современные представления об ЭД
- 2. Фундаментальная роль эндотелия в физиологии эрекции
- 3. Патофизиологические механизмы эндотелиальной дисфункции
- 4. Эректильная дисфункция и ССЗ: гипотеза калибра артерий
- 5. Особенности патогенеза при специфических состояниях
- 6. Современная диагностика эндотелиальной функции
- 7. Терапевтические стратегии, направленные на реабилитацию эндотелия
- 8. Заключение
- 9. Литература
1. Современные представления об ЭД
Современная урологическая наука рассматривает эректильную дисфункцию (ЭД) не просто как нарушение качества жизни или расстройство сексуальной сферы, но как ранний и высокочувствительный маркер системного сосудистого неблагополучия [1]. В течение последнего десятилетия концепция ЭД претерпела значительную эволюцию: от преимущественно психогенного состояния до понимания её как «верхушки айсберга» генерализованного поражения сосудистого русла [2, 3].
Ключевым звеном, объединяющим эректильную дисфункцию с сердечно-сосудистыми заболеваниями (ССЗ), сахарным диабетом и метаболическим синдромом, является эндотелиальная дисфункция (ЭнД) [4].
Эндотелий полового члена представляет собой уникальную структуру с чрезвычайно высокой площадью поверхности относительно объема ткани, что делает его критически уязвимым к метаболическим и гемодинамическим стрессорам. Для практикующего уролога понимание молекулярных механизмов ЭнД является залогом не только успешного восстановления половой функции, но и эффективной профилактики фатальных сердечно-сосудистых событий у пациентов [5, 6].
2. Фундаментальная роль эндотелия в физиологии эрекции
Эрекция является сложным нейроваскулярным процессом, требующим гармоничного взаимодействия центральной нервной системы, периферических нервов, эндотелия и гладкомышечных клеток кавернозных тел. Эндотелий — это не просто механическая выстилка сосудов, а активный орган, осуществляющий паракринную, эндокринную и аутокринную регуляцию [7, 8].
2.1. Молекулярный каскад оксида азота (NO)
Ведущим медиатором, обеспечивающим расслабление кавернозной ткани, является оксид азота (NO). В норме сексуальная стимуляция инициирует высвобождение NO из неадренергических нехолинергических (НАНХ) нейронов (нейрональная NO-синтаза, nNOS). Однако для достижения и поддержания полной ригидности необходим массивный выброс NO из эндотелиальных клеток под воздействием механического напряжения сдвига, возникающего при заполнении кавернозных тел кровью [9, 10].
Процесс биосинтеза NO в эндотелии катализируется ферментом eNOS (эндотелиальная NO-синтаза) в присутствии кофакторов, таких как тетрагидробиоптерин (BH4), НАДФН и ионы кальция. Уравнение реакции выглядит следующим образом:
Высвобожденный NO диффундирует в гладкомышечные клетки кавернозных тел и сосудов, активируя растворимую гуанилатциклазу (sGC), которая превращает ГТФ в циклический гуанозинмонофосфат (цГМФ). Рост концентрации цГМФ активирует протеинкиназу G (PKG), что приводит к снижению уровня внутриклеточного кальция (Сa2+) и дефосфорилированию легких цепей миозина, вызывая релаксацию мышц и расширение кавернозных лакун [11, 12].
2.2. Баланс вазодилатирующих и вазоконстрикторных факторов
Эндотелий поддерживает сосудистый тонус за счет динамического равновесия между расслабляющими и сокращающими факторами. В таблице 1 представлены ключевые медиаторы, участвующие в этом процессе.
Таблица 1. Медиаторы процесса эрекции
|
Категория |
Медиатор |
Механизм действия |
Влияние на эрекцию |
|
Вазодилататоры |
Оксид азота (NO) |
Активация цГМФ-пути |
Ключевой триггер эрекции |
|
Простациклин (PGI2) |
Активация цАМФ-пути |
Синергизм с NO |
|
|
EDHF |
Гиперполяризация мембраны |
Вспомогательная вазодилатация |
|
|
Вазоконстрикторы |
Эндотелин-1 (ET-1) |
Рецепторы ETA и ETB |
Флацидность, вазоконстрикция |
|
Ангиотензин II |
Рецепторы AT1 |
Сосудистое сопротивление |
|
|
Тромбоксан А2 |
Активация тромбоцитов |
Снижение кровотока |
Кавернозные тела полового члена образованы сетью сосудистых лакун (синусов), выстланных эндотелием и окружённых трабекулярными гладкими мышцами. Кровоснабжение осуществляется через кавернозные и гелициновые-артерии (спиралевидные артерии), обладающие выраженной способностью к изменению просвета. Венозный отток происходит через венулы, проходящие под белочной оболочкой.
Расслабление гладких мышц приводит к расширению синусов и артериол, увеличению притока крови и росту внутрипещеристого давления, что вызывает механическое сдавление венозных сосудов (вено-окклюзионный механизм). Напротив, сокращение гладкомышечных элементов уменьшает объем синусов, снижает приток и восстанавливает свободный венозный отток.
Следовательно, клеточный уровень регуляции — изменение концентрации внутриклеточного Ca²⁺ и чувствительности сократительного аппарата к кальцию — является конечной точкой действия всех нейрогуморальных факторов.
2.2.1. Вазодилатирующие механизмы
Оксид азота и система cGMP
Центральную роль в инициации и поддержании эрекции играет оксид азота (NO). Он синтезируется нервными окончаниями (нейрональная NO-синтаза) и эндотелиальными клетками (эндотелиальная NO-синтаза).
NO свободно диффундирует в гладкомышечные клетки, где активирует растворимую гуанилатциклазу, повышая концентрацию циклического гуанозинмонофосфата (cGMP).
Последующая активация протеинкиназы G приводит к:
- снижению входа Ca²⁺ через потенциалзависимые каналы,
- усилению захвата Ca²⁺ саркоплазматическим ретикулумом,
- открытию калиевых каналов и гиперполяризации мембраны,
- снижению фосфорилирования миозина.
Совокупность этих эффектов вызывает выраженную релаксацию гладких мышц и вазодилатацию. Продолжительность действия сигнала ограничивается фосфодиэстеразой 5-го типа, расщепляющей cGMP.
Простаноиды и система cAMP
Эндотелий кавернозных сосудов также продуцирует простациклин (PGI₂), который через рецепторно-аденилатциклазный путь повышает уровень cAMP и активирует протеинкиназу A. Данный каскад, аналогично системе cGMP, снижает внутриклеточный Ca²⁺ и способствует расслаблению гладкой мускулатуры.
Эндотелий-зависимая гиперполяризация
Дополнительный вклад в вазорелаксацию вносят механизмы эндотелий-зависимой гиперполяризации, реализующиеся через активацию калиевых каналов гладкомышечных клеток. Это снижает их возбудимость и усиливает дилатационный ответ.
Нейропептидные медиаторы
Парасимпатические и NANC-нейроны могут выделять вазоактивные пептиды (например, VIP), потенцирующие образование cAMP и усиливающие NO-зависимую релаксацию, что стабилизирует эрекцию.
2.2.2. Вазоконстрикторные механизмы
Симпатическая адренергическая регуляция
В состоянии покоя преобладает симпатический тонус. Норадреналин, воздействуя на α₁-адренорецепторы гладкомышечных клеток, повышает внутриклеточный Ca²⁺ и активирует сократительный аппарат. Это обеспечивает сужение кавернозных артериол и поддержание флакцидности.
Эндотелин-1
Эндотелин-1 является одним из наиболее мощных эндогенных вазоконстрикторов. Его связывание с ETA-рецепторами вызывает стойкое сокращение гладкой мускулатуры и уменьшение кавернозного кровотока. Повышенная активность этой системы характерна для эндотелиальной дисфункции.
Ангиотензин II
Ангиотензин II через AT₁-рецепторы усиливает вазоконстрикцию, повышает чувствительность сосудов к катехоламинам и поддерживает высокий базальный тонус.
Простаноиды вазоконстрикторного типа
Тромбоксан A₂ и некоторые простагландины способны индуцировать сокращение гладких мышц и противодействовать дилатационным сигналам.
Путь RhoA/ROCK
Особое значение имеет система кальциевой сенситизации через каскад RhoA/ROCK. Она подавляет активность миозин-фосфатазы, что усиливает сокращение даже без дополнительного повышения Ca²⁺. Этот механизм играет ведущую роль в поддержании базального тонуса и детумесценции.
2.2.3. Динамика баланса в различные фазы эректильного ответа
В фазе покоя преобладают вазоконстрикторные влияния симпатической нервной системы, эндотелина и ангиотензина II.
При сексуальной стимуляции активируются нитрэргические нейроны, происходит выброс NO, что инициирует быстрое расслабление кавернозных артериол и синусов. Возрастающий кровоток усиливает эндотелиальную продукцию NO, формируя положительную обратную связь.
В фазе полной ригидности поддержание низкого тонуса гладких мышц сочетается с механической компрессией венозного русла, обеспечивая эффективную вено-окклюзию.
Детумесценция развивается при восстановлении симпатического доминирования, распаде cGMP и активации сократительных путей, что приводит к уменьшению притока и возобновлению венозного оттока (рис. 1, 2).
Рис. 1. Схематическое представление каскада реакций эректильной функции.
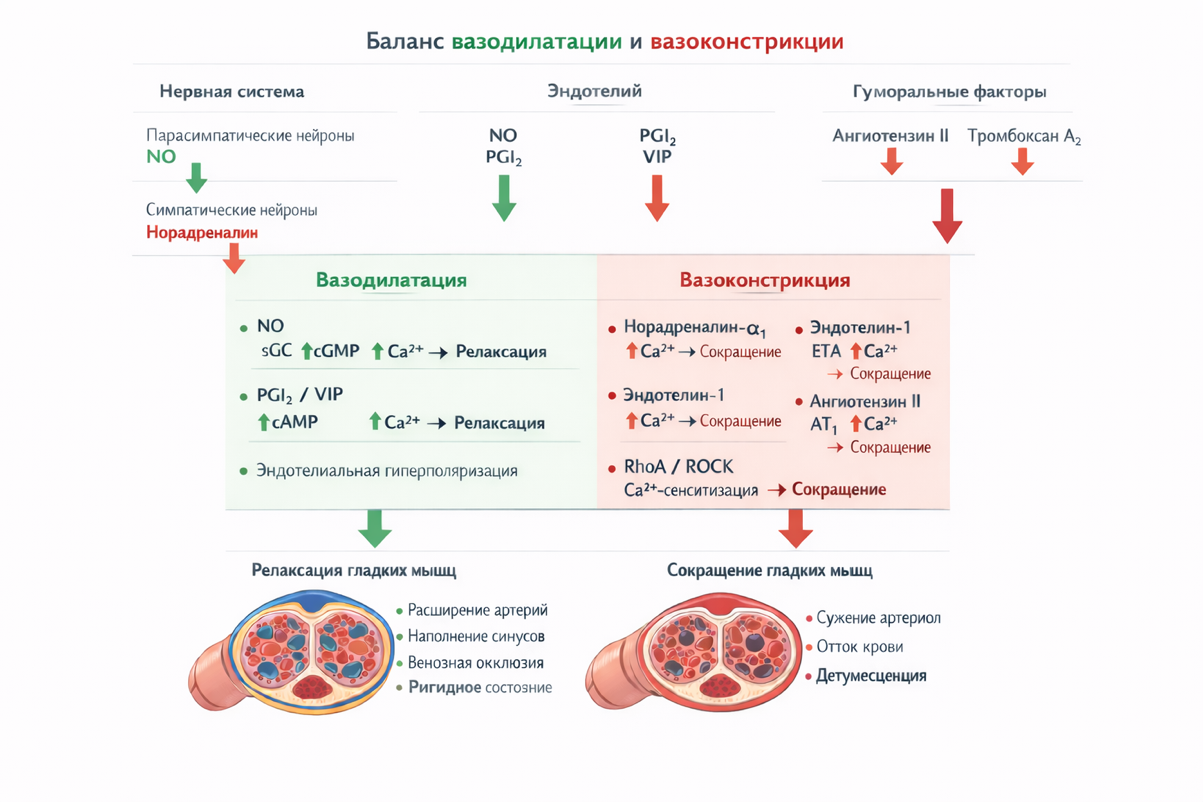
Рис. 2. Баланс вазодилатирующих и вазоконстрикторных факторов. Иллюстрация носит схематический характер. Не предназначена для клинической интерпретации.
Нарушение соотношения вазодилататоров и вазоконстрикторов лежит в основе большинства форм эректильной дисфункции. Снижение биодоступности NO при эндотелиальной дисфункции, усиление симпатического тонуса, активация RhoA/ROCK-пути или структурная перестройка кавернозной ткани (фиброз, снижение эластичности) приводят к преобладанию вазоконстрикции и невозможности адекватной релаксации гладких мышц.
Таким образом, эректильная дисфункция может рассматриваться как сосудисто-эндотелиальный феномен, отражающий системные нарушения микроциркуляции и часто ассоциированный с сердечно-сосудистыми заболеваниями.
3. Патофизиологические механизмы эндотелиальной дисфункции
Эндотелиальная дисфункция (ЭнД) характеризуется потерей физиологического баланса, снижением биодоступности NO и активацией патологических путей, ведущих к вазоконстрикции, пролиферации и фиброзу [13, 14].
3.1. Оксидативный стресс и «разобщение» eNOS
Центральным звеном ЭнД является избыточная продукция активных форм кислорода (АФК), таких как супероксид-анион (О2-). В условиях гипергликемии, гипертензии или курения активность НАДФН-оксидаз резко возрастает. Супероксид крайне быстро вступает в реакцию с NO, образуя пероксинитрит (ONOO-) — мощный окислитель:
Этот процесс не только «крадет» доступный NO, но и приводит к окислению кофактора BH4. Дефицит BH4 вызывает феномен «разобщения» eNOS, при котором фермент вместо NO начинает продуцировать супероксид, что создает порочный круг повреждения эндотелия и прогрессирования ЭД [15, 16].
3.2. Система RhoA/Rho-киназы как «тормоз» эрекции
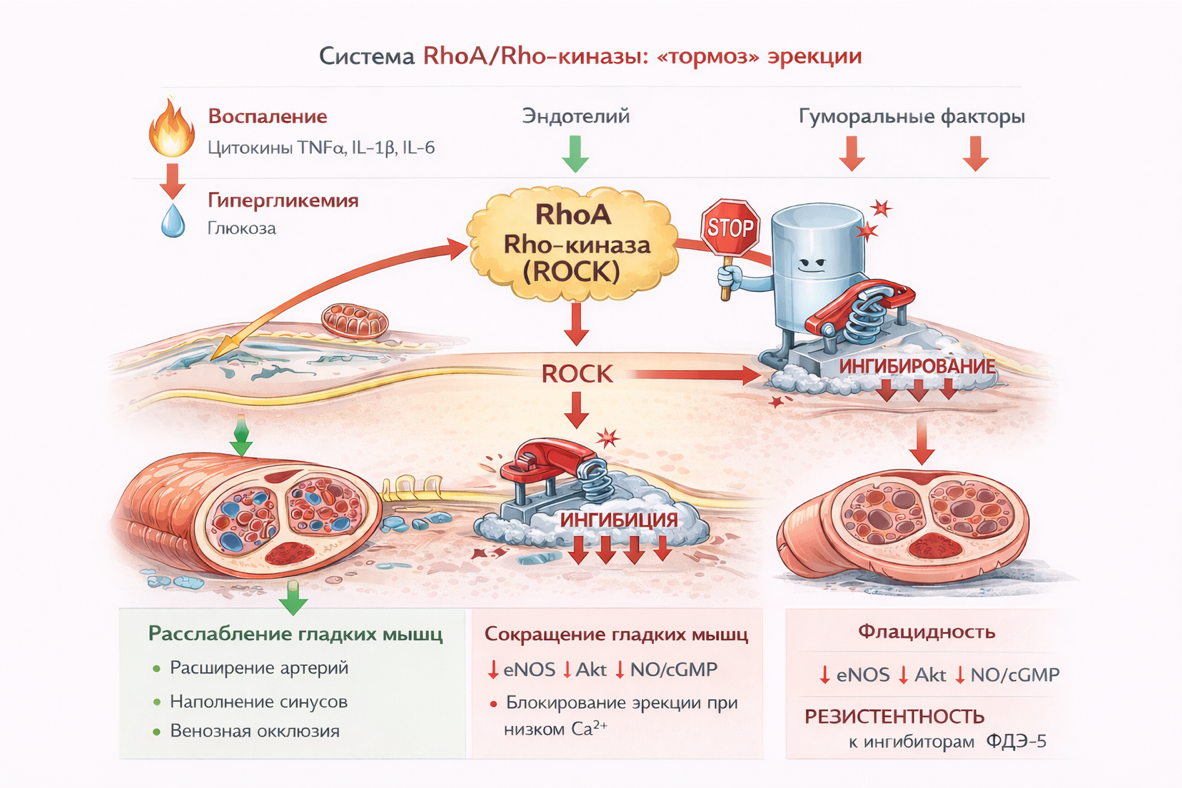
Современные исследования (2023–2024 гг.) подтверждают важнейшую роль сигнального пути RhoA/Rho-киназы (ROCK) в поддержании состояния детумесценции и развитии ЭД [7]. Активация ROCK под действием провоспалительных цитокинов или гипергликемии приводит к ингибированию фосфатазы легких цепей миозина (MLCP) [17]. Это поддерживает гладкомышечные клетки в состоянии сокращения даже при низких уровнях кальция, блокируя возможность эрекции (рис. 3).
Рис. 3. Роль системы RhoA/Rho-киназы в развитии ЭД. Иллюстрация носит схематический характер. Не предназначена для клинической интерпретации.
Кроме того, путь RhoA/ROCK напрямую подавляет экспрессию eNOS и активность протеинкиназы Akt, что делает ЭД резистентной к стандартной терапии ингибиторами ФДЭ-5 [16].
3.3. Роль эндотелина-1 и воспалительных маркеров
Эндотелин-1 (ET-1) является мощнейшим вазоконстриктором, уровень которого значительно повышен при васкулогенной ЭД. Гиперпродукция ET-1 не только сужает сосуды полового члена, но и стимулирует пролиферацию неоинтимы и фиброз кавернозной ткани.
Системное воспаление низкого порядка, проявляющееся повышением уровня С-реактивного белка (СРБ), интерлейкина-6 (ИЛ-6) и фактора некроза опухоли-альфа (ФНО-альфа), также вносит вклад в развитие ЭД [18]. Эти цитокины активируют экспрессию молекул адгезии (E-селектин, ICAM-1, VCAM-1), что способствует лейкоцитарной инфильтрации сосудистой стенки и инициации атеросклеротического процесса [19, 20]. В российских исследованиях было показано, что уровень селектинов и ICAM-1 у пациентов с ЭД достоверно коррелирует с тяжестью поражения коронарных артерий [21, 22].
4. Эректильная дисфункция и ССЗ: гипотеза калибра артерий
Связь между ЭД и ССЗ объясняется «гипотезой калибра артерий». Атеросклероз – хроническое воспалительное заболевание, характеризующееся образованием в стенках артерий среднего и крупного калибра фиброзно-жировых бляшек (атером). Его развитие связано с дисфункцией эндотелия, накоплением липопротеинов (особенно ЛПНП) в интиме сосуда и последующей воспалительной реакцией, что может приводить к сужению просвета артерии, острой тромботической окклюзии и ишемическому повреждению органов. Как правило, это системный процесс, но клинические проявления зависят от диаметра сосуда. Артерии полового члена имеют диаметр 1–2 мм, коронарные — 3–4 мм, сонные — 5–7 мм. Таким образом, сужение просвета на 50% критически снижает кровоток в мелких артериях полового члена гораздо раньше, чем это приведет к ишемии миокарда или мозга [2].
Данные мета-анализов 2022–2024 годов подтверждают, что ЭД является независимым предиктором ССЗ, повышая риск:
- сердечно-сосудистых событий на 45–48%;
- инфаркта миокарда на 55%;
- инсульта на 35–42%;
- общей смертности на 25%.
ЭД предшествует развитию клинически значимой ИБС в среднем на 3–5 лет, что создает уникальное «терапевтическое окно» для кардиопротективного вмешательства [23, 24, 25].
5. Особенности патогенеза при специфических состояниях
5.1. Сахарный диабет и диабетическая ЭД
Диабет является наиболее агрессивным фактором риска ЭнД. Патогенез диабетической ЭД многогранен и включает:
- Конечные продукты гликирования (AGEs). Гликирование структурных белков делает сосуды жесткими и активирует рецепторы RAGE, запуская оксидативный стресс .
- Потеря перицитов. Перициты необходимы для стабильности сосудистой выстилки. При диабете наблюдается их массовый апоптоз в кавернозной ткани, что ведет к «утечке» крови и вено-окклюзивной недостаточности .
- Программируемая клеточная гибель. Новейшие данные (2025 г.) указывают на активацию ферроптоза и пироптоза в кавернозных эндотелиоцитах под влиянием гипергликемии [10, 26, 27].
5.2. Гипогонадизм и андрогенный дефицит
Тестостерон является фундаментальным регулятором функции эндотелия у мужчин [28]. Он не только поддерживает сексуальное желание, но и стимулирует экспрессию eNOS и ФДЭ-5 [29]. Дефицит тестостерона ведет к атрофии гладких мышц и замещению их коллагеном (фиброзу), что делает медикаментозную терапию ЭД неэффективной [30]. Международные рекомендации (EAU, AUA 2025) подчеркивают необходимость коррекции уровня тестостерона до еугонадных значений для восстановления реактивности эндотелия [22, 31].
6. Современная диагностика эндотелиальной функции
Для практикующего уролога диагностика должна быть направлена на выявление васкулогенного генеза ЭД и оценку системного риска [31].
6.1. Клинические инструменты и опросники
Использование валидированных инструментов, таких как IIEF-5 (МИЭФ-5) или SHIM, обязательно для оценки степени тяжести ЭД и мониторинга эффективности лечения. Рекомендации AUA (2024) также настаивают на проведении тщательного скрининга на наличие симптомов гипогонадизма и ССЗ [32, 33].
6.2. Лабораторные и инструментальные маркеры
Согласно стандартам доказательной медицины, диагностический минимум включает:
- Определение уровня общего тестостерона утром натощак (минимум дважды при низких значениях) .
- Гликемический профиль (HbA1c).
- Липидный спектр (ЛПНП, ЛПВП, триглицериды).
Инструментальная диагностика основывается на динамической ультразвуковой фармакодопплерографии сосудов полового члена (CDDU). Снижение пиковой систолической скорости (PSV < 25 см/с) является прямым признаком артериальной недостаточности вследствие ЭнД. Кроме того, оценка потокозависимой вазодилатации (FMD) плечевой артерии может служить маркером системного состояния эндотелия [32].
7. Терапевтические стратегии, направленные на реабилитацию эндотелия
Современный подход к лечению ЭД смещается от симптоматического («по требованию») к патогенетическому, направленному на восстановление сосудистой функции.
7.1. Ингибиторы ФДЭ-5 в формате курсовой терапии
Ингибиторы фосфодиэстеразы 5 типа (силденафил, тадалафил, варденафил, аванафил) остаются первой линией терапии консервативного медикаментозного лечения (табл. 2) [34, 35, 36, 45]. Помимо эффекта, длительный прием (особенно тадалафила 5 мг ежедневно) способствует реабилитации эндотелия за счет [46]:
- Постоянной активации eNOS и повышения продукции NO.
- Снижения уровней провоспалительных маркеров и ET-1.
- Улучшения функции эндотелиальных прогениторных клеток.
Табл. 2. Ингибиторы ФДЭ-5 типа в лечении ЭД.
|
Препарат |
Особенности |
Роль в реабилитации эндотелия |
|
Тадалафил |
Длительный T1/2 (36 ч) |
Оптимален для ежедневного приема (5 мг)* |
|
Силденафил |
Мощный быстрый эффект |
Доказанное влияние на системную гемодинамику |
|
Аванафил |
Высокая селективность |
Минимум побочных эффектов, быстрый старт |
|
Варденафил |
|
|
* По показанию доброкачественная гиперплазия предстательной железы (ДГПЖ) или ЭД/ДГПЖ или по показанию эректильная дисфункция (ЭД) для пациентов с частой сексуальной активностью (2 раза в неделю и более).
Российские исследования подтверждают эффективность и патофизиологическое обоснование применения ингибиторов фосфодиэстеразы 5-го типа (ИФДЭ-5) в том числе у пациентов с симптомами нижних мочевых путей (СНМП) на фоне доброкачественной гиперплазии предстательной железы (ДГПЖ) и сопутствующей эректильной дисфункции (ЭД). Авторы исследования установили достоверную корреляцию между тяжестью СНМП и риском развития ЭД. У мужчин в возрасте 50–78 лет наличие СНМП повышает риск развития ЭД до 7,5 раза. Развитие обоих состояний связывают с ослаблением передачи сигнала по пути NO-цГМФ, усилением сигнала RhoA-Rho-киназы, гиперактивностью вегетативной нервной системы и атеросклерозом артерий таза. Среди группы ИФДЭ-5 тадалафил выделяется благодаря длительному периоду полувыведения. Он официально разрешен для ежедневного приема в дозе 5 мг для лечения СНМП при ДГПЖ. Препарат способствует накоплению цГМФ, что обеспечивает релаксацию гладких мышц мочевого пузыря, простаты и сосудов, улучшает оксигенацию тканей и снижает интенсивность воспаления. Применение тадалафила 5 мг как в монотерапии, так и в комбинации с α1-адреноблокаторами или ингибиторами 5АРИ достоверно улучшает показатели по шкалам IPSS (индекс симптомов при заболеваниях простаты) и МИЭФ (международный индекс эректильной функции). Ученые сделали вывод о том, что ежедневный прием тадалафила в дозе 5 мг является эффективным и безопасным методом терапии первой линии медикаментозной терапии для пациентов с сочетанным течением ДГПЖ и ЭД, позволяя одновременно воздействовать на обе группы симптомов [37].
Другие российские авторы заявляют, что эффективность тадалафила зависит от этиологии ЭД, наличия сопутствующих заболеваний и характера проводимой терапии. Тадалафил может применяться у мужчин с сахарным диабетом и метаболическим синдромом, поскольку показал свою эффективность у этих групп пациентов с ЭД. Тадалафил отлично сочетается с типичными препаратами, применяющимися при ДГПЖ. Тадалафил эффективен в ряде случаев при нейрогенной ЭД, хотя и с некоторыми ограничениями; наиболее перспективно его применение при травме спинного мозга и рассеянном склерозе. Убедительных данных, свидетельствующих об отрицательном влиянии тадалафила на фертильность, не опубликовано, хотя делать вывод о его положительном воздействии на сперматогенез и подвижность сперматозоидов тоже преждевременно. Они отметили, что появление на российском рынке дженерика тадалафила – «Динамико Лонг», производимого компанией «Тева» на основе израильской субстанции с соблюдением современных требований и стандартов качества, может сделать такой вариант терапии более доступным по сравнению с применением оригинального тадалафила. Важно, что подобное лечение положительно сказывается не только на эректильной, но и на оргазмической и эякуляторной функциях, а длительный срок действия препарата способствует поддержанию спонтанности половой жизни и повышает уверенность мужчины в собственных силах [47].
7.2. Регенеративные технологии
Для пациентов с ЭнД, резистентной к фармакотерапии, активно внедряются новые методы:
1. Ударно-волновая терапия низкой интенсивности (Li-ESWT). Метод стимулирует неоангиогенез через выброс факторов роста (VEGF) и активацию eNOS. Согласно рекомендациям ISSM (2024), Li-ESWT может рассматриваться как метод восстановления естественной эректильной функции [38].
2. Стволовые клетки (ADSCs). Использование мезенхимальных стволовых клеток направлено на восстановление популяции эндотелиоцитов и нейронов в кавернозных телах [39, 40, 41].
3. PRP-терапия. Богатая тромбоцитами плазма содержит высокую концентрацию факторов регенерации, однако её широкое применение пока ограничено рамками клинических исследований [42, 43, 44].
7.3. Модификация образа жизни и кардиопротекция
Рекомендации AUA (2024) и клинические рекомендации МЗ РФ подчеркивают, что модификация образа жизни (диета, физическая активность) имеет доказанную эффективность в улучшении функции эндотелия и эрекции (уровень доказательности Grade C) [33, 45]. Физические упражнения повышают активность eNOS за счет периодического увеличения напряжения сдвига, что является естественным стимулятором здоровья сосудов.
8. Заключение
Эндотелиальная дисфункция является фундаментальной причиной васкулогенной эректильной дисфункции, связывая её с широким спектром метаболических и сердечно-сосудистых заболеваний. Потеря биодоступности NO, активация оксидативного стресса и пути Rho-киназы формируют основу патологического процесса, который зачастую манифестирует в мелких сосудах полового члена за несколько лет до серьезных кардиологических событий.
Для практикующего уролога ЭД должна служить сигналом к проведению глубокого кардиоваскулярного скрининга. Применение современных протоколов диагностики, включающих оценку гормонального профиля и сосудистой реактивности, в сочетании с патогенетической терапией (ежедневный прием PDE5i, TRT, Li-ESWT), позволяет не только восстановить сексуальную функцию, но и значительно улучшить общий прогноз жизни пациента.
Литература
- Salonia A, Bettocchi C, Boeri L, Capogrosso P, Carvalho J, Cilesiz NC, Cocci A, Corona G, Dimitropoulos K, Gül M, Hatzichristodoulou G, Jones TH, Kadioglu A, Martínez Salamanca JI, Milenkovic U, Modgil V, Russo GI, Serefoglu EC, Tharakan T, Verze P, Minhas S; EAU Working Group on Male Sexual and Reproductive Health. European Association of Urology Guidelines on Sexual and Reproductive Health-2021 Update: Male Sexual Dysfunction. Eur Urol. 2021 Sep;80(3):333-357. doi: 10.1016/j.eururo.2021.06.007. Epub 2021 Jun 26. PMID: 34183196.
- Gandaglia G, Briganti A, Jackson G, Kloner RA, Montorsi F, Montorsi P, Vlachopoulos C. A systematic review of the association between erectile dysfunction and cardiovascular disease. Eur Urol. 2014 May;65(5):968-78. doi: 10.1016/j.eururo.2013.08.023. Epub 2013 Aug 23. PMID: 24011423.
- Кызласов П.С., Бурдин К.А., Хворов В.В., Митин А.А., Белов В.О. Современные методы диагностики и лечения эректильной дисфункции. Экспериментальная и клиническая урология 2024;17(4):68-75; https://doi.org/10.29188/2222-8543-2024-17-4-68-75
- An J, Xiang B, Peng J, Li D. Understanding the erectile dysfunction-cardiovascular disease connection: clinical and pathophysiological insights. Sex Med Rev. 2025 Jul 3;13(3):406-422. doi: 10.1093/sxmrev/qeaf014. PMID: 40153594.
- L. Burnett, MD; Ajay Nehra, MD; Rodney H. Breau, MD; Daniel J. Culkin, MD; Martha M. Faraday, PhD; Lawrence S. Hakim, MD; Joel Heidelbaugh, MD; Mohit Khera, MD; Kevin T. McVary, MD; Martin M. Miner, MD; Christian J. Nelson, PhD; Hossein Sadeghi-Nejad, MD; Allen D. Seftel, MD; Alan W. Shindel, MD. Erectile dysfunction: AUA guideline, 2018
- Аполихин О.И., Ефремов Е.А., Шадеркин И.А., Золотухин О.В., Мадыкин Ю.Ю., Зеленский М.М., Красняк С.С. Прогнозирование развития эректильной дисфункции и сердечно-сосудистых заболеваний на основании профиля факторов риска. Экспериментальная и клиническая урология, 2017(4):34-40
- Sopko NA, Hannan JL, Bivalacqua TJ. Understanding and targeting the Rho kinase pathway in erectile dysfunction. Nat Rev Urol. 2014 Nov;11(11):622-8. doi: 10.1038/nrurol.2014.278. Epub 2014 Oct 14. PMID: 25311680; PMCID: PMC4696116
- Priviero FB, Leite R, Webb RC, Teixeira CE. Neurophysiological basis of penile erection. Acta Pharmacol Sin. 2007 Jun;28(6):751-5. doi: 10.1111/j.1745-7254.2007.00584.x. PMID: 17506932
- Шарвадзе Г.Г., Далари Р.Р., Марданов Б.У., Мамедов М.Н., Лечение эректильной дисфункции у больных сердечно-сосудистыми заболеваниями и коморбидным состоянием: обзор клинических исследований по курсовой терапии препаратами фосфодиэстеразы-5 типа. Кардиоваскулярная терапия и профилактика. 2018;17(3):79–84. http://dx.doi.org/10.15829/1728-8800-2018-3-79-84
- Zhang J, Xin S, Mao J, Liu X, Wang T, Liu J, Song X, Song W. The role of programmed cell death in diabetes mellitus-induced erectile dysfunction: from mechanisms to targeted therapy. Reprod Biol Endocrinol. 2025 Mar 3;23(1):32. doi: 10.1186/s12958-025-01368-1. PMID: 40033391; PMCID: PMC11874627
- Toda N, Ayajiki K, Okamura T. Nitric oxide and penile erectile function. Pharmacol Ther. 2005 May;106(2):233-66. doi: 10.1016/j.pharmthera.2004.11.011. Epub 2005 Mar 2. PMID: 15866322
- Burnett AL. Nitric oxide regulation of penile erection: biology and therapeutic implications. J Androl. 2002 Sep-Oct;23(5):S20-6. PMID: 12236169] [Carneiro FS, Webb RC, Tostes RC. Emerging role for TNF-α in erectile dysfunction. J Sex Med. 2010 Dec;7(12):3823-34. doi: 10.1111/j.1743-6109.2010.01762.x. PMID: 20345734; PMCID: PMC3031865
- MacDonald SM, Burnett AL. Physiology of Erection and Pathophysiology of Erectile Dysfunction. Urol Clin North Am. 2021 Nov;48(4):513-525. doi: 10.1016/j.ucl.2021.06.009. PMID: 34602172
- Dean RC, Lue TF. Physiology of penile erection and pathophysiology of erectile dysfunction. Urol Clin North Am. 2005 Nov;32(4):379-95, v. doi: 10.1016/j.ucl.2005.08.007. PMID: 16291031; PMCID: PMC1351051
- Joo HK, Jeon BH. Endothelial Dysfunction: From Pathophysiology to Novel Therapeutic Approaches 2.0. Biomedicines. 2025 Oct 28;13(11):2639. doi: 10.3390/biomedicines13112639. PMID: 41301733; PMCID: PMC12650252
- Yao L, Romero MJ, Toque HA, Yang G, Caldwell RB, Caldwell RW. The role of RhoA/Rho kinase pathway in endothelial dysfunction. J Cardiovasc Dis Res. 2010 Oct;1(4):165-70. doi: 10.4103/0975-3583.74258. PMID: 21264179; PMCID: PMC3023892
- Randar S, Silva-Velasco DL, Priviero F, Webb RC. RhoA/Rho-Kinase Signaling in Vascular Smooth Muscle and Endothelium: Mechanistic Insights and Translational Implications in Hypertension. Biomolecules. 2025 Nov 16;15(11):1607. doi: 10.3390/biom15111607. PMID: 41301525; PMCID: PMC12650322
- Vlachopoulos C, Aznaouridis K, Ioakeimidis N, Rokkas K, Vasiliadou C, Alexopoulos N, Stefanadi E, Askitis A, Stefanadis C. Unfavourable endothelial and inflammatory state in erectile dysfunction patients with or without coronary artery disease. Eur Heart J. 2006 Nov;27(22):2640-8. doi: 10.1093/eurheartj/ehl341. Epub 2006 Oct 20. PMID: 17056702
- Richard L. Jayaraj, Elhadi H Aburawi. Mechanistic relationship between obesity-induced inflammation triggering endothelial dysfunction and the initiation of atherosclerosis development. Heart, Vessels and Transplantation 2025; 9: doi: 10.24969/hvt.2024.542
- Ledina D, Ivić I, Tadin A, Bodulić K, LeDuc JW, Markotić A. A Comprehensive Analysis of Renal and Endothelium Dysfunction Markers Fourteen Years after Hemorrhagic Fever with Renal Syndrome Contraction. Life. 2024; 14(5):575.https://doi.org/10.3390/life14050575
- Шарвадзе Г.Г., Далари Р.Р., Марданов Б.У., Мамедов М.Н., Лечение эректильной дисфункции у больных сердечно-сосудистыми заболеваниями и коморбидным состоянием: обзор клинических исследований по курсовой терапии препаратами фосфодиэстеразы-5 типа. Кардиоваскулярная терапия и профилактика. 2018;17(3):79–84. http://dx.doi.org/10.15829/1728-8800-2018-3-79-84
- И.А. Хрипун, С.В. Воробьев. Влияние тестостерона на функцию эндотелия у мужчин с сахарным диабетом 2 типа. Южно-Российский журнал терапевтической практики 2021;2(3):78-85. DOI 10.21886/2712-8156-2021-2-3-78-85
- Mostafaei H, Mori K, Hajebrahimi S, Abufaraj M, Karakiewicz PI, Shariat SF. Association of erectile dysfunction and cardiovascular disease: an umbrella review of systematic reviews and meta-analyses. BJU Int. 2021 Jul;128(1):3-11. doi: 10.1111/bju.15313. Epub 2021 Jan 9. PMID: 33260254; PMCID: PMC8359379
- Wenbin Guo MM, Cun Liao M, Fei Li MM, Xiangming Mao. Erectile Dysfunction and Risk of Clinical Cardiovascular Events: A Meta‐Analysis of Seven Cohort Studies. Journal of Sexual Medicine 7(8):2805 - 2816 DOI: 10.1111/j.1743-6109.2010.01792.x
- Osondu CU, Vo B, Oni ET et al.The relationship of erectile dysfunction and subclinical cardiovascular disease: a systematic review and meta‐analysis. Vasc Med 2018; 23: 9–20
- Seo-Gyeong Bae, Guo Nan Yin, Jiyeon Ock, Jun-Kyu Suh, Ji-Kan Ryu, Jihwan Park (2023). Single cell transcriptome analysis of cavernous tissues reveals the key roles of pericytes in diabetic erectile dysfunction. eLife12:RP88942. https://doi.org/10.7554/eLife.88942.1
- Jingbang Liu, Tao Jiang. Current status and advances in adipose-derived stem cells therapy for diabetes mellitus erectile dysfunction. Front. Med. 12:1634521. doi: 10.3389/fmed.2025.1634521
- Rajfer J. Relationship between testosterone and erectile dysfunction. Rev Urol. 2000 Spring;2(2):122-8. PMID: 16985751; PMCID: PMC1476110] [Mikhail N. Does testosterone have a role in erectile function? Am J Med. 2006 May;119(5):373-82. doi: 10.1016/j.amjmed.2005.07.042. PMID: 16651047
- Yassin AA, Saad F. Testosterone and erectile dysfunction. J Androl. 2008 Nov-Dec;29(6):593-604. doi: 10.2164/jandrol.107.004630. Epub 2008 Jul 17. PMID: 18641415
- Boloña ER, Uraga MV, Haddad RM, Tracz MJ, Sideras K, Kennedy CC, Caples SM, Erwin PJ, Montori VM. Testosterone use in men with sexual dysfunction: a systematic review and meta-analysis of randomized placebo-controlled trials. Mayo Clin Proc. 2007 Jan;82(1):20-8. doi: 10.4065/82.1.20. PMID: 17285782
- EAU 2025, https://uroweb.org/guidelines/sexual-and-reproductive-health
- Noah Stern, Petar Bajic, Jeffrey Campbell, Paolo Capogrosso, Trustin Domes, Eduardo P Miranda, John P Mulhall, Bruno Nascimento, Michael Pignanelli, Alexander W Pastuszak, Gerald Brock, Evolving medical management of erectile dysfunction: recommendations from the Fifth International Consultation on Sexual Medicine (ICSM 2024), Sexual Medicine Reviews, Volume 13, Issue 4, October 2025, Pages 513–537, https://doi.org/10.1093/sxmrev/qeaf035
- Arthur L. Burnett, MD; Ajay Nehra, MD; Rodney H. Breau, MD; Daniel J. Culkin, MD; Martha M. Faraday, PhD; Lawrence S. Hakim, MD; Joel Heidelbaugh, MD; Mohit Khera, MD; Kevin T. McVary, MD; Martin M. Miner, MD; Christian J. Nelson, PhD; Hossein Sadeghi-Nejad, MD; Allen D. Seftel, MD; Alan W. Shindel, MD. Erectile dysfunction: AUA guideline 2018
- Kouvelas D, Goulas A, Papazisis G, Sardeli C, Pourzitaki C. PDE5 inhibitors: in vitro and in vivo pharmacological profile. Curr Pharm Des. 2009;15(30):3464-75. doi: 10.2174/138161209789206971. PMID: 19860692] [Schwarz ER, Kapur V, Rodriguez J, Rastogi S, Rosanio S. The effects of chronic phosphodiesterase-5 inhibitor use on different organ systems. Int J Impot Res. 2007 Mar-Apr;19(2):139-48. doi: 10.1038/sj.ijir.3901491. Epub 2006 Jun 8. PMID: 16761012
- Andersson KE. Mechanisms of penile erection and basis for pharmacological treatment of erectile dysfunction. Pharmacol Rev. 2011 Dec;63(4):811-59. doi: 10.1124/pr.111.004515. Epub 2011 Aug 31. PMID: 21880989] [Hamzehnejadi M, Ranjbar Tavakoli M, Abiri A, Ghasempour A, Langarizadeh MA, Forootanfar H. A Review on Phosphodiesterase-5 Inhibitors as a Topical Therapy for Erectile Dysfunction. Sex Med Rev. 2022 Jul;10(3):376-391. doi: 10.1016/j.sxmr.2022.02.002. Epub 2022 Apr 1. PMID: 35370122
- Shafiee A, Bahri RA, Teymouri Athar MM, Afsharrezaei F, Gholami M. Phosphodiesterase 5 (PDE-5) inhibitors (sildenafil, tadalafil, and vardenafil) effects on esophageal motility: a systematic review. BMC Gastroenterol. 2023 May 22;23(1):170. doi: 10.1186/s12876-023-02787-3. PMID: 37217851; PMCID: PMC10201782
- Tsukanov AY, Semikina SP. The question of the treatment of patients with symptoms of the lower urinary tract on the background of benign prostatic hyperplasia with combined erectile dysfunction. Consilium Medicum. 2019;21(7):81-85. DOI: 10.26442/20751753.2019.7.190560.
- https://www.issm.info/issm-answers-your-questions-videos/what-are-your-thoughts-on-shockwave-therapy-for-erectile-dysfunction][Carolyn A. Salter, AUA2024 RECAPS Penile Rehabilitation 2024: Where Are We? https://www.auanews.net/issues/articles/2024/august-2024/aua2024-recaps-penile-rehabilitation-2024-where-are-we
- Wang B, Gao W, Zheng MY, Lin G, Lue TF. Recent advances in stem cell therapy for erectile dysfunction: a narrative review. Expert Opin Biol Ther. 2023 Jan-Jun;23(6):565-573. doi: 10.1080/14712598.2023.2203811. Epub 2023 Apr 20. PMID: 37078259; PMCID: PMC10330142
- 40. Patel, A.A., Shafie, A., Mohamed, A.H. et al. The promise of mesenchymal stromal/stem cells in erectile dysfunction treatment: a review of current insights and future directions.Stem Cell Res Ther 16, 98 (2025). https://doi.org/10.1186/s13287-025-04221-9
- Park HJ, Jeong H, Park YH, Yim HW, Ha US, Hong SH, Kim SW, Kim NJ, Lee JY. Adipose Tissue-Derived Stem Cell Therapy for Cavernous Nerve Injury-Induced Erectile Dysfunction in the Rat Model: A Systematic Review and Meta-Analysis Using Methodological Quality Assessment. Int J Stem Cells. 2019 Jul 31;12(2):206-217. doi: 10.15283/ijsc18122. PMID: 31022999; PMCID: PMC6657942
- Schirmann A, Boutin E, Faix A, Yiou R. Pilot study of intra-cavernous injections of platelet-rich plasma (P-shot®) in the treatment of vascular erectile dysfunction. Prog Urol. 2022 Dec;32(16):1440-1445. doi: 10.1016/j.purol.2022.05.002. Epub 2022 Jun 10. PMID: 35697553
- Panunzio A, Labate C, Zacheo F, Orlando R, Rizzo FL, Porcaro AB, Migliorini F, Pagliarulo V, Tafuri A. Platelet-rich plasma intracavernosal injections for the treatment of primary organic erectile dysfunction: a systematic review and meta-analysis of contemporary controlled studies. Int J Impot Res. 2024 Sep;36(6):562-571. doi: 10.1038/s41443-023-00798-y. Epub 2023 Nov 22. PMID: 37993601
- Jacob D, Hay J, Rahemtoola MS, Sim S, Libretto L, Chawareb EA, Hammad M, Mubarak M, Yafi F, Pearce I, Modgil V. Current advances in platelet-rich plasma therapy for erectile dysfunction: a meta-analysis of randomized controlled trials. J Sex Med. 2026 Jan 5;23(1):qdaf325. doi: 10.1093/jsxmed/qdaf325. PMID: 41288551
- Клинические рекомендации «Эректильная дисфункция» 45, 2025, https://cr.minzdrav.gov.ru/preview-cr/15_3
- Konstantinovsky A, Kuchersky N, Kridin K, Blum A. Improvement in Endothelial Function in Men Taking Phosphodiesterase Type 5 Inhibitors for Erectile Dysfunction. Am J Med. 2023 Oct;136(10):1041-1043. doi: 10.1016/j.amjmed.2023.07.010. Epub 2023 Jul 26. PMID: 37506991.
- С.И. Гамидов, Т.В. Шатылко, Н.Г. Гасанов , Н.А. Наумов. Применение тадалафила по требованию при эректильной дисфункции у особых категорий пациентов. «Андрология и генитальная хирургия» 2018(4): 15-20.

DYNL-RU-00356-DOC-03.2026






 Скачать
Скачать









Комментарии