Мочеточниковые стенты: стремление к «святому Граалю»
Автор обзора: Шадёркин Игорь Аркадьевич, к.м.н., уролог, основатель Uroweb.ru.
План обзора
- 1. Эволюция парадигмы внутреннего дренирования верхних мочевыводящих путей
- 2. Доказательная база декомпрессии верхних мочевых путей
- Таблица 1. Сводные доказательные рекомендации по показаниям к стентированию в различных клинических сценариях
- 3. Гемодинамика и оптимизация геометрических параметров
- Таблица 2. Сравнительная эффективность методов подбора длины стента (на основе исследований корреляции длины мочеточника и роста)
- 4. Биоматериалы, покрытия и патобиология инкрустации: поиск идеального стента
- 5. Злокачественная обструкция мочеточников (MUO)
- Табл. 3. Сравнительная биомеханическая и клиническая эффективность стратегий стентирования при злокачественной обструкции мочеточника
- 6. Гестационная урология: управление экстремальным метаболизмом при беременности
- 7. Стент-ассоциированные симптомы (SRSs): фармакологическое управление
- Табл. 4. Доказательная база фармакологического управления стент-ассоциированными симптомами на основе сетевых метаанализов
- 8. Перспективы и передовые технологии диагностики: эпоха искусственного интеллекта
- 9. Выводы
- 10. Литература
1. Эволюция парадигмы внутреннего дренирования верхних мочевыводящих путей
С момента первого описания эндоскопического стентирования мочеточника силиконовой трубкой, выполненного Zimskind и соавторами в 1967 году, данная процедура стала фундаментальным краеугольным камнем эндоурологии и реконструктивной хирургии мочевыводящих путей [1]. Внедрение мочеточниковых стентов (в частности, стентов типа «double-J» или «pigtail») радикально изменило подходы к лечению обструкции мочевых путей, позволив урологам эффективно купировать почечную колику, обеспечивать адекватный пассаж мочи в обход препятствий, восстанавливать просвет мочеточника после реконструктивных вмешательств и предотвращать развитие угрожающего жизни уросепсиса [2]. Тем не менее, как справедливо отмечается в современной научной литературе, введение любого инородного тела в высокочувствительный и динамичный орган, которым является мочеточник, представляет собой так называемый «обоюдоострый меч» [2, 3].
С одной стороны, стент спасает функцию почки, обеспечивая ее декомпрессию. С другой стороны, он неминуемо инициирует сложный каскад патофизиологических реакций. К ним относятся механическое раздражение механорецепторов уротелия, рефлюкс мочи из мочевого пузыря в почку при повышении внутрипузырного давления, спазм гладкой мускулатуры, а также высокий риск колонизации поверхности стента микроорганизмами с последующей массивной инкрустацией [3]. Исторически урологическая практика опиралась на упрощенный, эмпирический подход, при котором выбор диаметра, длины и биоматериала стента диктовался преимущественно наличием конкретных расходных материалов на складе клиники, а не индивидуальными анатомо-физиологическими и метаболическими особенностями пациента. Такой подход приводил к тому, что более 80% пациентов в послеоперационном периоде сталкивались с выраженными стент-ассоциированными симптомами, включающими дизурию, поллакиурию, макрогематурию, тазовую боль и снижение качества жизни. Кроме того, экономическое бремя, связанное с лечением осложнений (например, удалением «забытых» и инкрустированных стентов), оказалось колоссальным. Лечение тяжелой инкрустации требует проведения нескольких этапов оперативных вмешательств и может обходиться системе здравоохранения в 6–21 раз дороже, чем рутинное удаление неосложненного стента [4].
В течение последнего десятилетия произошел фундаментальный сдвиг мнений в сторону прецизионной, персонифицированной медицины. Благодаря накоплению массива данных доказательной медицины — в первую очередь, обновленных клинических рекомендаций Европейской ассоциации урологов (EAU 2024–2025 гг.), Американской урологической ассоциации (AUA), а также детальных метаанализов и рандомизированных контролируемых исследований (РКИ) — сформировался строго научный подход к выбору метода декомпрессии [5, 6, 7].
Фундаментальные критерии персонифицированного подбора в современной парадигме включают этиологию обструкции (доброкачественная, злокачественная, ятрогенная травма), ожидаемую продолжительность дренирования (дни, недели или пожизненно), метаболический статус пациента (например, беременность, склонность к агрессивному камнеобразованию, гиперурикемия), а также точные анатомические параметры мочевыводящих путей. Глубокое понимание биомеханики стентов, их радиальной компрессионной жесткости, гидродинамики экстра- и интралюминального потока, а также молекулярного взаимодействия новейших полимерных и металлических биоматериалов с уротелием является критическим фактором для минимизации осложнений и обеспечения максимального качества жизни пациентов [8, 9, 10].
2. Доказательная база декомпрессии верхних мочевых путей
Принятие клинического решения об установке мочеточникового стента должно базироваться на строгих критериях доказательной медицины, где ожидаемая польза от внутреннего дренирования неоспоримо и многократно превышает риск развития инфекционно-воспалительных осложнений и стент-ассоциированной симптоматики. Международные (EAU, AUA) и российские клинические рекомендации четко стратифицируют сценарии, требующие обязательного стентирования, ситуации, допускающие вариативность, и те случаи, где от установки стента следует категорически отказаться (таблица 1).
2.1. Эндоскопическое лечение мочекаменной болезни
Согласно самым актуальным руководствам EAU (версия 2024–2025 гг.) и AUA, аксиома обязательного завершения любой эндоскопической операции установкой стента признана устаревшей [6]. Рутинное стентирование после неосложненной ретроградной уретерореноскопии (URS) не рекомендуется (сильная рекомендация с уровнем доказательности 1a) [6]. Масштабные мультицентровые рандомизированные клинические испытания, проведенные с 2019 по 2024 год (включающие такие центры, как University of California, Vanderbilt University и Indiana University), убедительно доказали, что отказ от стентирования при неосложненной URS не снижает показатели частоты полного избавления от камней (SFR) и не увеличивает частоту отсроченных стриктур, однако достоверно избавляет пациента от послеоперационной боли, дизурии и необходимости повторного визита для удаления стента [11]. Аналогичным образом, после проведения дистанционной ударно-волновой литотрипсии (SWL) превентивная установка стента перед процедурой не снижает риск формирования «каменной дорожки» и не улучшает показатели отхождения фрагментов, но достоверно повышает вероятность развития изнурительных симптомов нижних мочевыводящих путей, в связи с чем она признана нецелесообразной (Уровень доказательности B) [12-14].
Несмотря на стремление к минимизации использования инородных тел, существует спектр абсолютных показаний к обязательному внутреннему дренированию мочеточника. AUA и EAU строго регламентируют установку стента в следующих клинических сценариях:
- Выполнение двусторонних эндоскопических оперативных вмешательств (для предотвращения острой двусторонней обструкции отеком и развития анурии) [12-14].
- Хирургическое лечение на анатомически или функционально единственной почке [6].
- Наличие сопутствующей инфекции на фоне обструкции, подозрение на уросепсис или развитие почечной недостаточности (повышение уровня креатинина) [6]. В случае инфицированного гидронефроза любая активная литотрипсия должна быть отложена; приоритетом является экстренная декомпрессия собирательной системы с помощью стента или перкутанной нефростомы, и лишь после полного излечения инфекции соответствующим курсом антибиотикотерапии возможно проведение окончательного хирургического удаления конкремента [13].
- Интраоперационная перфорация или выраженная травматизация мочеточника во время эндоскопического вмешательства [15].
В контексте подготовки к сложным эндоскопическим вмешательствам, таким как ретроградная интраренальная хирургия (RIRS) по поводу крупных коралловидных камней, предварительное стентирование продемонстрировало высокую клиническую ценность (Уровень доказательности 1a) [6]. Данная тактика способствует пассивной дилатации мочеточника в течение 1–2 недель, что значительно облегчает последующее проведение мочеточниковых кожухов (UAS) большого диаметра, снижает внутрилоханочное давление во время операции, уменьшает время процедуры и повышает общую эффективность фрагментации камней [10]. Особенно критична эта стратегия для пациентов, получающих непрерывную антикоагулянтную или антиагрегантную терапию, у которых снижение риска интраоперационных кровотечений и травм мочеточника имеет первостепенное жизненное значение [7].
2.2. Урогенитальная травма и реконструктивная хирургия
При ведении урологических травм тактика стентирования зависит от гемодинамической стабильности пациента и степени повреждения. Согласно рекомендациям EAU по урогенитальной травме (2024–2025 гг.), гемодинамическая стабильность является первичным критерием для выбора неоперативного ведения [5]. При стабильных, бессимптомных травмах почки 4-й степени стентирование мочеточника не является необходимым [5]. Текущие доказательные базы предполагают вмешательство (установку мочеточникового стента, нефростомы или периренальное дренирование) исключительно в тех случаях, когда у пациентов развиваются симптомы, связанные с продолжающимся затеком мочи (уринома): боль в боку, лихорадка, нарастающий лейкоцитоз [5].
Однако при огнестрельных ранениях контузия мочеточника является частым явлением. В таких случаях, если интактный, но контуженный мочеточник выявляется во время лапаротомии, первичным методом выбора является его внутреннее стентирование для предотвращения отсроченной стриктуры или некроза с экстравазацией мочи [15]. В гинекологической и тазовой хирургии при первичном выявлении уретеровагинальных свищей установка стента является методом первой линии; современные исследования демонстрируют успешность такого малоинвазивного консервативного излечения (без необходимости реимплантации) на уровне от 64% до 100% [15]. В случаях, когда установка стента технически невозможна или не обеспечивает адекватного оттока мочи (например, при продолжающемся росте уриномы или появлении гнойного отделяемого), международные протоколы требуют немедленного выполнения перкутанной нефростомии (PCN) для экстренной декомпрессии [15].
2.3. Интеграция с российскими клиническими рекомендациями
Российские национальные клинические рекомендации полностью солидарны с международными протоколами в вопросах декомпрессии верхних мочевыводящих путей при обструкции и инфекции, однако вносят важные уточнения относительно абсолютных противопоказаний к процедуре трансуретрального стентирования [16]. В отечественной практике стентирование мочеточника ретроградным путем строго противопоказано:
- На фоне острого воспалительного процесса (в фазе экссудации) в любом из органов малого таза.
- При наличии сопутствующей острой травмы уретры, которая сопровождается уретроррагией (кровотечением из мочеиспускательного канала), формированием гематомы промежности и острой задержкой мочи. В таких ургентных ситуациях, во избежание генерализации инфекции или усугубления травмы нижних мочевыводящих путей, приоритет безоговорочно отдается антеградным методам декомпрессии (чрескожной пункционной нефростомии).
Таблица 1. Сводные доказательные рекомендации по показаниям к стентированию в различных клинических сценариях.
|
Клиническая ситуация |
Статус стентирования |
Уровень доказательности / Источник |
|
Неосложненная уретерореноскопия (URS) |
Не рекомендуется (Стент не устанавливается) |
Сильная рекомендация, LE 1a (EAU, AUA) [6] |
|
Дистанционная литотрипсия (SWL) |
Не рекомендуется рутинно |
EAU, AUA [12-14] |
|
Единственная почка / Двусторонняя URS |
Строго показано (Обязательное стентирование) |
Сильная рекомендация (EAU, AUA) [12-14] |
|
Обструкция с сопутствующей инфекцией |
Экстренная декомпрессия (Стент или PCN) |
Жизненные показания [6] |
|
Уретеровагинальный свищ |
Первая линия терапии (Успех 64-100%) |
AUA [15] |
|
Травма уретры с гематомой/уретроррагией |
Абсолютно противопоказано (Трансуретрально) |
Российские клинические рекомендации [16] |
3. Гемодинамика и оптимизация геометрических параметров
Традиционно выбор геометрических характеристик стента (диаметра и длины) оставался субъективным решением хирурга, основанным на личном опыте. Однако гидродинамика верхних мочевыводящих путей при наличии стента подчиняется сложным физическим законам, и последние масштабные метаанализы демонстрируют, что именно эти параметры оказывают критическое прямое влияние на качество жизни пациента в послеоперационном периоде.
3.1. Диаметр стента
Долгие годы в урологическом сообществе доминировало мнение «больший просвет обеспечивает лучший дренаж», что приводило к повсеместному использованию стентов диаметром 6 Fr и 7 Fr. В основе этого заблуждения лежало прямолинейное применение закона Пуазейля к внутрипросветному потоку. Однако физиология дренирования почки стентированным мочеточником устроена сложнее: отток мочи происходит не только интралюминально, но в значительной степени и экстралюминально — по наружной поверхности стента в естественном просвете мочеточника между полимерной стенкой и уротелием.
Клинические исследования и системные обзоры последних лет убедительно доказывают, что стенты меньшего калибра (4.8 Fr или 5 Fr) значительно превосходят стенты диаметром 6 Fr по показателям субъективной переносимости, при этом абсолютно не уступая им в клинической эффективности дренирования [10]. Применение стентов диаметром 4.8 Fr ассоциировано с достоверно меньшей выраженностью стент-ассоциированных симптомов. В сравнительных исследованиях средний балл по валидированной шкале USSQ (Ureteric Stent Symptoms Questionnaire) у пациентов с тонкими стентами составлял 47,0 ± 4,5 против 53,9 ± 4,2 у пациентов со стентами 6 Fr (p < 0,001) [17]. Интенсивность послеоперационной боли по Визуальной аналоговой шкале (ВАШ) также достоверно ниже в группе 4.8 Fr (1,4 ± 0,7 против 2,2 ± 0,8; p < 0,001) [17].
Дискомфорт и болевой синдром возрастают пропорционально наружному диаметру устройства. Это связано с тем, что толстый стент вызывает более выраженное механическое растяжение мышечной оболочки мочеточника, приводит к компрессии микроциркуляторного русла, ишемизации подслизистого слоя и постоянному раздражению нервных окончаний [10]. При этом частота серьезных ранних урологических осложнений — таких как миграция стента, обструкция, экстравазация мочи или развитие острой инфекции мочевыводящих путей (ИМП) — остается абсолютно идентичной для обоих диаметров [17]. Кроме того, исследования сексуальной функции (один из наиболее уязвимых доменов качества жизни у таких пациентов) показали значительное ее снижение на фоне стентирования, причем негативный эффект был тем сильнее, чем больше был диаметр стента [18-20].
Таким образом, рутинное использование малокалиберных стентов (4.8 Fr или 5 Fr) является научно обоснованной стратегией выбора для улучшения послеоперационного комфорта пациентов (особенно лиц молодого возраста) после эндоскопических литотрипсий. Исключением являются специфические ситуации, например, необходимость максимальной пассивной предварительной дилатации мочеточника (предстентирование) перед последующим использованием мочеточникового кожуха большого калибра (UAS 12/14 Fr) при сложной ретроградной интраренальной хирургии. В таких случаях стент 6 Fr может в большей степени облегчить последующее проведение инструмента и сократить оперативное время второго этапа.
3.2. Оптимальная длина стента
Несоответствие длины стента анатомической длине мочеточника является независимым и мощным предиктором тяжелых осложнений. Слишком короткий стент имеет крайне высокий риск проксимальной миграции (ухода стента вверх, в полостную систему почки), что потребует повторной уретероскопии для его извлечения [1]. Напротив, чрезмерно длинный стент образует избыточные петли в полости мочевого пузыря. Если дистальный завиток стента пересекает среднюю линию мочевого пузыря, он вызывает постоянное механическое раздражение богатой механорецепторами зоны треугольника Льето, что приводит к мучительной поллакиурии, императивным позывам, макрогематурии и тазовой боли [1].
Парадоксально, но интраоперационное прямое эндоскопическое измерение длины мочеточника с помощью измерительных катетеров или градуированных проводников часто приводит к грубым клиническим ошибкам (таблица 2). Анатомическое объяснение этому кроется в динамических свойствах самого органа. Обструктивный или длительно дилатированный (на фоне камня) мочеточник характеризуется избыточной извитостью и патологическим удлинением. Непосредственно после установки стента происходит устранение обструкции, пассаж мочи восстанавливается, и изгибы расправляются. Исследования динамического натяжения (как в исторических экспериментах in vivo, так и в клинических наблюдениях) показывают, что мочеточник способен значительно укорачиваться под влиянием ригидной выпрямляющей трубки стента [21, 22]. В результате проспективных исследований выяснилось, что стент, длина которого была математически точно рассчитана по прямому интраоперационному измерению, в послеоперационном периоде оказывается избыточно длинным в 83% случаев, и лишь в 17% случаев метод предсказывает идеальную длину [22].
Доказательная медицина однозначно свидетельствует, что рост пациента является наиболее надежным, простым и эффективным предиктором идеальной длины стента, поскольку рост напрямую коррелирует с общей длиной туловища и полностью нивелирует влияние локальной извитости и временного растяжения мочеточника [1].
В мировой клинической практике широко используется формула Wieder для точного подбора длины у взрослых[23, 24]:
Длина стента (в см) = рост пациента (в дюймах) – 42.
Для педиатрической практики исторически применяется иная метрика, длина мочеточника рассчитывается по формуле [22]:
Возраст ребенка в годах + 10 см.
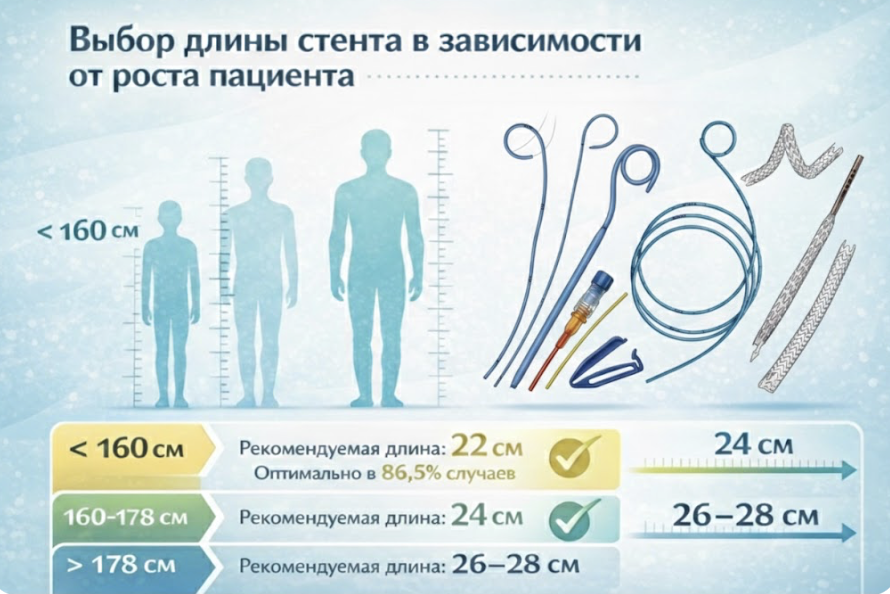
Альтернативным, еще более простым подходом для взрослых пациентов является категоризация по росту [22]. Исследование с участием 408 пациентов показало высокую валидность следующих параметров (рис. 1):
- Для пациентов с ростом менее 160 см наиболее подходящим является стент длиной 22 см (он оказался оптимальным в 86,5% случаев в данной подгруппе).
- Для пациентов с ростом 160–178 см идеальным является стент 24 см.
- Для пациентов высокого роста (выше 178 см) необходимы стенты 26–28 см.
Рис. 1. Выбор длины стента в зависимости от роста пациента.
Применение этих простых антропометрических корреляций позволяет точно позиционировать дистальный завиток, минимизировать внутрипузырный объем инородного материала и существенно (до 61% идеального попадания) снизить риск ирритативных симптомов по сравнению с прямым измерением [22].
Таблица 2. Сравнительная эффективность методов подбора длины стента (на основе исследований корреляции длины мочеточника и роста).
|
Метод подбора длины стента |
Точность попадания в оптимальный размер (Grade 0) |
Риск установки избыточно длинного стента |
|
Антропометрический (по росту / формула Wieder) |
61% |
Низкий |
|
Прямое интраоперационное эндоскопическое измерение |
17% |
83% |
4. Биоматериалы, покрытия и патобиология инкрустации: поиск идеального стента
«Святой Грааль» эндоурологии.
Он должен обладать абсолютной биосовместимостью, полной устойчивостью к инкрустации солями мочи, резистентностью к формированию бактериальных биопленок, достаточной радиальной прочностью для предотвращения внешнего коллапса (например, при опухолях) и, одновременно, высокой термочувствительной гибкостью для минимизации болевого синдрома [3]. Поскольку ни один из существующих на рынке материалов не удовлетворяет всем этим противоречивым физическим требованиям одновременно, глубокое понимание патофизиологии взаимодействия поверхности стента с мочой является ключевым для клинического выбора.
4.1. Патофизиология инкрустации
Инкрустация (обызвествление) стента представляет собой неизбежный, многоступенчатый и многофакторный биохимический процесс. Непосредственно в первые часы после установки поверхность любого инородного материала покрывается так называемой кондиционирующей пленкой [3]. Эта молекулярная пленка состоит из белков мочи (альбумин, уромодулин), электролитов и макромолекул [25]. Кондиционирующая пленка кардинально модифицирует поверхностное натяжение и электростатический заряд полимера, создавая идеальный питательный плацдарм для адгезии уропатогенных бактерий [25].
В норме кристаллизация подавляется благодаря наличию в моче ингибиторов (цитрат, магний), однако при колонизации стента бактериями баланс рушится. Бактерии, вырабатывающие фермент уреазу (в первую очередь Proteus mirabilis, Klebsiella spp., Enterococcus spp., Pseudomonas aeruginosa), расщепляют присутствующую в моче мочевину до аммиака и углекислого газа. Это приводит к резкому локальному защелачиванию мочи (повышению pH). В щелочной среде происходит перенасыщение и стремительная преципитация кристаллов магний-аммоний-фосфата (струвита) и карбонат-апатита непосредственно на бактериальном матриксе [3]. In vitro испытания в 37°C литогенной искусственной моче (AUE) доказали, что этот процесс запускается мгновенно [3]. Параллельно, даже в абсолютно стерильной моче, при наличии метаболических нарушений у пациента (гиперкальциурия, гипероксалурия, гиперурикемия) может происходить прямая кристаллизация оксалата кальция и мочевой кислоты на полимерной матрице [25].
Риск массивной инкрустации экспоненциально возрастает при длительном нахождении стента в мочевых путях, при наличии сопутствующей инфекции, рецидивном камнеобразовании в анамнезе (мочекаменная болезнь), а также у пожилых пациентов (в связи с дисфункцией мочевого пузыря и нарушением опорожнения) и беременных женщин [25]. Доказано, что черное окрашивание удаленных стентов строго коррелирует с пролонгированным сроком стояния и ИМП, вызванными Escherichia coli и Klebsiella spp. (p < 0.001) [26, 27]. Бессимптомная бактериурия на фоне стента развивается неизбежно, и международные клинические рекомендации прямо указывают, что рутинное лечение стент-ассоциированной бессимптомной бактериурии антибиотиками не приносит пользы и не рекомендуется [28].
4.2. Выбор базовых полимеров и оценка инновационных покрытий
Метаанализы, оценивающие базовые структурные материалы стентов, показывают, что более мягкие эластомеры, такие как 100% силикон, предпочтительнее жесткого полиуретана или Перкуфлекса (Percuflex) для снижения выраженности симптомов нижних мочевыводящих путей и микрогематурии [8]. Однако сама по себе жесткость базового материала не оказывает статистически значимого влияния на снижение частоты инкрустации (Отношение шансов (OR): 0,97; p=0,17) [8].
Для модификации поверхности стентов в последние годы активно применяются высокотехнологичные покрытия, однако их реальная клиническая эффективность варьирует:
4.2.1. Гидрофильные покрытия (гидрогели)
Нанесение гидрофильных гидрогелей (например, в стентах COOK Universa Soft) значительно снижает коэффициент трения поверхности стента, облегчая его установку и извлечение. Во влажной среде они создают смазывающий слой. Клинические исследования демонстрируют, что гидрофильные стенты достоверно улучшают качество жизни (QoL): 60% пациентов с гидрофильными стентами не сообщали о послеоперационной боли по сравнению с 7,5% в группе стандартных непокрытых стентов (p < 0,001). Тем не менее, длительное ингибирование бактериальной адгезии исключительно за счет гидрофильности в условиях in vivo остается под вопросом — гидрофильный гель сам по себе не способен полностью предотвратить рост биопленок [2, 29].
4.2.2. Гепариновое покрытие
Гепарин обладает сильным суммарным отрицательным ионным зарядом, который отталкивает клетки уротелия, белки и бактерии. Сравнительные исследования in vivo (электронная микроскопия и спектрофотометрия) у одних и тех же пациентов, которым устанавливали один гепариновый и один обычный полиуретановый стент (при двусторонней обструкции), показали впечатляющие результаты. На гепарин-покрытых стентах слой инкрустации образуется значительно тоньше (в среднем 8,5 мкм против 17,0 мкм на непокрытом полиуретане), а площадь поражения кратно меньше [3]. Гепариновые стенты (например, BraidStent-H) демонстрируют высокую резистентность к инкрустации на протяжении как минимум 6 недель [30].
4.2.3. Антимикробные покрытия (наночастицы серебра, триклозан)
Хотя in vitro эти покрытия демонстрируют блестящую способность нарушать биосинтез бактериальных жирных кислот и убивать микроорганизмы, их перенос в клиническую практику не стал выходом. Масштабные метаанализы не выявили статистически значимого снижения частоты клинически выраженных ИМП (OR: 1,67; p=0,99) или предотвращения инкрустации (OR: 1,26; p=0,52) при применении антибактериальных покрытий у реальных пациентов [8]. Белки мочи быстро инактивируют эти агенты.
В качестве революционного направления обозримого будущего рассматриваются полностью биодеградируемые мочеточниковые стенты (Biodegradable Ureteral Stents, BUS), созданные на основе природных (альгинаты, хитозан) или синтетических полимеров (полигликолевая кислота, полилактид) [31]. Главная их клиническая концепция заключается в полном устранении экзистенциальной проблемы «забытого стента» и исключении необходимости проведения дорогостоящей и дискомфортной повторной цистоскопии для его удаления [31]. Главным вызовом для инженеров сейчас является строгий контроль скорости деградации полимеров: стент должен поддерживать просвет не менее 3-6 недель, а затем раствориться в моче без образования крупных обструктивных фрагментов, способных вызвать вторичную почечную колику [30]. Технология активно проходит клинические испытания.
5. Злокачественная обструкция мочеточников (MUO)
Злокачественная компрессия мочеточников (Malignant Ureteral Obstruction, MUO) — тяжелое состояние, возникающее вследствие роста первичных опухолей уротелия, инвазии экстраорганных опухолей малого таза (рак шейки матки, колоректальный рак, рак предстательной железы), ретроперитонеального лимфатического метастазирования или выраженного лучевого фиброза после радиотерапии [32, 33]. Ведение MUO представляет собой наиболее сложную биомеханическую задачу для уролога [34]. Пациенты с MUO часто имеют паллиативный статус и ожидаемую продолжительность жизни менее 1 года, поэтому сохранение почечной функции для проведения химиотерапии и улучшение качества жизни выходят на первый план [32].
Внешнее гидростатическое и тканевое давление на стенку мочеточника при злокачественном росте многократно превышает радиальное компрессионное напряжение, которое способны выдержать стандартные полимерные стенты [9]. Глубокий анализ неудач дренирования (на основе 10-летнего исследования 150 пациентов и 556 процедур стентирования) наглядно демонстрирует эту проблему. Стандартные тонкостенные полиуретановые стенты (например, Vortek 7Fr, обладающие низким радиальным напряжением 1.4 N·mm⁻²) терпят неудачу и сдавливаются опухолью в 34,2% случаев в среднем через 4,3 месяца [9]. Стенты из более плотных полимеров (Urosoft 7-8Fr, напряжение ~2,8 N·mm⁻²) демонстрируют еще более высокую частоту обструкции — до 42,9% за 5,1 месяца [9].
Установлено, что сохранение большого внутреннего просвета стента является критическим фактором оттока (вероятность отказа снижается на 71% при увеличении просвета на каждый 1 мм), однако именно механическая жесткость стента (радиальная резистентность) служит тем единственным щитом, который способен удержать этот просвет открытым в условиях растущей опухоли. Применение сверхжестких армированных полимерных катетеров (Superglide 8Fr, радиальное напряжение 5,4 N·mm⁻²) снижает частоту неудач до приемлемых 15,4% [9].
При исчерпании возможностей одиночных полимерных стентов, урологический алгоритм предписывает переход к специализированным, высокотехнологичным методикам.
5.1. Тандемное стентирование
Инновационная методика одновременной установки сразу двух полимерных стентов (например, двух стентов 8 Fr) в один пораженный мочеточник [9]. Технически это выполняется путем введения сверхжесткого и жесткого струнных проводников и параллельного проведения стентов (один из которых часто укорачивается, чтобы лишь слегка выступать в мочевой пузырь). Такая геометрия формирует колоссальный суммарный просвет (до 3,2 мм) и критически увеличивает общую радиальную жесткость конструкции. Два стента физически препятствуют перегибу друг друга под действием внешних сил. Метаанализы и крупные когортные исследования демонстрируют падение частоты неудач при тандемном стентировании до беспрецедентных 6,5% – 13% при сохранении адекватного дренажа в течение 5 месяцев [9].
5.2. Саморасширяющиеся металлические стенты (MUS)
Устройства из специальных нитиноловых или иных металлических сплавов (Resonance, Allium, Memokath, Uventa, спиральные Metal-mesh) разработаны специально для противостояния экстремальной злокачественной компрессии [32]. Их первичная проходимость достигает 91,2-95% [35, 36, 37]. Медиана продолжительности функционирования без необходимости замены для металлических стентов составляет более 6,2 – 12 месяцев (по сравнению с 3 месяцами для полимерных) [37]. В 90% случаев перевод пациента на металлический стент приводит к стабилизации гидоуретеронефроза и снижению креатинина [38]. Доказанными факторами риска досрочного отказа металлического стента являются локализация обструкции в абдоминальном отделе мочеточника (p = 0,0279) и наличие массивного лимфатического метастазирования вокруг мочеточника (p = 0,0398) [35].
5.3. Фармакоэкономический аспект при MUO
Несмотря на то, что первоначальная стоимость самого металлического стента значительно выше полимерного аналога, фармакоэкономический анализ прямых медицинских затрат и QALY (Quality-Adjusted Life Year) демонстрирует их высочайшую рентабельность на длинной дистанции [39] (рис. 2). Отказ от необходимости подвергать тяжелого онкологического больного процедуре замены стента каждые 3 месяца экономит колоссальные средства на операционное время, расходные материалы, наркоз и пребывание в стационаре. Расчетная годовая стоимость ведения пациента на полимерных стентах (с заменой каждые 90 дней) составляет от 9648 до 13128 долларов США. Применение металлических стентов, функционирующих медианно 288 дней и более, радикально снижает эти затраты до 4,211 – 5,313 долларов США в год [40].
Рис. 2. Рынок мочеточниковых стентов 2024-2032 г. [Ureteral Stents Market Size & Share 2024 – 2032 Market Size by Product Type (Double Pigtail, Open-Ended, Close-Ended, Multiloop), by Application (Kidney Stones, Kidney Transplant, UTI), by Material (Metal, Polyurethane, Silicon, Hydrogel) Report ID: GMI8522. Published Date: March 2024]
Доля прямых расходов пациента при использовании металлических стентов также ниже (21,6% против 25,4% от общих затрат) [39]. Прирост QALY для металлических стентов (Resonance) на первый, второй и третий годы терапии неизменно превышает показатели полимерных стентов (+0,022, +0,034, +0,041 соответственно) [41]. Таким образом, у паллиативных онкологических пациентов металлические стенты не только значительно улучшают качество дожития, но и снижают финансовую нагрузку на систему здравоохранения (таблица 3) [39].
Табл. 3. Сравнительная биомеханическая и клиническая эффективность стратегий стентирования при злокачественной обструкции мочеточника.
|
Тип стента при MUO |
Радиальное напряжение / Жесткость |
Уровень неудач (Failure Rate) |
Медиана времени до отказа |
Рекомендации по замене |
|
Стандартный полимерный (Vortek, 7Fr) |
Низкая (1,4 N·mm⁻²) |
34,2% |
~4,3 месяца |
Каждые 3 месяца |
|
Усиленный полимерный (Superglide, 8Fr) |
Высокая (5,4 N·mm⁻²) |
15,4% |
~4,0 месяца |
Каждые 3-6 месяцев |
|
Тандемные стенты (2 × 8Fr) |
Очень высокая |
6,5% - 13% |
~5,0 месяцев |
При неэффективности одиночных |
|
Металлические стенты (Resonance, Allium) |
Экстремально высокая |
< 10% в первые 6 мес |
6-12+ месяцев |
Длительное паллиативное дренирование |
Доброкачественные стриктуры мочеточника и реконструктивный контекст
Для лечения рецидивирующих доброкачественных стриктур мочеточника — возникающих вследствие предшествующей уретеропластики (40,8% случаев), вклиненных камней (29,1%), лучевой терапии, травм малого таза или ишемии трансплантата почки (17,4%) — эндоскопический подход с применением саморасширяющихся металлических стентов (MUS, таких как Allium, покрытых биосовместимым полимером) зарекомендовал себя как высокоэффективная малоинвазивная альтернатива сложным открытым или лапароскопическим реконструктивным операциям. Это особенно актуально для пациентов старшего возраста или лиц с тяжелой сопутствующей патологией [42, 43].
Проспективные клинические исследования (с анализом сотен наблюдений) показывают, что общий показатель клинического успеха металлических стентов составляет 71,7% – 85,5% при длительном медианном наблюдении в 18–24 месяца. Успешное стентирование приводит к впечатляющему физиологическому восстановлению: средний объем гидронефроза снижается с 68,9 до 32,1 см³, уровень креатинина крови - с 103,7 до 94,4 мкмоль/л, а азот мочевины — с 6,7 до 5,1 ммоль/л [42, 43, 44].
Примечательно, что успех напрямую зависит от этиологии и анатомии стриктуры. Наивысшие показатели эффективности (78,2%) отмечены при лечении ишемических стриктур после трансплантации почки. Это обусловлено тем, что стриктура трансплантата обычно короче, а сам трансплантированный мочеточник имеет малую длину. В результате длинный металлический стент (длиной 10 или 12 см) способен перекрыть стриктуру с необходимым запасом опоры (не менее 2 см здоровых тканей с каждой стороны от сужения), что радикально снижает частоту миграции до 10,9% [42]. Важно отметить, что баллонная дилатация перед установкой стента в трансплантат проводится более щадяще — до 20 атмосфер (1,72 МПа) по сравнению с 25 атмосферами в нативном мочеточнике. Хуже всего поддаются эндоскопическому лечению рецидивные стриктуры после предшествующей хирургической уретеропластики (успех 67,6%) из-за выраженных патологических колебаний внутреннего диаметра мочеточника [42-44].
Главным «ахиллесовой пятой» и самым частым осложнением при применении полностью интралюминальных металлических стентов (в отличие от double-J) является их миграция, достигающая 20% – 27,5% случаев. Миграция требует повторной уретероскопии для репозиции (удалось в 33 из 53 случаев) или полной замены стента. Многофакторный анализ показал, что единственным независимым дооперационным предиктором миграции металлического стента Allium является низкий показатель скорости клубочковой фильтрации (GFR) ипсилатеральной почки [44]. При этом частота окклюзии (2,3%) и инкрустации (1,9–20%) для полимер-покрытых металлических стентов остается весьма приемлемой для долгосрочных устройств [42].
6. Гестационная урология: управление экстремальным метаболизмом при беременности
Ведение беременных пациенток с обструктивной уропатией (вследствие нефролитиаза или физиологического гидронефроза) требует ювелирного баланса между сохранением функции почек матери и предотвращением угроз для развивающегося плода. При беременности в организме женщины происходят глубокие физиологические и анатомические изменения. Дилатация мочеточников обусловлена как механической компрессией растущей маткой (преимущественно справа), так и расслабляющим действием высоких доз прогестерона. Одновременно с этим, повышение скорости клубочковой фильтрации (GFR) приводит к массивной абсорбтивной гиперкальциурии и гиперурикозурии [4]. Этот уникальный «пролитогенный» метаболический статус, в сочетании с изменениями pH мочи, превращает поверхность любого мочеточникового стента в гиперактивный центр кристаллизации с беспрецедентной скоростью [4].
Главной клинической догмой стентирования при беременности является жесточайший контроль сроков нахождения инородного тела. Клинические исследования демонстрируют, что частота инкрустации стента у беременных возрастает экспоненциально в зависимости от времени. Если при нахождении стента в мочевыводящих путях менее 6 недель уровень выявляемой инкрустации составляет 26,8%, то при превышении срока индукции в 12 недель этот показатель достигает катастрофических 75,9%. Оставленный, или «забытый», стент ведет к тотальной обструкции, тяжелым ИМП, прогрессирующей потере функции почки, угрозе уросепсиса и прямым акушерским рискам (преждевременные роды, влияние на рост плода). Таким образом, абсолютный международный консенсус требует обязательной превентивной замены или удаления стента каждые 4–6 недель в течение всей беременности [4].
Дооперационное планирование, диагностика и мониторинг состояния стента у беременных имеют строгие радиационные ограничения. Применение КТ (даже низкодозных протоколов) и обзорной рентгенографии (KUB) крайне нежелательно. Тератогенные эффекты облучения плода наиболее высоки в период между 8-й и 20-й неделями гестации (порог тератогенеза составляет около 5 рад или 50 мГр). Однако риск радиационного канцерогенеза для плода вообще не имеет безопасного порога [11-14]. В связи с этим радиационные методы должны применяться только при прямой угрозе жизни. Золотым стандартом и первой линией визуализации является ультразвуковое исследование (включая трансабдоминальное и трансвагинальное) [4].
Дифференциальная диагностика неосложненного физиологического гидронефроза беременных от истинной патологической обструкции (камнем или инкрустированным стентом) проводится с помощью цветового допплеровского картирования. Ключевыми параметрами являются измерение индекса резистентности (RI = [пиковая систолическая скорость − конечная диастолическая скорость] / пиковая систолическая скорость) почечных артерий и выявление так называемого артефакта мерцания, который высокоспецифичен для кальцификации поверхности double-J стента [4].
При развитии выраженной инкрустации стента управление ситуацией должно осуществляться мультидисциплинарной командой, включающей опытных эндоурологов, акушеров-гинекологов и анестезиологов. Перед вмешательством тяжесть инкрустации обязательно классифицируется по валидированным системам: FECal (пять степеней — от I, минимального налета, до V, тотального обызвествления завитков и тела стента) или V-GUES [4]. Эта градация позволяет рассчитать каменную нагрузку и выбрать инструмент.
При невозможности извлечения стента стандартным цистоскопом категорически запрещается применение физической силы (тракции) во избежание полного отрыва (авульсии) мочеточника [4].
Методом абсолютного выбора для безопасного пошагового освобождения застрявшего стента является уретерореноскопия (URS) — ригидная или гибкая (RIRS) — с применением контактной Гольмиевой лазерной литотрипсии (Ho:YAG). Хирург всегда начинает с освобождения нижних фрагментов в мочевом пузыре, затем продвигается по мочеточнику и в конце высвобождает почечный завиток [4]. Использование гольмиевого лазера через полужесткий уретероскоп признано высокоэффективным и абсолютно безопасным на любых сроках беременности. Лазер доставляет энергию крайне локально, не вызывая коллатерального термического повреждения соседних тканей и не оказывая никакого негативного влияния на плод (в том числе акустического воздействия, вызывающего глухоту новорожденных). Дистанционная ударно-волновая литотрипсия (ESWL) для фрагментации проксимального завитка стента или почечных камней у беременных строго и абсолютно противопоказана ввиду доказанного риска внутриутробной гибели плода, повреждения плаценты и индукции преждевременных родов [4].
Если пациентка находится в третьем триместре и анестезиологические риски для проведения эндоскопического вмешательства (URS) оцениваются как неприемлемо высокие, предпочтение следует отдать чрескожной пункционной нефростомии (PCN). Под местной анестезией PCN является более безопасной, выполнимой и эффективной альтернативой внутреннему стентированию при симптоматическом гидронефрозе, значительно снижая риск необходимости повторных травматичных вмешательств до родов.
7. Стент-ассоциированные симптомы (SRSs): фармакологическое управление
Несмотря на колоссальные успехи в оптимизации диаметра, длины, применения гидрофильных и антимикробных покрытий стентов, более 80% пациентов продолжают испытывать стент-ассоциированные симптомы (SRSs), которые сильно снижают качество их жизни. Патофизиология SRSs имеет четкую нейромышечную основу. Она базируется на постоянном механическом раздражении механорецепторов дистальным завитком стента в чувствительной зоне треугольника Льето. Это раздражение через рефлекторные дуги вызывает мощный спазм гладкой мускулатуры предстательной железы, дистального отдела мочеточника и шейки мочевого пузыря (опосредованно через альфа-1D адренорецепторы), а также провоцирует выраженную гиперактивность детрузора (опосредованно через M2 и M3 мускариновые холинорецепторы и бета-3 адренорецепторы).
Детальное понимание этого патогенетического каскада привело к разработке и широкому внедрению мультимодальной фармакотерапии, направленной на блокирование конкретных рецепторных мишеней. EAU настоятельно рекомендует предлагать медицинскую экспульсивную терапию (MET) для лечения стент-ассоциированных симптомов (Сильная рекомендация) [6]. Крупнейший сетевой метаанализ (включающий 16 РКИ и 1865 пациентов) позволил объективно ранжировать эффективность различных препаратов [45]:
7.1. Альфа-адреноблокаторы
Являются препаратами первой линии для расслабления гладкой мускулатуры тазовых органов. Блокируя альфа-1D рецепторы, они купируют спазм дистального отдела мочеточника. Доказано, что их применение значительно снижает выраженность мочеточниковой колики, боли и дизурии. Более того, назначение альфа-блокаторов за неделю до планируемой процедуры URS способствует пассивной дилатации устья мочеточника, облегчая операцию [6]. По данным исследований, тамсулозин (0,2–0,4 мг) стабильно занимает лидирующие позиции по купированию дизурических явлений [46].
7.2. Антимускариновые препараты
Блокируя M2 и M3-холинорецепторы, эти препараты мощно подавляют гиперактивность детрузора мочевого пузыря, вызванную трением стента. Масштабный сетевой метаанализ с байесовским ранжированием (P-score) показал, что монотерапия солифенацином имеет наивысший P-score (0.8484) и вероятность быть абсолютно лучшим препаратом среди всех монотерапий для снижения общего балла по валидированной шкале USSQ; тамсулозин занял в этом рейтинге второе место (0.7054) [45]. Важно отметить, что комбинированная терапия (например, Тамсулозин 0,4 мг + Солифенацин 5 мг) демонстрирует мощнейший синергетический эффект. Воздействуя на два различных патофизиологических пути одновременно, такая комбинация является наиболее эффективной стратегией для контроля как интенсивного болевого синдрома, так и ургентных позывов [46].
7.3. Агонисты бета-3 адренорецепторов
Это инновационный фармакологический подход, позволяющий активно расслабить детрузор в фазу накопления мочи без системных антихолинергических побочных эффектов. Недавние метаанализы (2023–2024 гг.) показывают, что мирабегрон в дозировке 50 мг превосходит антимускариновые препараты в достоверном улучшении симптомов нижних мочевыводящих путей (MD −1,39; p = 0,03) и оценке общего состояния здоровья (MD −1,65; p = 0,0007) [45]. Самое главное преимущество мирабегрона заключается в профиле безопасности: он имеет значительно более низкую частоту развития изнуряющих побочных эффектов. Отношение шансов (OR) для развития запоров при приеме мирабегрона по сравнению с холинолитиками составляет всего 0,10 (p = 0,03), а для сухости во рту — 0,15 [47]. Мирабегрон в настоящее время рассматривается как приоритетная терапия у пациентов, нуждающихся в длительном ношении стента, но плохо переносящих классические холинолитики [47].
7.4. Ингибиторы фосфодиэстеразы 5-го типа (ФДЭ-5)
Применение тадалафила (5–10 мг) оказывает комплексное положительное влияние. За счет накопления цГМФ происходит выраженное расслабление гладкой мускулатуры мочеточника и улучшение микроциркуляции. Тадалафил продемонстрировал высокую эффективность в снижении болевого синдрома (в некоторых исследованиях превосходя тамсулозин) [45]. Но его уникальное преимущество заключается в том, что он демонстрирует наивысшие показатели в улучшении домена сексуальной функции у пациентов со стентами, которая обычно резко снижается при наличии инородного тела [46].
Табл. 4. Доказательная база фармакологического управления стент-ассоциированными симптомами на основе сетевых метаанализов.
|
Фармакологическая группа |
Основной механизм действия при SRS |
Клиническая эффективность и доказательная база |
Специфические клинические преимущества и профиль |
|
Альфа-1D блокаторы |
Блокада α-1D рецепторов гладкой мускулатуры таза |
Снижают боль и дизурию; Первая линия терапии по EAU |
Ускоряют отхождение конкрементов (MET), подготавливают устье к URS |
|
М-холинолитики |
Блокада М2/М3 рецепторов гиперреактивного детрузора |
Наивысший рейтинг (P-score 0.84) в монотерапии для снижения USSQ |
Оптимален в комбинации с тамсулозином. Риск: сухость во рту, запоры |
|
Агонисты β-3 рецепторов |
Активация β-3 рецепторов, прямое расслабление детрузора |
Эффективнее холинолитиков по показателю общего здоровья |
Минимальный риск антихолинергических эффектов (OR 0.10 для запоров) |
|
Ингибиторы ФДЭ-5 |
Накопление внутриклеточного цГМФ, релаксация тканей |
Значительное снижение боли, сравнимое с альфа-блокаторами |
Наилучший результат для сохранения домена сексуальной функции USSQ |
8. Перспективы и передовые технологии диагностики: эпоха искусственного интеллекта
Своевременное выявление начальной инкрустации стента до момента полной блокады почки является сложной диагностической задачей. Обзорная рентгенография часто не позволяет дифференцировать резидуальные камни мочеточника от обызвествления самого полимера. Сегодня превентивное прогнозирование риска инкрустации выходит на абсолютно новый технологический уровень с внедрением систем искусственного интеллекта (AI) и глубокого машинного обучения. Разрабатываются алгоритмы, такие как сверхточные сверточные нейронные сети (Deep-learning CNN, Mask-RCNN), способные в автоматическом режиме анализировать данные низкодозной компьютерной томографии (КТ).
Применение 3D-морфологического анализа на базе нейросетей позволяет сегментировать контур стента с колоссальной точностью до 94,4%, безошибочно дифференцируя кальцификацию самого стента от прилежащих фрагментов конкрементов в мочеточнике. Более того, среднее время компьютерного анализа одного клинического случая составляет всего 12 секунд [48]. Использование таких предиктивных моделей совместно с анализом биохимического профиля мочи пациента позволяет урологам на самых ранних стадиях планировать сочетанные хирургические вмешательства, удалять стент до наступления критической обструкции и предотвращать необратимую потерю почечной функции [48].
9. Выводы
Всесторонний анализ современных научных данных, международных руководств (EAU, AUA) и российских клинических рекомендаций однозначно демонстрирует, что успешность дренирования верхних мочевыводящих путей напрямую зависит от полного отказа от рутинных, шаблонных паттернов в пользу строгой прецизионной медицины.
Алгоритм персонифицированного подбора диктует жесткое соблюдение показаний: следует категорически исключить профилактическое стентирование при неосложненной уретерореноскопии и дистанционной литотрипсии. Ключом к минимизации изнурительных стент-ассоциированных симптомов и предотвращению катастрофических осложнений (таких как тотальная инкрустация, миграция или постренальная анурия) является тщательный индивидуальный подбор физических параметров устройства. Безоговорочный приоритет должен отдаваться использованию стентов малого диаметра (4.8 Fr вместо 6 Fr) и математическому расчету длины стента на основе роста пациента (формула Wieder), а не обманчивому прямому интраоперационному измерению длины извитого мочеточника.
В условиях злокачественной обструкции (MUO) стандартом должна стать клиническая оценка радиальной компрессионной жесткости. При исчерпании возможностей усиленных полимерных стентов (таких как Superglide) необходимо осуществлять своевременный переход к методике тандемного стентирования или установке металлических саморасширяющихся стентов (Allium, Resonance), обладающих не только непревзойденной способностью удерживать просвет до 12 месяцев, но и доказанной высочайшей фармакоэкономической эффективностью (QALY) для паллиативных онкологических пациентов.
Особого внимания требуют беременные пациентки, для которых сроки замены стента (строго каждые 4–6 недель) диктуются экстремальными пролитогенными сдвигами гестационного метаболизма. Любая оперативная тактика при инкрустации в этой группе должна исключать экстракорпоральное воздействие (ESWL) и опираться исключительно на деликатную гольмиевую лазерную литотрипсию (Ho:YAG) под строгим ультразвуковым контролем.
Наконец, медикаментозное сопровождение стентированного пациента более не может ограничиваться одним препаратом. Фармакотерапия должна быть мультимодальной, с интеграцией бета-3 агонистов, антимускариновых препаратов и альфа-блокаторов, синергетически воздействующих на все звенья нейромышечного патофизиологического каскада спазма и боли. Глубокая интеграция этих доказательных научно-обоснованных подходов позволяет трансформировать стентирование из процедуры, исторически сопряженной с высочайшей морбидностью, в высокоточный, прогнозируемый и безопасный инструмент современной реконструктивной урологии.
10. Литература
- Zimskind PD, Fetter TR, Wilkerson JL. Clinical use of long-term indwelling silicone rubber ureteral splints inserted cystoscopically. J Urol. 1967 May;97(5):840-4. doi: 10.1016/S0022-5347(17)63130-6. PMID: 6025928.
- Bernasconi V, Tozzi M, Pietropaolo A, De Coninck V, Somani BK, Tailly T, Bres-Niewada E, Mykoniatis I, Gregori A, Talso M. Comprehensive overview of ureteral stents based on clinical aspects, material and design. Cent European J Urol. 2023;76(1):49-56. doi: 10.5173/ceju.2023.218. Epub 2023 Jan 12. PMID: 37064263; PMCID: PMC10091895.
- Tomer N, Garden E, Small A, Palese M. Ureteral Stent Encrustation: Epidemiology, Pathophysiology, Management and Current Technology. Journal of Urology [Internet]. 2021 Jan 1 [cited 2026 Feb 20];205(1):68–77. Available from: https://doi.org/10.1097/JU.0000000000001343
- Di Bello F, Califano G, Morra S, Ruvolo CC, Fraia A, Pezone G, Di Mauro E, Aprea S, Napolitano L, Saccone G, Creta M, Longo N. Urological Challenges during Pregnancy: Current Status and Future Perspective on Ureteric Stent Encrustation. J Clin Med. 2024 Jul 3;13(13):3905. doi: 10.3390/jcm13133905. PMID: 38999471; PMCID: PMC11242795.
- EAU Guidelines on Urological Trauma https://uroweb.org/guidelines/urological-trauma/chapter/urogenital-trauma-guidelines
- EAU Guidelines on Urolithiasis https://uroweb.org/guidelines/urolithiasis
- RS, Kim SK, et al. Surgical Management of Kidney and Ureteral Stones: AUA Guideline (2026). Part III: Treatment of Patients With Kidney and/or Ureteral Stones and Future Directions. Journal of Urology [Internet]. 2026 Feb 1 [cited 2026 Feb 20];215(2):132–41. Available from: https://doi.org/10.1097/JU.0000000000004844
- Putrantyo II, Warli SM, Siregar GP, Prapiska FF, Kadar DD, Sihombing B. Role of ureteral stent material and coating to prevent ureteral stent related issue: A systematic review and meta analysis. Arch Ital Urol Androl. 2024 Mar 4;96(1):12067. doi: 10.4081/aiua.2024.12067. PMID: 38441193.
- Vogt B, Blanchet LH. Analysis of Ureteral Tumour Stents for Malignant Ureteral Obstruction: Towards Reshaping an Optimal Stent. Res Rep Urol. 2021 Oct 27;13:773-782. doi: 10.2147/RRU.S334277. PMID: 34737982; PMCID: PMC8558035.
- Cubuk A, Yanaral F, Ozgor F, Savun M, Ozdemir H, Erbin A, Yuksel B, Sarilar O. Comparison of 4.8 Fr and 6 Fr ureteral stents on stent related symptoms following ureterorenoscopy: A prospective randomized controlled trial. Kaohsiung J Med Sci. 2018 Dec;34(12):695-699. doi: 10.1016/j.kjms.2018.07.001. Epub 2018 Jul 21. PMID: 30527204; PMCID: PMC11915623.
- AUA 2025: https://www.urotoday.com/conference-highlights/aua-2025/aua-2025-endourology-and-stone-disease/160051-aua-2025-p2s-paradigm-shifting-practice-changing-clinical-trials-in-urology-randomized-multicenter-trial-of-ureteral-stent-placement-versus-stent-omission-after-ureteroscopy-for-renal-stones.html
- Pearle MS, Matlaga BR, Antonelli JA, et al. Surgical Management of Kidney and Ureteral Stones: AUA Guideline (2026) Part I: Evaluation and Treatment of Patients with Kidney and/or Ureteral Stones. J Urol. 0(0). doi:10.1097/JU.0000000000004842. Https://www.auajournals.org/doi/10.1097/JU.0000000000004842
- Pearle MS, Matlaga BR, Antonelli JA, et al. Surgical Management of Kidney and Ureteral Stones: AUA Guideline (2026) Part II: Evaluation and Treatment of Patients with Kidney and/or Ureteral Stones. J Urol. 0(0). doi:10.1097/JU.0000000000004843. Https://www.auajournals.org/doi/10.1097/JU.0000000000004843
- Pearle MS, Matlaga BR, Antonelli JA, et al. Surgical Management of Kidney and Ureteral Stones: AUA Guideline (2026) Part III: Evaluation and Treatment of Patients with Kidney and/or Ureteral Stones. J Urol. 0(0). doi:10.1097/JU.0000000000004844. Https://www.auajournals.org/doi/10.1097/JU.0000000000004844
- Urotrauma Guideline (2020) https://www.auanet.org/guidelines-and-quality/guidelines/urotrauma-guideline
- https://cr.minzdrav.gov.ru/view-cr/374_3#doc_a1
- Wongtreeratanachai R, Phengsalae Y, Arpornsujaritkun N, Kantachuvesiri S, Kijvikai K, Sirisopana K, Kongchareonsombat W, Sangkum P, Ketsuwan C. Impact of ureteric stent diameter on stent-related symptoms and early outcomes after kidney transplantation: A randomised controlled trial. BJUI Compass. 2026 Jan 25;7(1):e70166. doi: 10.1002/bco2.70166. PMID: 41589193; PMCID: PMC12832192.
- Considerations in ureteral stent selection in order to minimize symptoms - The Canadian Journal of Urology, дата последнего обращения: февраля 20, 2026, https://www.canjurol.com/html/subscriber/Spdf/V29I04/Cdn_JU29-I4_04_10_DrRamkumar.pdf
- Comparison of ureteral stent diameters on ureteral stent-related symptoms: A systematic review and meta-analysis, дата последнего обращения: февраля 20, 2026, https://urologyresearchandpractice.org/index.php/pub/article/view/3465/3461
- Comparison of 4.8 Fr and 6 Fr ureteral stents on stent related symptoms following ureterorenoscopy: A prospective randomized controlled trial - PMC, дата последнего обращения: февраля 20, 2026, https://pmc.ncbi.nlm.nih.gov/articles/PMC11915623/
- Kwong J, Honey RJD, Lee JY, Ordon M. Determination of optimal stent length: a survey of urologic surgeons. Cent European J Urol. 2023;76(1):57-63. doi: 10.5173/ceju.2023.83. Epub 2023 Jan 16. PMID: 37064265; PMCID: PMC10091891.
- Pilcher JM, Patel U. Choosing the correct length of ureteric stent: a formula based on the patient's height compared with direct ureteric measurement. Clin Radiol. 2002 Jan;57(1):59-62. doi: 10.1053/crad.2001.0737. PMID: 11798204.
- Ho CH, Huang KH, Chen SC, Pu YS, Liu SP, Yu HJ. Choosing the ideal length of a double-pigtail ureteral stent according to body height: study based on a Chinese population. Urol Int. 2009;83(1):70-4. doi: 10.1159/000224872. Epub 2009 Jul 27. PMID: 19641363.
- NCT00919386 | Ureteral Stent Size Measurement Study - ClinicalTrials.gov, https://clinicaltrials.gov/study/NCT00919386
- Guo H, Yuan JB. New insights into the prevention of ureteral stents encrustation. Open Med (Wars). 2023 Dec 6;18(1):20230854. doi: 10.1515/med-2023-0854. PMID: 38075034; PMCID: PMC10710215.
- AUA 2022: Comparison of Ureteral Stent BioMaterial Encrustation Profile in Lithogenic Artificial Urine Models https://www.urotoday.com/conference-highlights/2022-annual-meeting/aua-2022-stone-disease/137081-aua-2022-comparison-of-ureteral-stent-biomaterial-encrustation-profile-in-lithogenic-artificial-urine-models.html
- Maxim LS, Rotaru RM, Scarneciu CC, Moga MA, Gherasim RD, Badea MA, Ghicavîi A, Multescu RD, Feciche BO, Scarneciu I. The Impact of Ureteral Stent Indwelling Duration on Encrustation Degree and Extraction Difficulty: A Retrospective Study. J Clin Med. 2025 Jun 18;14(12):4334. doi: 10.3390/jcm14124334. PMID: 40566079; PMCID: PMC12194611.
- EAU Guidelines on Urological Infections https://uroweb.org/guidelines/urological-infections/chapter/the-guideline
- Sharma G, Kumar N, Bai D, Patel S, Mishra DK, Yadav A, Agrawal MS. A randomized controlled trial comparing hydrophilic coated to uncoated polyurethane double J stents: Does it impact stent-related symptoms? Indian J Urol. 2025 Jul-Sep;41(3):190-194. doi: 10.4103/iju.iju_487_24. Epub 2025 Jul 1. PMID: 40756226; PMCID: PMC12312835.
- Soria F, de La Cruz JE, Fernandez T, Budia A, Serrano Á, Sanchez-Margallo FM. Heparin coating in biodegradable ureteral stents does not decrease bacterial colonization-assessment in ureteral stricture endourological treatment in animal model. Transl Androl Urol. 2021 Apr;10(4):1700-1710. doi: 10.21037/tau-21-19. PMID: 33968658; PMCID: PMC8100852.
- Hu K, Hou Z, Huang Y, Li X, Li X and Yang L (2024) Recent development and future application of biodegradable ureteral stents. Front. Bioeng. Biotechnol. 12:1373130. doi: 10.3389/fbioe.2024.1373130
- Update on the Management of Malignant Ureteral Obstruction. Derek J. Lomas, MD, Mayo Clinic, Rochester, Minnesota; Matthew J. Ziegelmann, MD, Mayo Clinic, Rochester, Minnesota, Posted on: 04 May 2023, American Urological Association https://auanews.net/issues/articles/2023/may-2023/update-on-the-management-of-malignant-ureteral-obstruction
- Nonoyama S, Furumido J, Kato R, Ozaki N, Matsugase Y. Safety and Efficacy of Double-J Metallic Mesh Ureteral Stents in Malignant Ureteral Obstruction. Cureus. 2025 May 14;17(5):e84072. doi: 10.7759/cureus.84072. PMID: 40519441; PMCID: PMC12163359.
- Pavlovic K, Lange D, Chew BH. Stents for malignant ureteral obstruction. Asian J Urol. 2016 Jul;3(3):142-149. doi: 10.1016/j.ajur.2016.04.002. Epub 2016 May 13. PMID: 29264182; PMCID: PMC5730830.
- Effectiveness of Double-J Metallic Mesh Ureteral Stents for Malignant Ureteral Obstruction: A Retrospective Study Tomohiro Hori, Tomoyuki Makino, Tetsuya Kawahara, Satoko Urata, Tohru Miyagi, In Vivo Mar 2023, 37 (2) 806-810; DOI: 10.21873/invivo.13145
- Kallidonis P, Kotsiris D, Sanguedolce F, Ntasiotis P, Liatsikos E, Papatsoris A; Young Academic Urologists of the European Association of Urology – Endourology, Urolithiasis Working Party. The effectiveness of ureteric metal stents in malignant ureteric obstructions: A systematic review. Arab J Urol. 2017 Oct 16;15(4):280-288. doi: 10.1016/j.aju.2017.08.004. PMID: 29234529; PMCID: PMC5717459.
- Chow PM, Hsu JS, Wang SM, Yu HJ, Pu YS, Liu KL. Metallic ureteral stents in malignant ureteral obstruction: short-term results and radiological features predicting stent failure in patients with non-urological malignancies. World J Urol. 2014 Jun;32(3):729-36. doi: 10.1007/s00345-013-1143-y. Epub 2013 Aug 10. PMID: 23933664.
- Chow P-M, Chiang I-N, Chen C-Y, Huang K-H, Hsu J-S, Wang S-M, et al. (2015) Malignant Ureteral Obstruction: Functional Duration of Metallic versus Polymeric Ureteral Stents. PLoS ONE 10(8): e0135566. https://doi.org/10.1371/journal.pone.0135566
- Taylor ER, Benson AD, Schwartz BF. Cost analysis of metallic ureteral stents with 12 months of follow-up. J Endourol. 2012 Jul;26(7):917-21. doi: 10.1089/end.2011.0481. Epub 2012 Apr 17. PMID: 22360415.
- Metallic stents efficacious for malignant ureteral obstruction - Urology Times, https://www.urologytimes.com/view/metallic-stents-efficacious-malignant-ureteral-obstruction
- Cooper DM, Lines R, Shergill I. Cost-effectiveness of Resonance® metallic ureteral stent compared with standard polyurethane ureteral stents in malignant ureteric obstruction: A cost-utility analysis. BJUI Compass. 2024 Mar 20;5(5):465-475. doi: 10.1002/bco2.332. Erratum in: BJUI Compass. 2024 Dec 30;5(12):1324-1329. doi: 10.1002/bco2.482. PMID: 38751954; PMCID: PMC11090770.
- Gao X, Di X, Chen G, Wang W, Peng L, Chen J, Wei X. Metal ureteral stents for ureteral stricture: 2 years of experience with 246 cases. Int J Surg. 2024 Jan 1;110(1):66-71. doi: 10.1097/JS9.0000000000000841. PMID: 37812177; PMCID: PMC10793778.
- Salciccia S, De Marco F, Sciarra A, Moriconi M, Alfarone A, Polese M, Maggi M, Del Giudice F, Gentilucci A, De Berardinis E and Ricciuti GP (2022) Allium stent as a curative treatment for benign ureteral strictures: Preliminary experience, surgical technique, and functional results. Front. Urol. 2:984719. doi: 10.3389/fruro.2022.984719
- Su, B., Hu, W., Xiao, B. et al. Long-term outcomes of Allium ureteral stent as a treatment for ureteral obstruction. Sci Rep 14, 21958 (2024). https://doi.org/10.1038/s41598-024-73125-0
- Moon YJ, Chung DY, Kim DK, Jung HD, Jeon SH, Kang SH, Paick S, Lee JY, on behalf of the Korean Society of Endourology and Robotics (KSER) Research Committee. The Beneficial Effects of Alpha-Blockers, Antimuscarinics, Beta 3-Agonist, and PDE5-Inhibitors for Ureteral Stent-Related Discomfort: A Systematic Review and Meta-Analysis from KSER Update Series. Medicina. 2025; 61(2):232. https://doi.org/10.3390/medicina61020232
- Hinojosa-Gonzalez DE, Segall MR, Eisner BH. Pharmacological Management of Ureteral Stent–related Symptoms: A Systematic Review, Bayesian Network Meta-analysis, and Meta-regression. Journal of Urology [Internet]. 2023 Nov 1 [cited 2026 Feb 21];210(5):739–49. Available from: https://doi.org/10.1097/JU.0000000000003616
- Lu Y, Li Q, Zou Q and Cui Y (2023) Mirabegron and antimuscarinics for treating ureteral stent-related symptoms: a systematic review and meta-analysis of RCTs. Front. Pharmacol. 14:1266636. doi: 10.3389/fphar.2023.1266636
- Hu H, Yan M, Liu Z, Qiu J, Dai Y and Tang Y (2024) A method for detecting ureteral stent encrustations in medical CT images based on Mask-RCNN and 3D morphological analysis. Front. Physiol. 15:1432121. doi: 10.3389/fphys.2024.1432121







 Скачать
Скачать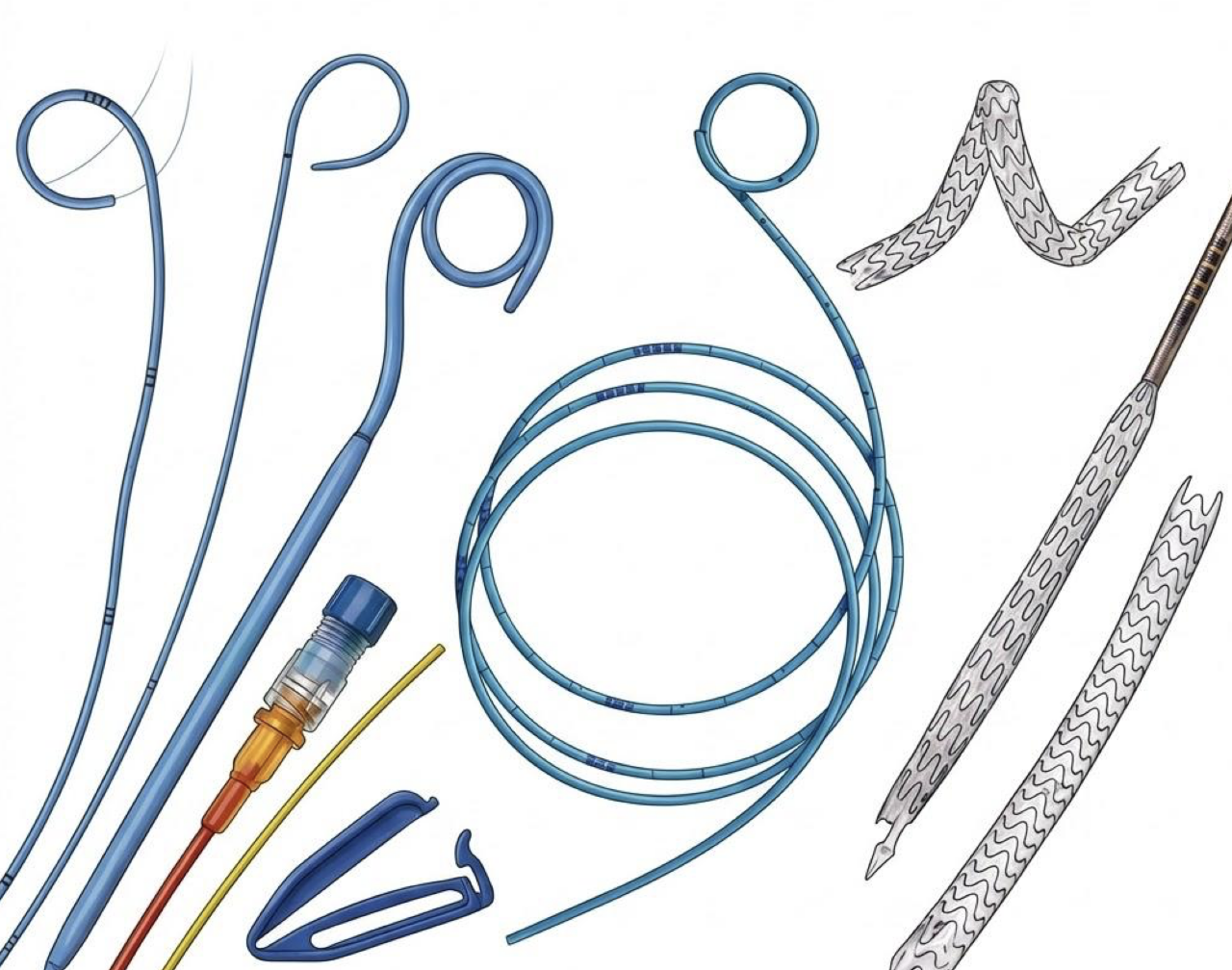











Комментарии