Остроконечные кондиломы: фундаментальное исследование этиологии, патогенеза, диагностики и терапевтических стратегий в практике врача-уролога
Шадеркина Виктория Анатольевна, CEO Uroweb.ru
План обзора:
- 1. Введение. Медико-социальная значимость и эпидемиология
- 2. Этиология и патогенез
- 3. Клиническая картина и диагностика
- 4. Фармакотерапия: доказательная база и механизмы действия
- 5. Хирургическое и инструментальное лечение: сравнительная характеристика технологий
- 6. Лечение интрауретральных кондилом: специфика урологического подхода
- 7. Иммуномодулирующая терапия: конфликт подходов
- 8. Вакцинация: профилактика и терапевтические перспективы
- 9. Прогноз, рецидивы и диспансеризация
- 10. Выводы
1. Введение. Медико-социальная значимость и эпидемиология
Остроконечные кондиломы (condylomata acuminata), также именуемые аногенитальными бородавками, представляют собой одно из наиболее распространенных клинических проявлений папилломавирусной инфекции (ПВИ) человека и занимают лидирующие позиции в структуре инфекций, передаваемых половым путем (ИППП). Для практикующего врача-уролога данная нозология является не только рутинной клинической задачей, но и сложным вызовом, требующим мультидисциплинарного понимания вирусологии, иммунологии, онкологии и дерматовенерологии. Несмотря на доброкачественный характер течения в большинстве случаев, заболевание ассоциировано с существенным снижением качества жизни, психосексуальной дисфункцией, значительными экономическими затратами на лечение и высоким риском рецидивирования, который, по различным данным, достигает 30–50% в течение первых месяцев после деструкции очагов [1, 2].
Глобальное бремя заболевания остроконечными кондиломами остается высоким, несмотря на внедрение программ вакцинации [2-5]. Согласно данным Европейской ассоциации урологов (EAU) и Центров по контролю и профилактике заболеваний США (CDC), ежегодная заболеваемость аногенитальными бородавками варьирует в широких пределах — от 160 до 289 случаев на 100 000 населения [2, 3]. Пик заболеваемости предсказуемо коррелирует с пиком сексуальной активности и приходится на возрастную когорту 20–24 года у женщин и 25–29 лет у мужчин.
В Российской Федерации эпидемиологическая ситуация зеркально отражает мировые тренды: наблюдается стабильный рост выявляемости данной патологии, что отчасти связано как с истинным увеличением инфицированности, так и с улучшением качества диагностики [5]. Важно отметить, что официальная статистика зачастую демонстрирует лишь «вершину айсберга», так как значительная часть пациентов либо не обращается за медицинской помощью, прибегая к самолечению, либо имеет субклинические формы инфекции, которые остаются недиагностированными при рутинном осмотре.
Актуальность проблемы для урологического сообщества обусловлена также спецификой локализации процесса у мужчин. Поражение уретры, особенно ее дистального отдела и ладьевидной ямки, требует от врача владения эндоскопическими навыками и специализированным оборудованием (лазерные установки, эндоскопы). Неадекватное лечение интрауретральных кондилом чревато развитием стриктур уретры — грозного осложнения, приводящего к инвалидизации пациентов молодого трудоспособного возраста. Кроме того, сохраняется онкологическая настороженность: хотя классические остроконечные кондиломы вызываются типами ВПЧ низкого онкогенного риска (преимущественно 6 и 11), феномен коинфекции с высокоонкогенными типами (16, 18 и др.) наблюдается у значительной части пациентов, что требует тщательного дифференциально-диагностического поиска и гистологической верификации в сомнительных случаях [6].
В настоящем отчете представлен исчерпывающий анализ современного состояния проблемы аногенитальных бородавок с акцентом на урологические аспекты. Работа базируется на критическом синтезе международных клинических рекомендаций (EAU 2024, CDC 2021, IUSTI 2020) и действующих нормативных актов Министерства здравоохранения Российской Федерации [1]. Особое внимание уделено сравнительному анализу терапевтических подходов, роли иммуномодулирующей терапии в различных национальных школах, нюансам применения лазерных энергий (Ho:YAG vs Tm:YAG) и дискуссионным вопросам адъювантной вакцинации.
2. Этиология и патогенез
2.1. Вирусологическая характеристика возбудителя
Этиологическим агентом заболевания выступает вирус папилломы человека (ВПЧ) — мелкий безоболочечный ДНК-содержащий вирус семейства Papillomaviridae. Геном вируса представлен двухцепочечной циркулярной ДНК, кодирующей ранние (E — early) и поздние (L — late) белки. Ранние белки (E1, E2, E4, E5, E6, E7) отвечают за репликацию вирусной ДНК, регуляцию транскрипции и трансформацию клетки-хозяина, в то время как поздние белки (L1, L2) формируют капсид вириона. Именно белок L1 обладает высокой иммуногенностью и является основой для создания современных профилактических вакцин [7, 8].
На сегодняшний день идентифицировано и секвенировано более 200 типов ВПЧ. Из них около 40 типов обладают тропностью к многослойному плоскому эпителию аногенитального тракта.
В клинической практике принято разделение генотипов ВПЧ на группы риска в зависимости от их онкогенного потенциала:
- Типы низкого онкогенного риска (Low-risk HPV): ВПЧ 6 и 11 типов являются причиной более 90% всех случаев экзофитных остроконечных кондилом [3]. Эти типы вирусов, как правило, находятся в клетке в эписомальной форме (вне хромосомы хозяина) и редко приводят к злокачественной трансформации, однако способны вызывать массивные, обезображивающие разрастания (гигантская кондилома Бушке-Левенштейна).
- Типы высокого онкогенного риска (High-risk HPV): К ним относятся типы 16, 18, 31, 33, 45, 52, 58 и ряд других. ДНК этих вирусов способна интегрироваться в геном клетки-хозяина, что приводит к нарушению клеточного цикла, ингибированию белков-супрессоров опухолевого роста (p53 и Rb) вирусными онкопротеинами E6 и E7 и развитию дисплазии (интраэпителиальной неоплазии) и карциномы [3].
Для уролога критически важным является понимание того факта, что наличие видимых кондилом, вызванных ВПЧ 6/11, не исключает присутствия высокоонкогенных типов вируса в той же анатомической зоне или на соседних участках. Коинфекция несколькими типами ВПЧ является распространенным явлением, особенно в группах риска (МСМ, пациенты с ВИЧ). Исследования показывают, что в ткани типичной остроконечной кондиломы могут одновременно детектироваться ДНК ВПЧ высокого риска, что диктует необходимость онкологической настороженности даже при доброкачественном внешнем виде образований [6].
2.2. Механизмы передачи и инфицирования
Вирус папилломы человека обладает строгой эпителиотропностью. Инфицирование происходит при прямом контакте поврежденного эпителия с инфицированной тканью (кожа-к-коже или слизистая-к-слизистой). «Входными воротами» для вируса служат микротравмы и мацерации, обнажающие базальный слой эпителия. Вирус связывается с гепаран-сульфатными рецепторами на базальной мембране и проникает в базальные кератиноциты — единственные делящиеся клетки эпидермиса, которые служат резервуаром для вируса.
Половой путь передачи является доминирующим. Риск передачи ВПЧ при однократном незащищенном половом контакте с инфицированным партнером оценивается в 60–75%, что делает ВПЧ одной из самых контагиозных инфекций. Презервативы снижают риск передачи, но не обеспечивают 100% защиты, так как вирус может находиться на участках кожи, не покрытых латексом (мошонка, лобок, перианальная область) [6].
Помимо полового пути, возможна вертикальная передача от матери к плоду (риск развития респираторного папилломатоза гортани у новорожденного) и, теоретически, контактно-бытовой путь. Обнаружение ДНК ВПЧ на поверхностях в медицинских учреждениях, общественных туалетах и на медицинском инструментарии поднимает вопрос о возможности непрямой трансмиссии, однако клиническая значимость этого пути остается предметом дискуссий. Для реализации инфекции необходима достаточная вирусная нагрузка и наличие входных ворот, что делает бытовое заражение менее вероятным, но не невозможным событием [6].
2.3. Жизненный цикл вируса и иммунный ответ
После инфицирования базальных клеток вирус может длительное время находиться в латентном состоянии. Репликация вируса жестко синхронизирована с дифференцировкой кератиноцитов. По мере продвижения инфицированной клетки из базального слоя к поверхности эпителия происходит экспрессия вирусных генов, сборка вирусных частиц и их выход при слущивании роговых чешуек (рис. 1).
Ключевой особенностью ВПЧ является его способность «ускользать» от иммунного надзора. Вирус не вызывает лизиса клеток (нет воспаления), не попадает в кровоток (нет системного иммунного ответа) и подавляет выработку интерферонов первого типа в зараженных клетках. Это объясняет, почему инфекция может персистировать месяцами и годами без клинических проявлений.
Клиническая манифестация в виде бородавок происходит при нарушении баланса между репликацией вируса и иммунным контролем. Иммуносупрессия любого генеза (ВИЧ-инфекция, прием иммуносупрессантов, беременность, стресс) является мощным триггером для активации латентной инфекции и бурного роста кондилом.
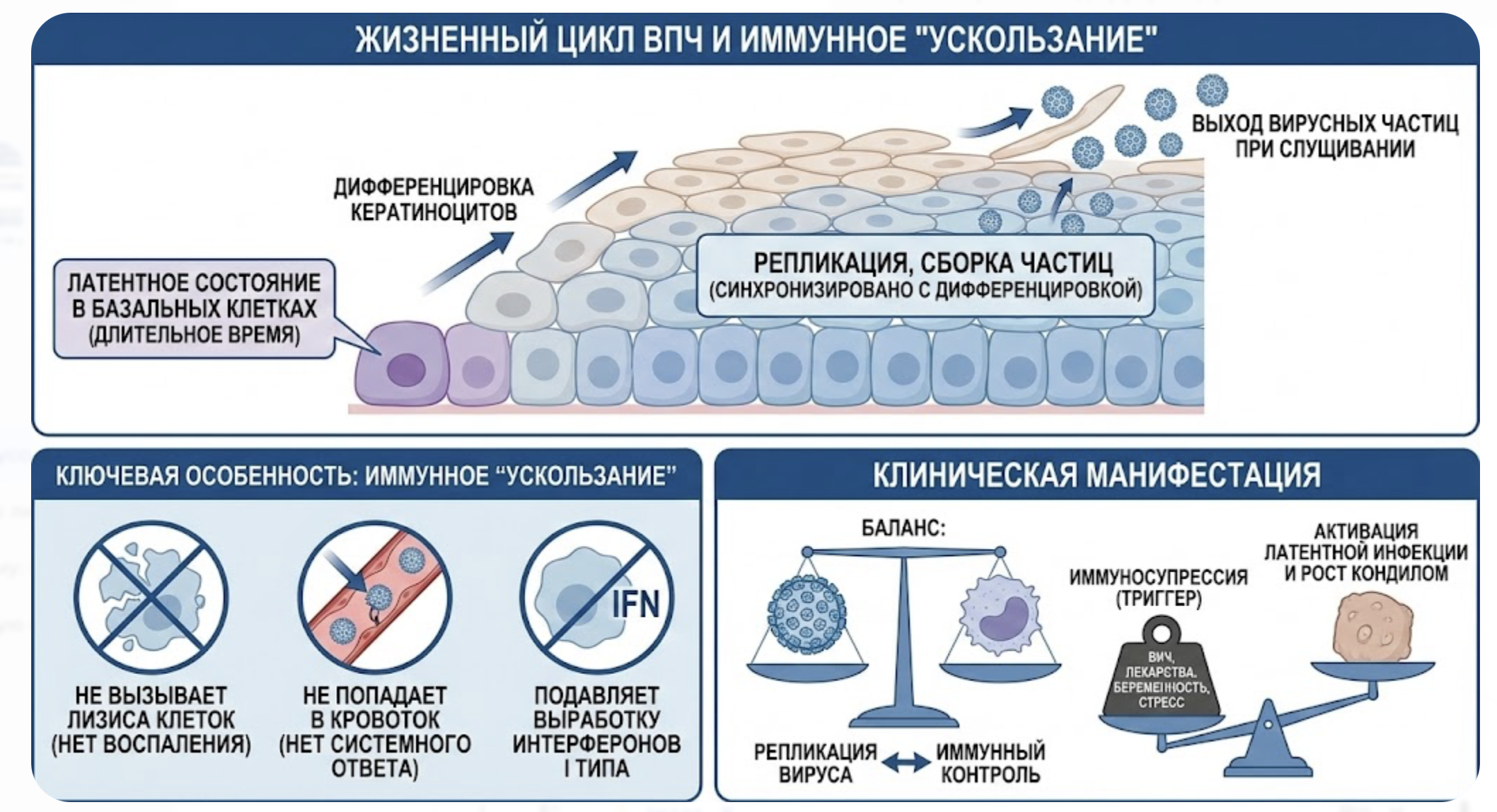
Рис. 1. Жизненный цикл ВПЧ
В естественном течении заболевания выделяют три возможных сценария:
- Спонтанный регресс. Около 30% бородавок могут регрессировать самостоятельно в течение первых 3 месяцев благодаря активации клеточного иммунитета.
- Стабилизация. Элементы сохраняются без существенного роста.
- Прогрессирование. Увеличение количества и размеров элементов, слияние их в конгломераты.
Важно подчеркнуть, что элиминация видимых проявлений не равнозначна эрадикации вируса. ДНК ВПЧ может сохраняться в визуально здоровой коже на расстоянии до 1-2 см от очага поражения, что создает субстрат для рецидивов [2].
3. Клиническая картина и диагностика
3.1. Визуальная семиотика
Диагноз аногенитальных бородавок в подавляющем большинстве случаев устанавливается клинически, на основании физикального осмотра. Классическая картина представлена экзофитными разрастаниями телесного, розового или сероватого цвета. Поверхность образований может быть гладкой (папулезные бородавки), но чаще имеет вид «цветной капусты» или «петушиного гребня» (остроконечные кондиломы). Образования могут быть единичными или множественными, иногда сливаясь в гигантские бляшки (рис. 2).
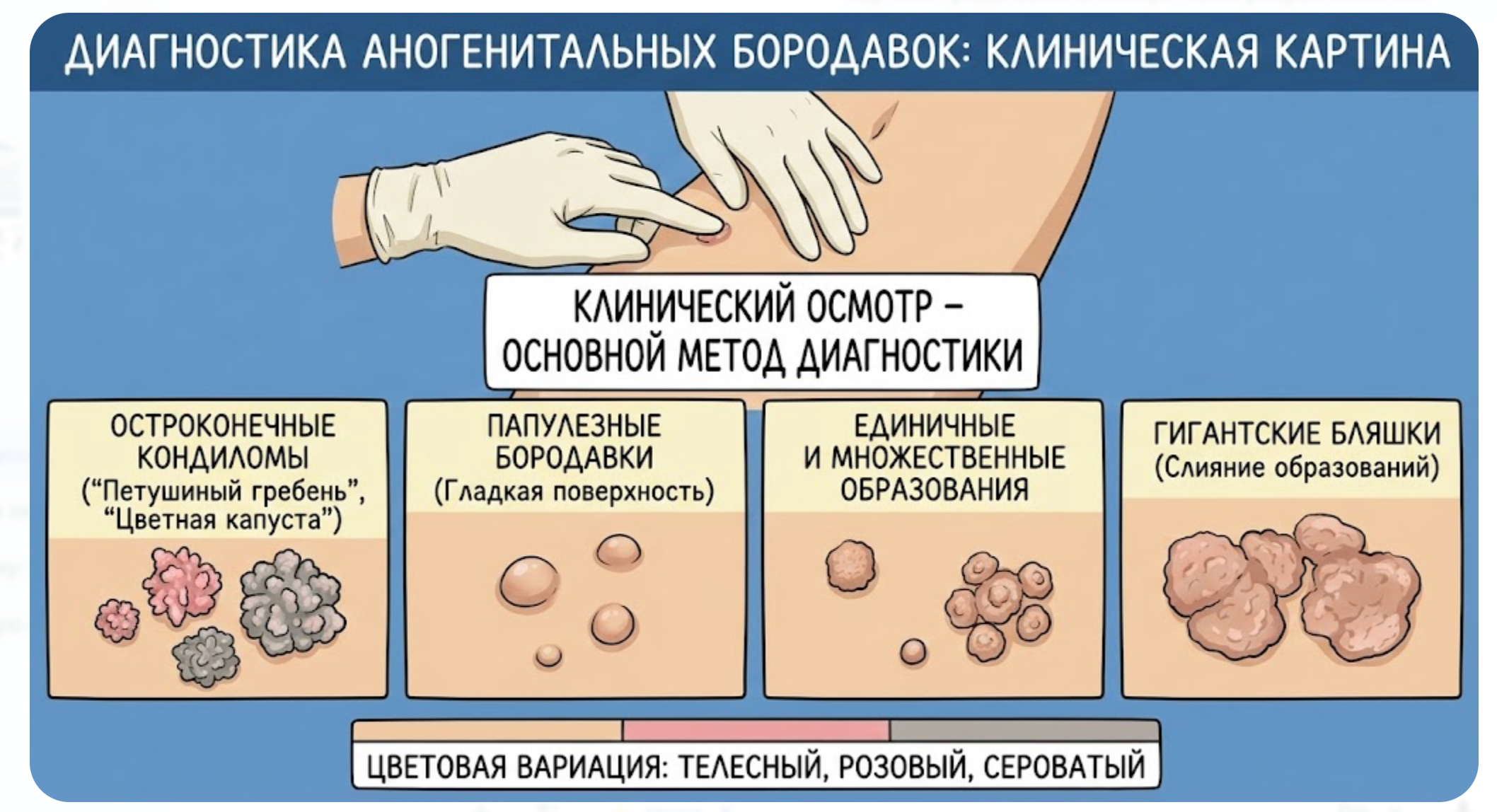
Рис. 2. Диагностика и внешний вид аногенитальных бородавок
У мужчин наиболее частыми локализациями являются:
- Внутренний листок крайней плоти (препуциальный мешок) — влажная среда способствует мацерации и росту вирусов.
- Венечная борозда головки полового члена.
- Уздечка полового члена (френулум).
- Ствол полового члена.
- Наружное отверстие уретры (меатус).
- Мошонка.
- Перианальная область и анальный канал.
Особую настороженность должны вызывать пигментированные, уплотненные, изъязвленные образования, а также элементы, спаянные с подлежащими тканями. Такие признаки могут указывать на бовеноидный папулез (предраковое состояние, ассоциированное с ВПЧ 16) или плоскоклеточный рак, что требует немедленной биопсии [6-9].
3.2. Дерматоскопия: современный стандарт неинвазивной диагностики
В последние годы дерматоскопия прочно вошла в арсенал не только дерматологов, но и урологов, занимающихся патологией наружных половых органов. Этот метод позволяет визуализировать структуры эпидермиса и дермы, невидимые невооруженным глазом, и значительно повышает точность дифференциальной диагностики.
Исследования показывают высокую корреляцию между дерматоскопическими паттернами и гистологическим строением кондилом.
Характерными признаками остроконечных кондилом при дерматоскопии являются:
- Сосудистые паттерны:
- Гломерулярные (клубочковые) сосуды – визуализируются как красные точки или свернутые клубочки внутри сосочков. Это наиболее специфичный признак.
- Шпилькообразные сосуды – петли капилляров в виде шпилек, часто окруженные белесоватым ореолом (кератином).
- Точечные сосуды – мелкие точки на вершинах папул.
- Структурные паттерны:
- Мозаичный паттерн – характерен для плоских элементов.
- Пальцевидный паттерн – множественные пальцеобразные выросты с сосудом в центре, типично для экзофитных форм.
- Бугристый паттерн – округлые выбухания без выраженной пальцевидной структуры.
Дерматоскопия позволяет надежно дифференцировать кондиломы от таких состояний, как:
- Жемчужные папулы полового члена – выглядят как ряды одинаковых белых или розоватых папул на венечной борозде, имеют характерные сосуды в виде «запятой», но не гломерулярные.
- Сальные железы (гранулы Фордайса) – желтоватые дольчатые структуры без сосудистого рисунка.
- Контагиозный моллюск – наличие центрального пупковидного вдавления и аморфной бело-желтой структуры в центре, окруженной венцом сосудов.
- Лихен – сетка Викхема (белые полосы) при дерматоскопии.
При поражении меатуса дерматоскопия помогает определить точные границы распространения процесса на слизистую уретры, что критично для планирования объема лазерной аблации [10].
3.3. Уретроскопия и диагностика интрауретральных поражений
Поражение уретры встречается у 20–25% мужчин с аногенитальными бородавками, причем в большинстве случаев процесс ограничивается дистальным отделом. Проксимальное распространение и поражение мочевого пузыря встречаются крайне редко [6].
Согласно рекомендациям EAU 2024, рутинная тотальная уретроцистоскопия всем пациентам с наружными кондиломами не показана, так как это инвазивная и дорогостоящая процедура с низким выходом находок. Однако, уретроскопия строго показана в следующих ситуациях:
- Наличие видимых кондилом в области наружного отверстия уретры (меатуса).
- Симптомы нарушения мочеиспускания (дизурия, странгурия, раздвоение или разбрызгивание струи мочи).
- Гематурия (микро- или макро-).
- Рецидивирующие кондиломы меатуса после лечения.
Для осмотра дистального отдела уретры (до 2-3 см) можно использовать разведение губок уретры или уретроскоп. Для осмотра всей уретры предпочтительно использование гибкого цистоскопа, который доставляет меньше дискомфорта пациенту.
3.4. Проба с уксусной кислотой
Тест с 3–5% раствором уксусной кислоты традиционно использовался для выявления субклинических поражений. При аппликации кислоты на 5–10 минут пораженные участки белеют.
Однако в настоящее время экспертные сообщества (CDC, EAU, IUSTI) не рекомендуют рутинное использование этого теста для скрининга из-за крайне низкой специфичности. Ложноположительные результаты часто возникают при воспалении, микротравмах, псориазе, лихене и просто на здоровой коже, что приводит к гипердиагностике и необоснованному лечению, вызывая у пациента ятрогенную тревогу [6].Тест может быть полезен только опытному врачу для уточнения границ поражения непосредственно перед деструкцией.
3.5. Биопсия
Гистологическое исследование не является обязательным для всех случаев, так как клиническая картина обычно типична. Однако биопсия становится императивом в следующих клинических сценариях:
- Диагностическая неопределенность (атипичный вид, пигментация).
- Отсутствие эффекта от стандартной терапии (резистентность).
- Ухудшение состояния на фоне терапии.
- Иммунокомпрометированные пациенты (ВИЧ-инфекция, трансплантация органов) — высокий риск дисплазии.
- Подозрение на предраковые процессы (бовеноидный папулез) или карциному [5].
3.6. Лабораторная диагностика и ВПЧ-тестирование
Критически важный аспект, часто вызывающий недопонимание у пациентов и врачей: тестирование мужчин на ВПЧ не имеет доказанной клинической ценности и не рекомендуется международными протоколами [6].
Причины отсутствия рекомендаций:
- Высокая распространенность транзиторного носительства вируса, которое не требует лечения.
- Отсутствие валидированных тест-систем для забора материала с кожи полового члена (в отличие от шейки матки).
- Положительный результат теста не меняет тактику лечения видимых кондилом.
- Отрицательный результат не исключает наличие вируса.
Российские клинические рекомендации 2024 года также солидарны с международными в вопросе тестирования половых партнеров: тестирование мужчин-партнеров женщин с ВПЧ не рекомендовано [10-16]. Диагноз и показания к лечению базируются исключительно на наличии клинических проявлений.
4. Фармакотерапия: доказательная база и механизмы действия
Лечение аногенитальных бородавок направлено на удаление видимых элементов, уменьшение симптоматики и улучшение качества жизни. Выбор метода зависит от морфологии высыпаний, их локализации, предпочтений пациента и опыта врача. Терапевтические опции принято делить на методы самостоятельного применения пациентом и методы врачебного применения.
4.1. Топическая терапия (пациент-контролируемые методы)
Подофиллотоксин (0,5% раствор или гель, 0,15% крем)
Является очищенным экстрактом растения Podophyllum.
- Антимитотическое действие. Вещество связывается с микротрубочками клеточного веретена деления, блокируя митоз в метафазе, что приводит к некрозу эпидермиса и разрушению бородавки.
- Наносится 2 раза в день (утром и вечером) в течение 3 дней, затем следует перерыв 4 дня. Цикл повторяется до 4 раз.
- Полный клиренс достигается у 45–83% пациентов. Мета-анализы показывают, что раствор эффективнее крема, но крем удобнее для самостоятельного нанесения, особенно в перианальной области [15].
- Токсичен, противопоказан при беременности. Может вызывать местное раздражение, эрозии. Не рекомендуется наносить на большие площади (более 10 см²) во избежание системной абсорбции.
Имиквимод (5% и 3,75% крем)
- Иммуномодулятор местного действия, агонист Toll-подобных рецепторов 7 (TLR7). Индуцирует выработку эндогенного интерферона-альфа, фактора некроза опухоли (TNF-alpha) и интерлейкинов, активируя клеточный иммунный ответ против вируса. В отличие от подофиллотоксина, не обладает прямым цитотоксическим действием.
- 5% крем наносится 3 раза в неделю на ночь (смыть через 6–10 часов) в течение до 16 недель. 3,75% крем наносится ежедневно.
- Клиренс 35–75%. Частота рецидивов ниже, чем при деструктивных методах, благодаря индукции иммунной памяти.
- Действие развивается медленно. Характерно развитие местной воспалительной реакции (эритема, отек), которая коррелирует с эффективностью лечения (признак активации иммунитета). Исследования показали, что имиквимод менее эффективен на ороговевающих сухих участках кожи (ствол пениса) по сравнению с влажными участками (препуций), вероятно, из-за худшего проникновения препарата [17].
Синекатехины (15% мазь)
- Экстракт листьев зеленого чая (Camellia sinensis). Механизм до конца не изучен, предполагается антиоксидантное, антипролиферативное и противовирусное действие.
- Применяется 3 раза в день до 16 недель. Не требует смывания.
- Сопоставима с имиквимодом (47–59%).
4.2. Врачебные методы деструкции
4.2.1. Криотерапия (жидкий азот)
-
Быстрое замораживание внутриклеточной жидкости приводит к разрыву клеточных мембран, тромбозу микроциркуляторного русла и ишемическому некрозу ткани. Кроме того, высвобождение вирусных антигенов при разрушении клеток может стимулировать иммунный ответ.
- Используется спрей или криозонд. Рекомендуется методика «двойного замораживания» для повышения эффективности. Процедуры повторяют каждые 1–2 недели.
- Эффективность составляет 44–87%. Эффективен, дешев, безопасен при беременности [14].
- Болезненность, риск гипопигментации (разрушение меланоцитов), низкая эффективность при гиперкератотических элементах.
4.2.2. Трихлоруксусная кислота (TCA 80–90%)
- Химическая коагуляция белков, вызывающая некроз ткани.
- Наносится врачом точечно на бородавку до появления белого налета («фрост»). Повторяется еженедельно.
- Эффективность 50–81%.
- Раствор обладает низкой вязкостью и может растекаться, повреждая здоровую кожу. Требует аккуратности. При сильном жжении нейтрализуется содой или тальком. Разрешен при беременности.
5. Хирургическое и инструментальное лечение: сравнительная характеристика технологий
Хирургические методы (лазер, электрокоагуляция, иссечение) обеспечивают наиболее быстрый результат и являются предпочтительными при обширных, множественных или резистентных к топической терапии поражениях (табл. 1).
5.1. Лазерная деструкция: физика и клиническое применение
Лазерные технологии занимают центральное место в современной урологии благодаря прецизионности и возможности контроля глубины воздействия.
5.1.1. CO2-лазер (углекислотный)
- Длина волны: 10 600 нм.
- Физика: Энергия поглощается водой (внутриклеточной и внеклеточной). Обеспечивает вапоризацию тканей.
- Преимущества: Высочайшая эффективность (первичный клиренс 90–100%) [18]. «Золотой стандарт» для обширных поражений и лечения беременных. Возможность послойной аблации под визуальным контролем.
- Недостатки: Низкая гемостатическая способность (плохо коагулирует сосуды диаметром > 0,5 мм), риск образования рубцов при глубоком воздействии. Генерирует дым, содержащий вирусную ДНК, что требует использования мощных эвакуаторов дыма и респираторов класса N95/FFP3 для защиты персонала [14].
5.1.2. Nd:YAG лазер (неодимовый)
- Длина волны: 1064 нм.
- Физика: Глубокое проникновение в ткани (до 4-5 мм). Энергия поглощается белками и гемоглобином.
- Применение: Хороший гемостаз, но высокий риск глубокого термического ожога и рубцевания. В настоящее время уступает позиции гольмиевому и тулиевому лазерам.
5.1.3. Holmium:YAG лазер (гольмиевый)
- Длина волны: 2140 нм.
- Физика: Хорошо поглощается водой. Глубина проникновения около 0.4 мм. Работает в импульсном режиме.
- Применение в урологии: Широко доступен (используется для литотрипсии). Обеспечивает эффективную аблацию с умеренной зоной коагуляционного некроза. Безопасен для интрауретрального применения [19].
5.1.4. Thulium:YAG лазер (тулиевый)
- Длина волны: 1940–2013 нм.
- Физика: Пик поглощения водой совпадает с длиной волны тулиевого лазера, что обеспечивает еще меньшую глубину проникновения (0.1–0.2 мм) по сравнению с гольмиевым. Работает в непрерывном режиме (CW), что позволяет делать очень ровные и чистые разрезы («лазерный скальпель»).
- Клинические данные: Исследования показывают, что тулиевый лазер является безопасной и эффективной альтернативой Nd:YAG и Ho:YAG. Благодаря минимальной глубине проникновения риск рубцевания и стриктур уретры при его использовании минимален, что делает его методом выбора для деликатных зон (уретра, головка полового члена) [19].
Табл. 1. Сравнительная эффективность методов лечения [18]
|
Метод лечения |
Первичный клиренс |
Частота рецидивов |
Риск побочных эффектов |
Уровень доказательности |
|
CO2-лазер |
Очень высокий (>90%) |
Средний |
Средний (боль, рубцы) |
High |
|
Хирургическое иссечение |
Очень высокий (100%) |
Низкий |
Высокий (кровотечение, рубцы) |
High |
|
Подофиллотоксин р-р |
Высокий (70-80%) |
Высокий (30-60%) |
Средний (эрозии) |
High |
|
Имиквимод крем |
Средний (50-60%) |
Низкий (<30%) |
Высокий (воспаление) |
High |
|
Криотерапия |
Высокий (60-80%) |
Высокий |
Низкий |
Moderate |
6. Лечение интрауретральных кондилом: специфика урологического подхода
Лечение кондилом наружного отверстия уретры и интрауретральных поражений — зона исключительной ответственности уролога. Основная задача — полное удаление образований при сохранении анатомической целостности уретры и предотвращении развития стриктур.
6.1. Хирургическая тактика
Согласно рекомендациям CDC и EAU, методом выбора для интрауретральных бородавок является эндоскопическая деструкция.
Использование топических средств (имиквимод, подофиллотоксин) внутри уретры не рекомендовано из-за невозможности контролировать зону воздействия, риска химического ожога слизистой и развития стриктур, а также системной абсорбции препаратов [14].
- Меатальные бородавки (видимые снаружи) могут быть удалены с помощью криодеструкции (с осторожностью), CO2-лазера или хирургического иссечения. Важно избегать циркулярного поражения меатуса, чтобы не вызвать стеноз. Рекомендуется оставлять «мостики» здоровой слизистой между зонами аблации.
- Интрауретральные бородавки – удаление проводится под эндоскопическим контролем. Предпочтительно использование лазерной энергии (Holmium или Thulium) через рабочее волокно цистоскопа. Лазерная аблация позволяет прецизионно вапоризировать кондиломы «слой за слоем» до основания, минимизируя термическое повреждение стенки уретры.
- Электрорезекция (ТУР) – при массивных поражениях возможно использование петли резектоскопа или биполярного электрода. Однако этот метод несет более высокий риск рубцевания по сравнению с лазером.
6.2. Адъювантная интрауретральная химиотерапия (5-фторурацил)
В случаях рецидивирующего «коврового» папилломатоза уретры, когда множественные хирургические вмешательства травматичны, возможно применение инстилляций 5-фторурацила (5-FU). Это применение «off-label» (вне инструкции), но оно описано в литературе и применяется в экспертных центрах.
- Протокол. Инстилляция 5% крема или раствора 5-FU в уретру. В одном из исследований использовалась методика: 500 мг 5-FU в 50 мл физраствора или введение крема с экспозицией 20 минут и массажем уретры для распределения препарата. Курс: 1 раз в неделю в течение 5–8 недель [21].
- Осложнения. Высокий риск химического уретрита, дизурии, гематурии, изъязвления мошонки (при вытекании препарата). Требует тщательного мониторинга и защиты кожи наружных половых органов цинковой мазью во время процедуры.
7. Иммуномодулирующая терапия: конфликт подходов
В вопросах применения системной иммунотерапии наблюдается существенное расхождение между западными и российскими клиническими рекомендациями.
7.1. Международная позиция (CDC, EAU, IUSTI)
Западные руководства не рекомендуют системное применение иммуномодуляторов (интерферонов, инозина пранобекса) для лечения остроконечных кондилом [14]. Основанием служит отсутствие убедительных данных крупных РКИ, подтверждающих превосходство системной терапии над локальной деструкцией, а также высокая стоимость и риск системных побочных эффектов (гриппоподобный синдром при введении интерферонов). Внутриочаговое введение интерферона рассматривается лишь как резервный метод для резистентных случаев, но на практике применяется редко.
7.2. Российская клиническая практика и рекомендации
Действующие Клинические рекомендации Минздрава РФ «Аногенитальные (венерические) бородавки» (2024) включают иммуномодуляторы в схемы комбинированной терапии, особенно при рецидивирующем течении процесса [5].
- Инозин пранобекс. Синтетическое производное пурина, обладающее иммуностимулирующей и неспецифической противовирусной активностью. Рекомендованный режим: 1000 мг (2 таблетки) 3 раза в день в течение 14–28 дней. Российские мета-анализы указывают, что комбинация деструкции с инозином пранобексом повышает эффективность лечения до 87–97% и снижает частоту рецидивов по сравнению с монотерапией деструктивными методами [22].
- Интерферон альфа-2b. Рекомендуется в виде ректальных суппозиториев (500 000 – 3 000 000 МЕ) или геля. Механизм действия связан с восполнением дефицита эндогенного интерферона, который подавляется вирусом, и активацией противовирусного иммунитета. Рекомендация имеет уровень убедительности C (достоверность 5) и позиционируется как средство профилактики рецидивов [16].
Практический вывод для врача в РФ: Назначение иммуномодуляторов находится в правовом поле и обосновано национальными стандартами, однако врач должен информировать пациента о различиях в международных подходах.
8. Вакцинация: профилактика и терапевтические перспективы
8.1. Профилактическая вакцинация
Квадривалентная (против типов 6, 11, 16, 18) и девятивалентная (дополнительно типы 31, 33, 45, 52, 58) вакцины продемонстрировали феноменальную эффективность (99–100%) в предотвращении аногенитальных бородавок у лиц, не инфицированных ранее [3]. В странах с масштабными программами вакцинации (Австралия) заболеваемость среди молодежи снизилась практически до нуля. CDC рекомендует вакцинацию всех мужчин до 26 лет (и до 45 лет по индивидуальным показаниям) [14].
8.2. Адъювантная (терапевтическая) вакцинация: спорный вопрос
Наиболее острая дискуссия в современной литературе ведется вокруг вопроса: нужно ли вакцинировать пациента, у которого УЖЕ есть кондиломы, для предотвращения рецидивов после лечения?
Аргументы в пользу вакцинации
- Профилактика аутоинокуляции. После хирургической деструкции вирус может высвобождаться и обсеменять соседние участки (феномен Кебнера). Высокий титр L1-антител, индуцированный вакциной, может нейтрализовать вирус и предотвратить повторную адгезию к базальной мембране заживающей раны [3].
- Защита от других типов. Пациент с кондиломами (ВПЧ 6/11) не защищен от инфицирования типами высокого риска (16, 18), которые также покрываются вакциной.
Данные исследований (2020–2024)
Результаты мета-анализов противоречивы.
- Исследование Petras et al. (2023) и другие работы показали, что адъювантная вакцинация достоверно снижает риск рецидива тяжелых интраэпителиальных неоплазий (CIN2+) после эксцизии [25].
- Однако в отношении именно аногенитальных бородавок данные менее оптимистичны. Мета-анализ Husein-ElAhmed (2020) и обзор Tavassoli (2024) не выявили статистически значимого снижения частоты рецидивов кондилом у вакцинированных пациентов по сравнению с невакцинированными [27].
- Тем не менее, исследование 2024 года показало тренд к снижению рецидивов (11.6% против 21.7%) и достоверное увеличение интервала без болезни у вакцинированных [29].
Вакцинация при наличии кондилом не является официально утвержденным методом лечения («off-label» как терапия), но настоятельно рекомендуется как средство профилактики суперинфекции другими типами и, возможно, как способ снижения риска рецидивов, хотя доказательная база последнего эффекта требует дальнейшего подтверждения.
9. Прогноз, рецидивы и диспансеризация
Аногенитальные бородавки характеризуются высокой частотой рецидивов (до 50%), которые чаще всего возникают в первые 3–6 месяцев после лечения [14].
Факторы риска рецидива
- Иммуносупрессия (ВИЧ, диабет).
- Курение (снижает местный иммунитет эпителия).
- Наличие вируса в краях резекции (при хирургическом лечении).
- Повторное инфицирование от нелеченного партнера ("ping-pong" инфекция).
Тактика при рецидивах
Если монотерапия неэффективна или возникает рецидив, показана смена метода (ротация) или использование комбинированной терапии (например, лазерная деструкция + последующий курс имиквимода или инозина пранобекса). Для интрауретральных рецидивов методом выбора остается повторная лазерная аблация.
Диспансерное наблюдение
Согласно Приказу Минздрава РФ №168н, пациенты подлежат диспансерному наблюдению [30]. Осмотр рекомендуется проводить через 1 месяц после лечения, затем каждые 3 месяца в течение года. При отсутствии рецидивов в течение года пациент может быть снят с учета.
Важной частью наблюдения является консультирование партнера и, при необходимости, его обследование и лечение, хотя жестких требований по «контактному лечению» (как при сифилисе или гонорее) для ВПЧ нет из-за повсеместной распространенности вируса.
10. Выводы
Аногенитальные бородавки в практике уролога — это патология, требующая не просто механического удаления «нароста», а комплексного подхода к пациенту.
Современная стратегия ведения включает:
- Точную диагностику. Использование дерматоскопии для верификации и уретроскопии для исключения интрауретральных поражений.
- Дифференцированный выбор терапии. Топические иммуномодуляторы (имиквимод) предпочтительны для профилактики рецидивов на коже, в то время как лазерная деструкция (особенно тулиевым или гольмиевым лазером) является «золотым стандартом» для уретры и меатуса.
- Рациональную фармакотерапию. В российских реалиях обосновано применение системных иммуномодуляторов в сложных случаях, опираясь на национальные клинические рекомендации.
- Профилактику. Активное продвижение вакцинации среди мужчин, даже имеющих в анамнезе эпизоды ВПЧ-инфекции, для предотвращения коинфекции онкогенными типами вируса.
Понимание биологии ВПЧ, владение современными методами деструкции и умение выстроить доверительный диалог с пациентом (учитывая психосексуальный аспект болезни) являются залогом успешного лечения этой распространенной, но коварной патологии.
Источники
- Nugent D, Apoola A, Coleman H, Gilmour C, Lawton MD, Nori A, D C Ross J, Whitlock G, Yeend-Curd-Trimble H. British association for sexual health and HIV national guideline for the management of anogenital warts in adults (2024). Int J STD AIDS. 2024 Jun;35(7):498-509. doi: 10.1177/09564624241233338. Epub 2024 Mar 8. PMID: 38456387 https://pubmed.ncbi.nlm.nih.gov/38456387/
- EAU Guidelines on Urological Infections, дата последнего обращения: декабря 7, 2025, https://uroweb.org/guidelines/urological-infections/chapter/the-guideline
- Wangu Z, Hsu KK. Impact of HPV vaccination on anogenital warts and respiratory papillomatosis. Hum Vaccin Immunother. 2016 Jun 2;12(6):1357-62. doi: 10.1080/21645515.2016.1172754. Epub 2016 May 23. PMID: 27217191; PMCID: PMC5036961. https://pubmed.ncbi.nlm.nih.gov/27217191/
- Genital Warts in Women Vaccinated against HPV in Childhood: A Systematic Review - MDPI, дата последнего обращения: декабря 7, 2025, https://www.mdpi.com/2076-393X/12/5/548
- Аногенитальные (венерические) бородавки (ВПЧ, папилломавирус, кондилома) (РОАГ) – 2024-2025-2026 (12.07.2024) – Утверждены Минздравом РФ - Скачать, распечатать, читать онлайн - Клинические рекомендации (протоколы лечения) - http :// disuria. ru, дата последнего обращения: декабря 7, 2025, http://disuria.ru/load/zakonodatelstvo/klinicheskie_rekomendacii_protokoly_lechenija/anogenitalnye_venericheskie_borodavki_vpch_papillomavirus_kondiloma_roag_2024_2025_2026_12_07_2024_utverzhdeny_minzdravom_rf/54-1-0-1441
- EAU Guidelines on Urological Infections - Cloudfront.net, дата последнего обращения: декабря 7, 2025, https://d56bochluxqnz.cloudfront.net/documents/full-guideline/EAU-Guidelines-on-Urological-Infections-2024.pdf
- Summary of CDC STI Treatment Guidelines, 2021, дата последнего обращения: декабря 7, 2025, https://www.cdc.gov/std/treatment-guidelines/wall-chart.pdf
- HPV and Recurrent Respiratory Papillomatosis: A Brief Review - MDPI, дата последнего обращения: декабря 7, 2025, https://www.mdpi.com/2075-1729/11/11/1279
- IUSTI 2019 Europe guideline for the management of anogenital warts, дата последнего обращения: декабря 7, 2025, https://iusti.org/wp-content/uploads/2020/08/IUSTIHPVGuidelines2020.pdf
- Non-Invasive Imaging for the Diagnosis of Genital Warts and Their Imitators - MDPI, дата последнего обращения: декабря 7, 2025, https://www.mdpi.com/2077-0383/13/5/1345
- Clinical utility of dermoscopy in diagnosing pigmented genital warts: A case report, дата последнего обращения: декабря 7, 2025, https://jpad.com.pk/index.php/jpad/article/download/2233/2061
- Veasey JV, Framil VM, Nadal SR, Marta AC, Lellis RF. Genital warts: comparing clinical findings to dermatoscopic aspects, in vivo reflectance confocal features and histopathologic exam. An Bras Dermatol. 2014 Jan-Feb;89(1):137-40. doi: 10.1590/abd1806-4841.20141917. PMID: 24626658; PMCID: PMC3938364. https://pubmed.ncbi.nlm.nih.gov/24626658/
- Application of dermoscopy image analysis technique in diagnosing urethral condylomata acuminata - PMC - NIH, дата последнего обращения: декабря 7, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC5871365/
- Human Papillomavirus (HPV) Infection - STI Treatment Guidelines, дата последнего обращения: декабря 7, 2025, https://www.cdc.gov/std/treatment-guidelines/anogenital-warts.htm
- Anogenital warts 2024 - BASHH, дата последнего обращения: декабря 7, 2025, https://www.bashh.org/resources/96/anogenital_warts_2024/
- Аногенитальные (венерические) бородавки > Клинические рекомендации РФ 2024 (Россия) https://cr.minzdrav.gov.ru/preview-cr/204_2
- A short, 8-week course of imiquimod 5% cream versus podophyllotoxin in the treatment of anogenital warts: A retrospective comparative cohort study, дата последнего обращения: декабря 7, 2025, https://ijdvl.com/a-short-8-week-course-of-imiquimod-5-cream-versus-podophyllotoxin-in-the-treatment-of-anogenital-warts-a-retrospective-comparative-cohort-study/?fbclid=IwAR0MnQ2mNHxU6z7hSS_Ikw4zjDTrBXJItB0wUFfcg_4zP_ohpWpiT0yggXw
- Effectiveness of topical and ablative therapies in treatment of anogenital warts: a systematic review and network meta- analysis - BMJ Open, дата последнего обращения: декабря 7, 2025, https://bmjopen.bmj.com/content/bmjopen/9/10/e027765.full.pdf
- Comparing Thulium Laser and Nd:YAG Laser in the Treatment of Genital and Urethral Condylomata Acuminata in Male Patients - ResearchGate, дата последнего обращения: декабря 7, 2025, https://www.researchgate.net/publication/257648732_Comparing_Thulium_Laser_and_NdYAG_Laser_in_the_Treatment_of_Genital_and_Urethral_Condylomata_Acuminata_in_Male_Patients
- Discussion - Clinical effectiveness and cost-effectiveness of interventions for the treatment of anogenital warts: systematic review and economic evaluation - NCBI, дата последнего обращения: декабря 7, 2025, https://www.ncbi.nlm.nih.gov/books/NBK355277/
- Pan-urethral Wart Treated with 5-Fluorouracil Intraurethral Instillation - ResearchGate, дата последнего обращения: декабря 7, 2025, https://www.researchgate.net/publication/6821283_Pan-urethral_Wart_Treated_with_5-Fluorouracil_Intraurethral_Instillation
- Kovachev SM. A Review on Inosine Pranobex Immunotherapy for Cervical HPV-Positive Patients. Infect Drug Resist. 2021 Jun 2;14:2039-2049. doi: 10.2147/IDR.S296709. PMID: 34103950; PMCID: PMC8180272 дата последнего обращения: декабря 7, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC8180272/
- Study Details | NCT03296397 | Efficacy of Quadrivalent HPV Vaccine to Prevent Relapses of Genital Warts After Initial Therapeutic Response | ClinicalTrials.gov, дата последнего обращения: декабря 7, 2025, https://www.clinicaltrials.gov/study/NCT03296397
- Ciccarese G, Herzum A, Serviddio G, Occella C, Parodi A, Drago F. Efficacy of Human Papillomavirus Vaccines for Recalcitrant Anogenital and Oral Warts. J Clin Med. 2023 Nov 26;12(23):7317. doi: 10.3390/jcm12237317. PMID: 38068369; PMCID: PMC10706929, дата последнего обращения: декабря 7, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC10706929/
- Di Donato V, Caruso G, Petrillo M, Kontopantelis E, Palaia I, Perniola G, Plotti F, Angioli R, Muzii L, Benedetti Panici P, Bogani G. Adjuvant HPV Vaccination to Prevent Recurrent Cervical Dysplasia after Surgical Treatment: A Meta-Analysis. Vaccines (Basel). 2021 Apr 21;9(5):410. doi: 10.3390/vaccines9050410. PMID: 33919003; PMCID: PMC8143003, дата последнего обращения: декабря 7, 2025, https://pubmed.ncbi.nlm.nih.gov/33919003/
- Timing of HPV vaccination as adjuvant treatment of CIN2+ recurrence in women undergoing surgical excision: a meta-analysis and meta-regression | Sexually Transmitted Infections, дата последнего обращения: декабря 7, 2025, https://sti.bmj.com/content/99/8/561
- Effect of human papillomavirus (HPV) vaccination on HPV infection and recurrence of HPV related disease after local surgical treatment: A systematic review and meta-analysis | PLOS One - Research journals, дата последнего обращения: декабря 7, 2025, https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0312128
- HPV vaccination and prevention of ano-genital warts recurrence: a systematic review and meta-analysis - Consensus, дата последнего обращения: декабря 7, 2025, https://www.consensus.app/search/hpv-vaccination-and-prevention-of-ano-genital-wart/DzECk_10R0qA2_urMN4vXw/
- Asl FM, Ghaffari P, Safari M. The relationship between the recurrence rate of genital warts and administration of quadrivalent human papilloma virus vaccine in women. Diagn Microbiol Infect Dis. 2025 Feb;111(2):116607. doi: 10.1016/j.diagmicrobio.2024.116607. Epub 2024 Nov 16. PMID: 39580907. PubMed, дата последнего обращения: декабря 7, 2025, https://pubmed.ncbi.nlm.nih.gov/39580907/
- Приказ Министерства здравоохранения Российской Федерации от 15.03.2022 № 168н. Официальное опубликование правовых актов, дата последнего обращения: декабря 7, 2025, http://publication.pravo.gov.ru/Document/View/0001202204210027







 Скачать
Скачать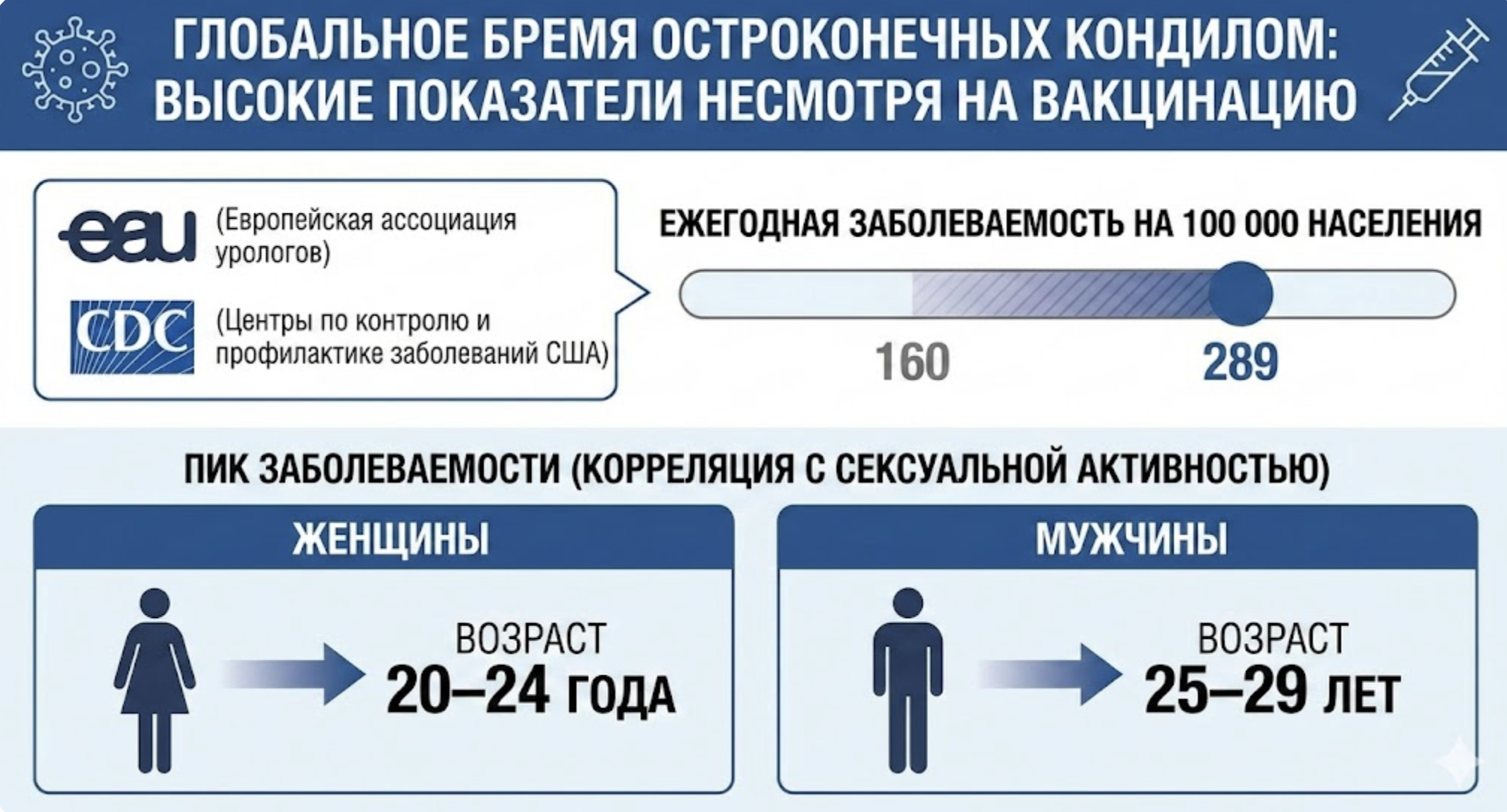











Комментарии