Просянников М.Ю., Анохин Н.В., Голованов С.А., Константинова О.В., Сивков А.В., Аполихин О.И.
Сведения об авторах:
- Просянников М.Ю. – к.м.н., зав. отделом мочекаменной болезни НИИ урологии и интервенцион- ной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России, prosyannikov@gmail.com. AuthorID 791050
- Анохин Н.В. – к.м.н., научный сотрудник отдела мочекаменной болезни НИИ урологии и интер- венционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России, anokhinnikolay@yandex.ru, AuthorID 880749
- Голованов С.А. – д.м.н., руководитель группы клинической лабораторной диагностики научно- лабораторного отдела НИИ урологии и интервенционной радиологии им. Н.А.Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России, sergeygol124@mail.ru, AuthorID 636685
- Константинова О.В. – д.м.н., главный научный сотрудник отдела мочекаменной болезни НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиоло- гии» Минздрава России, konstant-ov@yandex.ru, AuthorID 679965
- Сивков А.В. – к.м.н., заместитель директора по научной работе научно-исследовательского института урологии и интервенционной радиологии им. Н.А. Лопаткина - филиал ФГБУ «НМИРЦ» Минздрава России; uroinfo@yandex.ru, ID 622663
- Аполихин О.И. – д.м.н., профессор, член-корр. РАН, директор НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИЦ радиологии» Минздрава России. sekr.urology@gmail.ru, AuthorID: 683661
Проведенные эпидемиологические исследования мочекаменной болезни (МКБ) показали, что кальцийсодержащие конкременты встречаются в среднем в 80% случаев, при этом больший процент принадлежит кальций-оксалатным камням (до 60%) [1,2].
В то же время показано, что гиперкальциурия (ГКУ) является одним из основных метаболических литогенных нарушений, диагностируемых при МКБ [3,4], а частота встречаемости ГКУ при МКБ варьирует от 20 до 50 % [5]. Известно, что причиной ГКУ могут быть как наследственные заболевания, так и наличие приобретенных сопутствующих патологический состояний и синдромов. К ГКУ также могут приводить различные факторы окружающей среды. Одной из наиболее распространенных причин ГКУ является погрешность в диете [5].
В настоящее временя имеются многочисленные исследования, свидетельствующие о значимой роли кальция в патогенезе МКБ [3,6], поэтому оценка метаболического статуса пациента должна включать изучение метаболизма кальция.
Кальций является незаменимым макроэлементом в организме человека. Согласно современным представлениям от 30 до 40 % кальция, поступаемого с пищей, всасывается в кишечнике, при этом большая часть абсорбируется в тонкой кишке и только 10% в толстой. Основное депо кальция в организме человека – это кости и зубы, где находится до 99% кальция всего организма. Около 1% этого макроэлемента циркулирует в биологических жидкостях человека [7]. Количество всасываемого в желудочно-кишечном тракте кальция зависит от объема его потребления. При низком потреблении элемента повышается уровень его абсорбции, при высоком потреблении – поглощение кальция уменьшается.
Для пациентов, страдающих МКБ, необходимо помнить, что наибольшее количество алиментарного кальция поглощается при дробном потреблении продуктов, богатых этим макроэлементом. При одномоментном приеме большой разовой дозы абсорбция кальция из желудочно-кишечного тракта будет наименьшей [7].
Почками фильтруется 8,6 г кальция в сутки, он практически весь реабсорбируется и только 100-200 мг экскретируется с мочой, что соответствует средней суточной экскреции кальция в пределах от 2,0 до 5,0 мМоль/сут. Необходимо помнить, что экскреция кальция происходит в равных количествах с мочой и кишечным содержимым. Около 150 мг кальция в сутки секретируется в просвет кишечника с кишечным соком и желчью. Около 30% из этого количества кальция абсорбируются. Минимальная фекальная экскреция кальция составляет 100 мг/сутки [7]. Через кожу здоровый человек теряет приблизительно 15 мг кальция в сутки, при потоотделении это количество существенно увеличивается [8].
Четкое представление о нормальном обмене кальция необходимо для оценки метаболического статуса пациента с МКБ и для патогенетически обоснованной коррекции нарушений, ведущих к камнеобразованию при уролитиазе. Учитывая значимую роль кальция в патогенезе МКБ, доказанное влияние ГКУ на инициацию процессов камнеобразования при уролитиазе [3,4], было принято решение изучить силу воздействия степени кальциурии на вероятность образования камней различного химического состава при МКБ.
МАТЕРИАЛЫ И МЕТОДЫ
В исследовании проанализированные данные химического состава 708 мочевых камней от 303 мужчин и 405 женщин. Все пациенты проходили обследование и лечение в клинике НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиале «НМИЦ радиологии» Минздрава России.
Исследование проводилось ретроспективно. Всем пациентам выполняли анализ химического состава мочевого камня методом инфракрасной спектроскопии и биохимический анализ суточной мочи.
Химический состав мочевых конкрементов определялся методом инфракрасной спектроскопии с использованием спектрометра Nicolet iS10 (Thermo Scientific, США). Использовалась стандартная библиотека спектров мочевых камней, предоставленная производителем. При наличии в смешанном мочевом конкременте более 50% минерального компонента от всей минеральной основы химический состав камня относился к группе конкрементов по преобладающему элементу (оксалатные, мочекислые, фосфатные (из карбонатапатита или струвита).
Биохимический анализ суточной экскреции мочи проводился на анализаторе ADVIA 1200 (Bayer-Siemens) по стандартным методикам с помощью диагностических наборов реагентов фирмы Siemens (Германия). При биохимическом анализе суточной мочи исследовали уровень экскреции кальция.
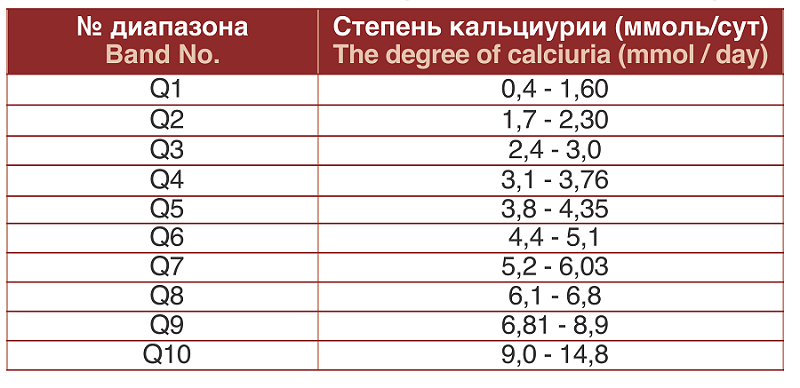
Для анализа силы воздействия уровня кальциурии на частоту формирования камней различного химического состава использовался метод разделения ранжированного вариационного ряда показателей кальциурии на 10 диапазонов, в каждом из которых насчитывалось от 64 до 75 наблюдений. В итоге в первый (Q1) диапазон распределения попадали все случаи с самыми низкими показателями кальциурии, а в последний (Q10) – с самыми высокими значениями (табл. 1).
Достоверность различия между частотами выявления камней различного химического состава при разной степени кальциурии оценивали с использованием статистического критерия Хи-квадрат Пирсона.
Таблица 1. Распределение степени кальциурии на диапазоны
Table 1. The distribution of the degree of calciuria in the ranges
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты определения выраженности кальциурии и частоты выявления мочевых камней различных метаболических типов представлены в таблице 2.
Таблица 2. Степень кальциурии и частота формирования мочевых камней различного химического состава
Table 2. The degree of calciuria and the frequency of formation of urinary stones of various chemical composition
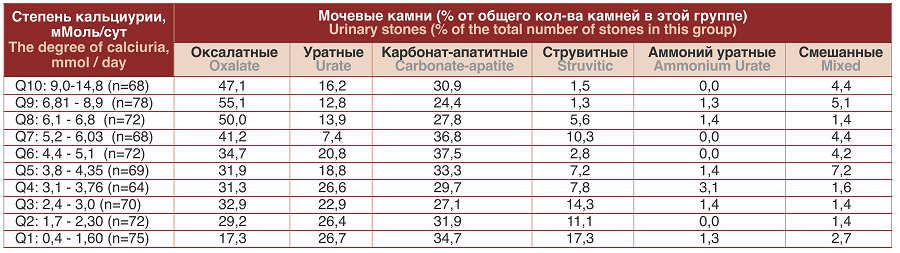
Известно, что ГКУ является одним из наиболее значимых метаболических факторов риска развития кальциевых мочевых камней [3,9,10.]. Результаты показывают, что ГКУ при уровне экскреции общего кальция более 4,4 мМоль/сут заметно повышает частоту формирования кальций-оксалатных камней (табл. 2). Частота встречаемости кальций-оксалатных конкрементов статистически достоверно увеличивается при изменении диапазона кальциурии от 4,4 – 5,1 мМоль/сут до диапазона 6,84 – 8,9 мМоль/сут на 20,4% (р=0,004), (табл. 3).
Таблица 3. Влияние различных уровней ГКУ на частоту формирования мочевых камней различного химического состава
Table 3. The effect of different levels of HCU on the frequency of formation of urinary stones of various chemical composition
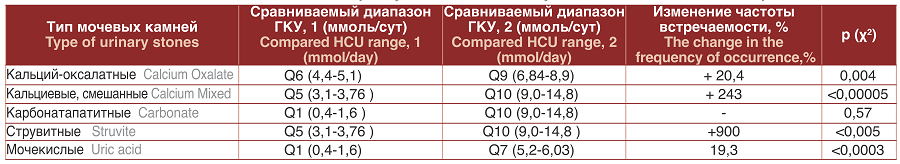
Полученные в настоящем исследовании данные подтверждают значимую роль ГКУ в генезе кальций-оксалатных камней. В одном из известных классических когортных исследований состояния здоровья медицинского персонала были получены схожие данные [11]. При обследовании 238 371 женщин 25 – 55 лет и 51 529 мужчин 40 – 75 лет были получены данные, указывающие на повышение относительного риска формирования кальций-оксалатных камней, начиная с диапазона экскреции кальция 200-249 мг (5,0-6,25 мМоль) в сутки.
Проведенное нами настоящее исследование также показало, что с возрастанием степени кальциурии также растет частота формирования кальциевых (оксалатно-фосфатных) камней. Причем заметный рост частоты выявления этих типов камней наблюдается при кальциурии выше 3,76 мМоль/сут. Частота встречаемости кальциевых камней статистически достоверно увеличивается в диапазоне кальциурии 3,1-3,76 мМоль/сут по сравнению с диапазоном 9,0-14,8 мМоль/сут в 2,43 раза (p<0,00005), (табл. 3).
Необходимо подчеркнуть, что кальциевые конкременты – это смешанные кальций–оксалатные и кальцийфосфатные камни. В эту группу не входили мономинеральные кальций содержашие конкременты, представленные на 100% либо кальций-оксалатом (вевеллит+веделлит), или на 100% кальций-фосфатом (карбонатапатит).
В соответствии с рекомендациями Европейской ассоциации урологов, Американской ассоциации урологов и многочисленными научными публикациями, посвященными теме ГКУ при уролитиазе, предусмотрено, что экскрецию кальция более 5 мМоль/сут, диагностированную у пациентов с МКБ, следует считать верхним пороговым нормальным уровнем кальциурии. ГКУ более 5,0 мМоль/сут требует проведения диетотерапии и/или консервативной терапии по устранению этого фактора риска [12,13].
Наше исследование показало, что, вероятно, пороговый уровень допустимой кальциурии при кальций-оксалатном уролитиазе необходимо снизить до значений 4,3-4,5 мМоль/сут. Тем не менее, данный вопрос является дискутабельным и требует проведения большего количества исследований и дополнительного набора данных.
Необходимо подчеркнуть, что в литературе также встречаются и другие значения экскреции кальция, принимаемые в качестве критериев ГКУ – 6,25 мМоль/сутки для женщин и 7,5 мМоль/сутки – для мужчин [14]. Можно полагать, что данные пороговые значения в настоящее время требуют пересмотра, поскольку не могут в полной мере отражать литогенный потенциал кальциурии и применяться при выборе тактики противорецидивного лечения в ходе динамического мониторинга пациентов с МКБ.
Результаты проведенного анализа также показывают, что ни высокая, ни низкая степень кальциурии не оказывали влияния на частоту образования кальций-фосфатных (карбонатапатитных) камней (табл. 1). При сравнении различных диапазонов степени кальциурии (Q1-Q10) частота встречаемости карбонатапатитных конкрементов не изменилась (p=0,63), (табл. 3). Наши данные согласуются с результатами мировых исследований, по результатам которых утверждается, что степень кальциурии не влияет на частоту формирования камней из карбонатапатита [9]. Отчасти это может быть связано с тем, что при определенных обстоятельствах инфекция мочевых путей может быть причиной формирования карбонатапатитных конкрементов [12 ].
При анализе степени кальциурии и частоты формирования струвитных конкрементов, отмечено, что при увеличении уровня кальциурии с 3,0 мМоль/сут по 14,8 мМоль/сут встречаемость струвитных камней снижалась более, чем в 10 раз (р < 0,005) по сравнению с группой пациентов, имевшими низкий уровень кальциурии (0,4-3,0 мМоль/сут), (табл. 3).
В настоящем исследовании показано, что ГКУ выше 5,0 мМоль/сут не приводит к увеличению риска образования мочекислых камней (табл. 1). Более того, прослеживается выраженное снижение частоты встречаемости мочекислых конкрементов более чем на 19,3% от общего количества камней (p=0,002) при возрастании кальциурии в диапазонах 0,4-1,6 мМоль/сут до 5,2-6,03 ммоль/сут (табл. 3), (p<0,0003). Похожие данные получены в работах C.Y. Pak и соавт., где также была отмечена низкая частота встречаемости мочекислых камней при абсорбтивной ГКУ, которая у таких больных довольно часто сочеталась с гиперурикурией [9].
ВЫВОДЫ
Результаты настоящего исследования позволяют сделать вывод о том, что, такой главный метаболический фактор риска уролитиаза как ГКУ с уровнем экскреции выше 5,0 мМоль/сут следует рассматривать как фактор, ведущий к формированию исключительно кальций-оксалатных камней, но не кальций-фосфатных (карбонатапатитных) мочевых камней, в генезе которых, как известно, участвуют другие ведущие механизмы, напрямую не связанные с ГКУ. При этом необходимо провести дополнительную работу по изучению верхнего порогового уровня кальциурии, при котором возрастает риск формирования кальций-оксалатных камней.
ЛИТЕРАТУРА
- Голованов С.А., Сивков А.В., Анохин Н.В., Дрожжева В.В. Тенденции распространенности метаболических типов мочекаменной болезни в Московском регионе. Сравнительный анализ за период с 2010 по 2013 гг. Экспериментальная и клиническая урология 2014;(4):54-59. [Golovanov S.A., Sivkov A.V., Anokhin N.V., Drozhzheba V.V. [Trends in the prevalence of metabolic types of urolithiasis in the Moscow region. Comparative analysis for the period from 2010 to 2013. Eksperimentalnaya i klinicheskaya urologiya=Experimental and clinical urology 2014;(4):54-59. (In Russian)].
- Sorokin I, Mamoulakis C, Miyazawa K, Rodgers A, Talati J, Lotan Y Epidemiology of stone disease across the world. World J Urol 2017;35(9):1301-1320. doi: 10.1007/s00345-017-2008-6.
- Константинова О.В. Прогнозирование и принципы профилактики мочекаменной болезни. Дисс. докт. мед. наук, М., 2000, 234 с. [Konstantinova O.V. Prediction and principles of prevention of urolithiasis. Dr. Med.Sci [dissertation]. M., 2000, 234 p. (In Russian)].
- Pac C.Y.C, Sakhaee K., Moe O.W., Poindexter J., Adams-Huet B. Defining hypercalciuria in nephrolithiasis. Kidney International 2011;(1):777-782.
- Coe FL, Worcester EM, Evan AP. Idiopathic hypercalciuria and formation of calcium renal stones. Nat Rev Nephrol 2016;12(9):519-33. doi: 10.1038/nrneph.2016.101.
- Ramaswamy K, Killilea DW, Kapahi P, Kahn AJ, Chi T, Stoller ML. The elementome of calcium-based urinary stones and its role in urolithiasis. Nat Rev Urol 2015;12(10):543-57. doi: 10.1038/nrurol.2015.208.
- Искендеров Б.Г. Артериальная гипертензия и метаболизм кальция: Монография. Пенза: 2010, 224 с. [Iskenderov B.G. Hypertension and calcium metabolism. Penza: 2010, 224 p. (In Russian)].
- Ritz E, Massry SG. The kidney in disorders of calcium metabolism. Contrib Nephrol 1977;7:114-27.
- Pak CY, Poindexter JR, Adams-Huet B, Pearle MS. Predictive value of kidney stone composition in the detection of metabolic abnormalities. Am J Med 2003;115(1):26-32.
- Worcester EM, Coe FL. New insights into the pathogenesis of idiopathic hypercalciuria. Semin Nephrol 2008;28(2):120-32. doi: 10.1016/j.semnephrol.2008.01.005.
- Curhan GC, Taylor EN. 24-h uric acid excretion and the risk of kidney stones. Kidney Int 2008; 73(4):489-96. doi: 10.1038/sj.ki.5002708.
- Turk C, Knoll T, Petřik A, Sarica K, Skolarikos A , Straub M, Seitz C. Guidelines on Urolithiasis. EAU, 2015. URL: http://uroweb.org/wp-content/uploads/22-Urolithiasis_LR_full.pdf.
- Pearle M.S., Goldfarb D.S., Assimos D.G., Curhan G, Denu-Ciocca C.J., Matlaga B.R., Monga M., Penniston K.L., Preminger G.M., Turk T.M.T., White J.R. Medical management of kidney stones: aua guideline. https://www.auanet.org/education/guidelines/management-kidney-stones.cfm.
- Parks JH, Coe FL. A urinary calcium-citrate index for the evaluation of nephrolithiasis. Kidney Int 1986;30(1):8.
Статья опубликована в журнале "Экспериментальная и клиническая урология" №3 2019, стр. 100-103











Комментарии