С.А. Голованов, А.В. Сивков, Н.В. Анохин
НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина – филиал ФГБУ «НМИРЦ» Минздрава России
Мочекаменная болезнь (МКБ) является общемировой проблемой. За последние 20 лет зарегистрирован неуклонный рост заболеваемости МКБ [1]. В Российской Федерации отмечен прирост числа пациентов за период с 2003 по 2013 годы на 26,6%: в 2013 г. зарегистрировано 805 212 человек с мочекаменной болезнью, тогда как в 2003 году таких пациентов было 635 812. В среднем по Российской Федерации в 2013 г. показатель числа пациентов с мочекаменной болезнью на 100 тыс. всего населения составил 561,7, тогда как в 2003 г. он равнялся 443 [2]. В ближайшем будущем ожидается увеличение частоты случаев МКБ вследствие изменения образа жизни людей, экологии, качества потребляемой пищи и увеличения числа лиц, страдающих ожирением [3,4].
Наиболее распространенными формами МКБ являются кальцийоксалатный и кальций-фосфатный уролитиаз. Согласно данным эпидемиологических исследований, проведенных в различных странах, кальций-оксалатный уролитиаз встречается у 37-82,5% пациентов, а кальций-фосфатный – у 33% больных [5-7,8]. При анализе конкрементов пациентов из Московского региона за периоды 1990-2000 гг. и 2005-2009 гг. установлено, что частота выявления кальций-оксалатного уролитиза имела тенденцию к росту: 63,4% и 64,8% соответственно [9]. Прогрессивный рост случаев кальций-оксалатного уролитиаза в последние годы наблюдают и среди населения многих индустриально развитых стран [10,11].
Важной характеристикой МКБ является тенденция к рецидивному камнеобразованию, которое по данным разных авторов наблюдают, приблизительно, в 50% случаев в течение 5 лет после первого эпизода заболевания [12,13]. Приведенные данные свидетельствуют о необходимости разработки действенных мер, направленных на снижение заболеваемости МКБ. В этом плане особую роль приобретают методы противорецидивного лечения (метафилактики) МКБ.
МЕТАФИЛАКТИКА МКБ: НЕРЕШЕННАЯ ПРОБЛЕМА
Пациенту, страдающему МКБ, традиционно, осуществляют комплекс инструментальных и лабораторных исследований, необходимых для определения тактики лечения пациента, в зависимости от числа, размеров и локализации уже существующих конкрементов. Однако, как правило, после оперативного или малоинвазивного лечения МКБ, должная профилактика повторного камнеобразования пациентам не проводится. В результате – большинство больных, рано или поздно, снова попадают в стационар (часто по экстренным показаниям) с рецидивом камнеобразования. Многие практикующие урологи при МКБ формально подходят к проведению противорецидивного лечения, ограничиваются лишь общими рекомендациями. Недостаточна подготовка большинства урологов (в первую очередь поликлинических) по проблеме метафилактики МКБ. Не работает система динамического наблюдения за пациентами с рецидивным камнеобразованием.
Помимо анамнестических, физикальных, инструментальных, клинико-лабораторных данных, особое внимание необходимо уделять результатам биохимического исследования суточной мочи, крови, химическому составу мочевого камня. В этой связи серьезную проблему составляет тот факт, что лабораторные службы многих учреждений не готовы осуществлять сложную дифференциальную диагностику многообразия видов метаболических литогенных нарушений, приводящих к камнеобразованию. В большинстве медучреждений отсутствует оборудование для определения состава мочевых камней.
Необходимыми условиями успешной метафилактики МКБ являются:
- устранение нарушений уродинамики верхних мочевых путей;
- ликвидация мочевой инфекции;
- выявление метаболических нарушений, способных привести к рецидиву камнеобразования и оценка степени их литогенности.
МЕТОДИКА ОБСЛЕДОВАНИЯ
Для проведения метафилактики МКБ врачу урологу необходимо назначить пациенту следующие обследования:
- определить антропометрические показатели пациента, исключить метаболический синдром;
- сдать посев мочи на флору и чувствительность к антибиотикам для исключения инфекции мочевых путей;
- выполнить ультразвуковое исследование органов мочевыделительной системы для исключения признаков нарушения уродинамики; определить химический состав камня;
- выполнить биохимический анализ крови, с определением уровней креатинина, мочевины, кальция, мочевой кислоты, фосфора, магния, хлора, натрия, калия;
- выполнить биохимический анализ суточной мочи, с определением уровней экскреции кальция, мочевой кислоты, фосфора, оксалатов, цитратов, магния, натрия, калия, креатинина;
- провести измерение pH мочи и суточного диуреза в течение нескольких суток;
- при определенных состояниях необходим анализ уровня паратгормона и активной формы витамина D (D-25OH) в крови.
Биохимический анализ крови и мочи целесообразно выполнять через 30 дней после удаления (отхождения) камня, по возможности, анализировать 2 последовательных сбора суточной мочи с интервалом 7-10 дней.
В определенных случаях, по показаниям, необходимо проводить специальные пробы для дифференциальной диагностики нарушения: исследование экскреции кальция после низкокальциевой диеты; проба с применением пшеничных отрубей; тиазидная провокация (табл. 1). На основании имеющихся клинических данных уролог выбирает соответствующую тактику противорецидивного лечения.
Таблица 1. Низкокальциевая диета, проба с отрубями, тиазидная провокация
| А | Низкокальциевая диета |
|---|---|
| После соблюдения 3-х дневной диеты (исключить молоко, кефир, йогурты, сыры, брынзу, творог, сметану, миндаль, фисташки, горчицу, фасоль, грецкие орехи, овсянку) выполняют сбор суточной мочи для определения экскреции кальция: при кальциурии менее 6,25 мМ/сут., диагностируют абсорбтивную гиперкальциурию II типа. |
|
| В | Проба с применением пшеничных отрубей |
| Выполняют для дифференциальной диагностики гиперкальциурии I и II типов. На фоне низкокальциевой диеты к рациону добавляют пшеничные отруби по 2 ст. ложки 3 раза в день во время еды в течение последующих 3-х дней, после чего проводят сбор суточной мочи с определением уровня кальция в моче. При выявлении кальциурии менее 6,25 мМ/сут, диагностируют абсорбтивную гиперкальциурию I типа. |
|
| С | Тиазидная провокация |
| Если после назначения тиазидных диуретиков, у пациента отмечена выраженная гиперкальциемия, то это свидетельствует в пользу резорбтивной гиперкальциурия. |
Важными задачами метафилактики МКБ являются: снижение концентрации в моче камнеобразующих веществ, увеличение содержания в моче ингибиторов камнеобразования и, если это необходимо, оптимизация уровня рН мочи [14]. В то же время следует отметить, что даже правильно проведенная метафилактика МКБ не гарантирует отсутствия рецидива камнеобразования.
ГИПЕРКАЛЬЦИУРИЯ И ЕЕ ВИДЫ
Под гиперкальциурией понимают превышение суточной экскреции кальция с мочой для женщин более 6,2 мМ/сут, а для мужчин – более 7,5 мМ/сут [15].
Важно понимать, что гиперкальциурия не представляет собой самостоятельное заболевание, а является метаболическим симптомом или лабораторным признаком, характерным для большого числа различных патологических состояний и заболеваний, каждое из которых требует индивидуального подхода (рис. 1).
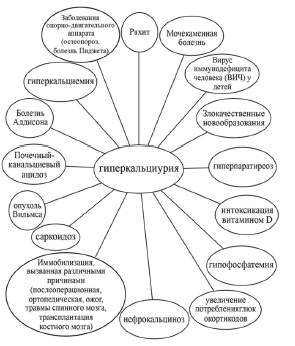
Рис. 1. Причины гиперкальциурии
У большинства пациентов, страдающих МКБ, формируются кальцийсодержащие камни: оксалатные или фосфатные [5-7, 12]. Нередко им сопутствует гиперкальциурия – основное литогенное нарушение обмена веществ при кальциевом уролитиазе. Гиперкальциурию выявляют у большинства пациентов, страдающих МКБ: 35-65% [16].
В настоящих рекомендациях рассмотрены диагностические подходы к выявлению основных типов гиперкальциурии, представлен практический алгоритм дифференциальной диагностики типов гиперкальциурии, что необходимо для выбора правильной тактики противорецидивной терапии.
Высокая концентрация кальция в моче ведет к увеличению насыщения мочи его солями и снижает ингибирующую активность мочи путем комплексообразования с отрицательно заряженными ингибиторами, такими как цитрат и хондроитина сульфат [16], в конечном счете, может инициировать кристаллои камнеобразование. Гиперкальциурии свойственно большое многообразие видов, поскольку в основе их формирования лежат различные патогенетические механизмы.
Для успеха противорецидивного лечения важен выбор адекватной патогенетической коррекции того или иного вида гиперкальциурии. С этой целью необходимо дифференцировать несколько типов гиперкальциурии:
- абсорбтивная – развивается в результате нарушения всасывания кальция в кишечнике;
- ренальная – наблюдается вследствие увеличения суточной экскреции кальция почками;
- резорбтивная – возникает вследствие повышенной деминерализации костной ткани;
- гиперкальциурия при почечном канальцевом ацидозе I типа (дистальном)
- развивается вследствие нарушенной реабсорбции кальция в почечных канальцах [13, 16];
Особенности патогенеза основных видов гиперкальциурии и их характерные лабораторные признаки приведены в табл. 2.
Таблица 2. Виды гиперкальциурии
| Вид гиперкальциурии | Тип | Патогенез | Лабораторные проявления |
|---|---|---|---|
| Абсорбтивная | I тип | Значительно увеличена абсорбции кальция из желудочно-кишечного тракта |
Гиперкальциурия сохраняется на фоне низкокальциевой диеты |
| II тип | Умеренно повышена абсорбции кальция из желудочно-кишечного тракта |
Гиперкальциурия исчезает на фоне низкокальциевой диеты. |
|
| III тип | Потеря фосфора с мочой Активация витамина D |
Гипофосфатемия, гиперфосфатурия. Сопутствующие гиперкальциемия и гиперкальциурия. |
|
| IV тип | Идиопатическая гиперпродукция витамина D-3 |
Высокая концентрация вит. D крови. Гиперкальциемия, гиперкальциурия.Низкий уровень паратгормона. |
|
| Ренальная | Нарушение реабсорбции кальция в почечных канальцах. Повышение уровня кальция в моче. Вторичный гиперпаратиреоз. Повышено всасывание кальция в кишечнике. |
Нормокальциемия. Высокий уровень паратгормона. Высокая гиперкальциурия натощак. |
|
| Резорбтивная | Первичный гиперпаратиреоз. Резорбция костной ткани. Повышение синтеза витамина D. |
Повышение уровня паратгормона сыворотки крови. Гиперкальциемия. |
|
| Почечный канальцевый ацидоз |
I тип | Уменьшение реабсорбции кальция в почечных канальцах в следствие хронического ацидоза |
Гиперхлоремия, Гиперкальциурия, гиперфосфатурия. |
Абсорбтивная гиперкальциурия – наиболее часто встречающаяся причина повышения экскреции кальция с мочой, которую в той или иной форме выявляют приблизительно у 50% пациентов с кальциевыми камнями [17]. В ее основе лежит увеличение абсорбции кальция из желудочно-кишечного тракта вследствие высокой концентрации витамина D или избыточного потребления кальций содержащих продуктов. Всасывание кальция происходит только в двенадцатиперстной кишке и в норме не должно превышать 20% от его потребления с пищей. Повышенное всасывание кальция в кишечнике, соответственно, увеличивает его концентрацию в плазме крови. При этом обычно уровень паратгормона в крови снижен или находится на нижней границе нормы.
Выделяют 4 типа абсорбтивной гиперкальциурии:
I тип встречается относительно редко (15% всех случаев гиперкальциурии) и считается самым тяжелым. Этот тип гиперкальциурии практически не корригируется низкокальциевой диетой, даже при серьезном ограничении потребления кальций содержащих продуктов. Важным характерным признаком абсорбтивной гиперкальциурии I типа является нормализация отношения кальций/креатинин при определении экскреции кальция и креатинина натощак.
II тип (основной) достигает 75% всех случаев гиперкальциурии. При этом варианте, после ограничения продуктов содержащих кальций, например, в виде 3-х дневной низкокальциевой диеты, отмечается снижение экскреции кальция с мочой и исчезновение гиперкальциурии. Соответственно, основным методом коррекции гиперкальциурии II типа, является изменение характера питания. При этом следует обратить внимание на то, что дневное потребление кальция с пищей не должно быть ниже физиологической нормы в 800 – 1200 мг в сутки.
III тип, сравнительно редкий тип гиперкальциурии (8% всех случаев). Основное звено патогенеза этого нарушения – потеря фосфатов в почках в результате ферментного дефекта, проявляющегося чрезмерной экскрецией фосфатов с мочой. Это ведет к понижению концентрации фосфора в плазме крови – гипофосфатемии. Низкий уровень фосфора крови активирует витамин D-3, который, в свою очередь, повышает всасывание в кишечнике, как фосфора, так и кальция. Вследствие высокой концентрации кальция в плазме крови и возникает гиперкальциурия. Таким образом, этот ее тип является абсорбтивным, из-за потери фосфора с мочой и гиперпродукции витамина D-3.
Недавно обнаружена сложносоставная гетерои гомозиготная мутация гена SLC34A3/NPT2с, которая сопровождается абсорбтивной гиперкальциурией III типа (некоторые авторы называют ее идиопатической). Этот ген кодирует информацию о структуре натрий-зависимого котранспортера фосфора. Мутация гена SLC34A3/NPT2с вызывает наследственный гипофосфатемический рахит с гиперкальциурией. Заболевание проявляется повышенной экскрецией фосфора в почках, гипофосфатемией и повышением уровня витамина D-3. Пациенты с мутацией, затрагивающей обе аллели гена SLC34A3/NPT2с, подвержены значительному риску камнеобразования [18, 19]. Основной метод коррекции нарушения – применение ортофосфатов.
IV тип связан с идиопатической гиперпродукцией витамина D-3, которая, в свою очередь, усиливает всасывание кальция из кишечника и стимулирует гиперкальциурию. Недавние генетические исследования обнаружили мутацию гена CYP24A1, кодирующего информацию о структуре фермента 1,25(OH)2D-24-гидроксилаза. Мутация приводит к снижению активности фермента, стимулирующего превращение активных форм витамина D 25(OH)D3 и 1,25(OH)2D3 в неактивную форму витамина 24,25(OH)2D3. Фермент превращает большинство активных форм витамина D в неактивные метаболиты. Таким образом, у пациентов отмечается высокий уровень активного витамина D (1,25(OH)2D3) и низкий уровень неактивного витамина D (24,25(OH)2D3). Клинические проявления мутации указанного гена наблюдаются, в основном, в раннем детстве [20]. Однако у некоторых пациентов эти клинические проявления выявляются и во взрослом возрасте [21].
Ренальная гиперкальциурия характеризуется нарушением реабсорбции кальция в почечных канальцах, что приводит к повышению уровня кальция в моче и развитию вторичного гиперпаратиреоза. Уровень кальция в крови остается нормальным, так как его потеря в почках компенсируется повышением всасывания кальция в кишечнике и резорбцией костей. Основной метаболический признак ренальной гиперкальциурии – высокий уровень кальция в моче натощак при нормальном уровне кальция в крови. Повышенная экскреция кальция с мочой натощак и высокий уровень паратгормона отличают ренальную гиперкальциурию от абсорбтивной гиперкальциурии I и II типов [22]. Основной метод коррекции ренальной гиперкальциурии – назначение тиазидных диуретиков.
Резорбтивная гиперкальциурия – литогенный синдром, вызванный потерей кальция вследствие резорбции костной ткани. Наиболее часто встречается в сочетании с первичным гиперпаратиреозом. Первичный гиперпаратиреоз является причиной нефролитиаза приблизительно в 5% случаев [17]. Повышенная секреция паратгормона при аденоме паращитовидных желез приводит к усилению резорбции костей и повышению синтеза активной формы витамина D, что, в свою очередь, повышает всасывание кальция в кишечнике [23]. У большинства пациентов с первичным гиперпаратиреозом выявляют и гиперкальциемию, и гиперкальциурию. Нормальный уровень кальция в крови при высокой концентрации паратгормона в крови может иметь место, что делает диагностику более сложной. Назначение тиазидных диуретиков ("тиазидная провокация") усиливает реабсорбцию кальция в почках и обостряет гиперкальциемию, тем самым облегчая постановку диагноза. Дополнительными редкими причинами резорбтивной гиперкальциурии могут быть злокачественные новообразования, саркоидоз, тиреотоксикоз. Основной метод коррекции резорбтивной гиперкальциурии – резекция паращитовидных желез [17]. В качестве альтернативного лечения применяют аналоги витамина D и кальцимиметики.
Почечный канальцевый ацидоз. Гиперкальциурия может также встречаться и при почечном канальцевом ацидозе – клиническом синдроме, связанном с метаболическим окислением в результате нарушения секреции ионов водорода в почечных канальцах и подкислением мочи. Существует несколько его типов: 1, 2 и 4 типы [16].
Почечный канальцевый ацидоз 1 типа (дистальный) имеет особое значение для клинической урологии, не только потому, что это наиболее частая его форма, но и потому, что это метаболическое нарушение, по некоторым данным, наиболее часто встречается у пациентов с МКБ [16].
Кислотно-щелочной баланс поддерживается почками при помощи нескольких механизмов, включающих в себя как проксимальные, так и дистальные нефроны. Так как бикарбонат свободно фильтруется клубочками, почкам необходимо реабсорбировать почти весь фильтруемый бикарбонат (приблизительно 4500 ммоль), для того, чтобы поддерживать буферную емкость [24]. Более того, почки должны экскретировать избыток кислоты, которая образуется после распада углеводов, жиров и белков. Клетки почечных канальцев теряют способность как реабсорбировать бикарбонаты из ламинарного просвета, так и экскретировать в мочу ионы H+, что ведет к метаболическому ацидозу. Реабсорбция кальция в канальцах уменьшается, что приводит к развитию гиперкальциурии, а также к повышению щелочности мочи и снижению концентрации цитрата. Основным методом коррекции почечного канальцевого ацидоза является применение тиазидных диуретиков и цитратных смесей.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА ГИПЕРКАЛЬЦИУРИИ
В клинической практике важно четко дифференцировать типы гиперкальциурии, поскольку от этого зависит выбор адекватного противорецидивного лечения. Для дифференциальной диагностики вида гиперкальциурии применяются описанные выше специальные тесты (табл. 1). Характерные изменения лабораторных показателей, позволяющие диагностировать основные типы гиперкальциурии, приведены в табл. 2 и 3. [17].
Таблица 3. Дифференциальная диагностика гиперкальциурии
| Моча (сбор в течение 24 час) | ||
|---|---|---|
| Экскреция кальция после низкокальциевой диеты |
Кальций (мг) / креатинин (г) отношение натощак (норма = < 0.11) |
|
| Абсорбтивная гиперкальциурия I тип |
>6,2 мМ/сут – жен. >7,5 мМ/сут – муж. |
= < 0,11 |
| Абсорбтивная гиперкальциурия II тип |
2,5-6,2 мМ/сут – жен. 2,5-7,5 мМ/сут – муж. |
= < 0,11 |
| Абсорбтивная гиперкальциурия III тип |
>6,2 мМ/сут – жен. >7,5 мМ/сут – муж |
>0,11 |
| Ренальная гиперкальциурия |
>6,2 мМ/сут – жен. >7,5 мМ/сут – муж. |
>0,11 |
| Резорбтивная гиперкальциурия |
>6,2 мМ/сут – жен. >7,5 мМ/сут – муж. |
>0,11 |
Экскреция кальция натощак будет одинаково высокой, как у пациентов с I, так и со II типом абсорбтивной гиперкальциурии. Основным отличием является то, что у пациентов с нарушением I типа будет сохраняться повышенная экскреция кальция с мочой даже после назначения низкокальциевой диеты. Если на фоне соблюдения низкокальциевой диеты отмечена нормализация уровня кальция в моче, то это является характерным признаком наличия у пациента абсорбтивной гиперкальциурии II типа и дальнейшие диагностические тесты не требуются [17].
Стоит обратить внимание и на отношение экскреции кальция к экскреции креатинина. При абсорбтивной гиперкальциурии I и II типов натощак отношение кальций (мг)/ креатинин (г) будет нормальным (< 0,11), в отличие от абсорбтивной гиперкальциурии 3 типа (табл. 3). Если после низкокальциевой диеты сохраняется высокий уровень кальция в моче, целесообразно использовать пробу с применением пшеничных отрубей. В случае нормализации кальциурии – наиболее вероятен диагноз абсорбтивной гиперкальциурии I типа.
Представленный нами алгоритм (рис. 2) поможет практикующим врачам стандартизировать дифференциальную диагностику различных типов гиперкальциурии с целью назначения больным МКБ адекватного противорецидивного лечения.
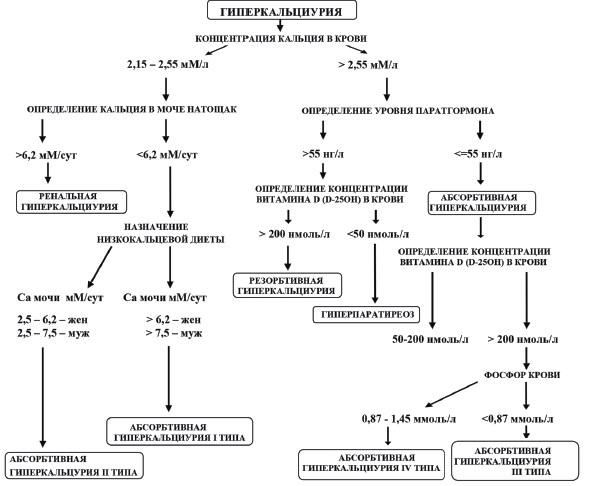
Рис. 2. Алгоритм дифференциальной диагностики типов гиперкальциурии
ПРИНЦИПЫ ЛЕЧЕНИЯ
Пациентам, у которых хотя бы раз в жизни были диагностированы камни мочевыделительной системы, должна проводиться метафилактика МКБ, как особая система противорецидивного лечения и мониторинга. В большей степени это актуально для пациентов, страдающих хронической почечной недостаточностью, пациентов с единственной почкой, для больных двусторонними и/или коралловидными камнями. При этом, эффективность терапии зависит от возможностей и способностей врача выявить причину повышенной экскреции кальция с мочой.
В случае умеренной абсорбтивной гиперкальциурии достаточно ограничиться низкокальциевой диетой.
Основным методом коррекции абсорбтивной гиперкальциурии II типа является изменение характера питания: ограничение продуктов, содержащих кальций, таких как молочные продукты (молоко, кефир, йогурты, сыры, брынза, творог, сметана), миндаль, фисташки, горчица, фасоль, грецкие орехи, овсянка. Однако следует подчеркнуть, что даже при выявленной гиперкальциурии нельзя ограничивать потребление кальция ниже 800 мг/сут. При дефиците кальция в организме и вызванной этим гипокальциемии, развиваются необратимые изменения костной ткани, повышается риск развития остеопороза, могут возникать судороги мышц, а в тяжелых случаях – конвульсии [25, 26].
В случае тяжелых или стойких типов абсорбтивной гиперкальциурии к диете необходимо добавить лекарственную терапию: тиазидные диуретики (индапамид 2,5 мг/сут); цитратные смеси; ортофосфаты [27].
Важными рекомендациями при всех типах гиперкальциурии – является увеличение диуреза, примерно до 2л в сутки, антимикробная санация мочевых путей, проведенная под контролем бактериального посева мочи, нормализация pH мочи. Основные принципы коррекции метаболических нарушений при гиперкальциурии различного типа представлены в таблице 4.
Таблица 4. Лечение гиперкальциурии
| Тип гиперкальциурии | Лечение |
| АГ I тип | Тиазидные диуретики: индапамид 2,5 мг/сут, гидрохлоротиазид 25 мг/сут (макс. 50 мг/сут), ортофосфаты. |
| АГ II тип | Низкокальциевая диета |
| АГ III тип |
Ортофосфаты: натрия фосфат (Дипиридамол) |
| Ренальная гиперкальциурия | Тиазидные диуретики |
| Резорбтивная гиперкальциурия | Резекция паращитовидных желез (для пациентов с гиперпаратиреозом). Парикальцитол – аналог витамина D. Кальцимиметики: цинакальцет |
| Почечный канальцевый ацидоз I типа | Тиазидные диуретики. Цитратные смеси. |
В случае если пациент отказывается от проведения метафилактики МКБ, его следует предупредить о возможности повторного камнеобразования. При согласии на проведение метафилактики МКБ, после определения типа метаболических литогенных нарушений и назначения лечения, следует проводить профилактический осмотр 1 раз в 3 месяца в течение первого года заболевания, далее 1 раз в год. С целью контроля уровня кальция и других веществ повторяют биохимические анализы крови и мочи. Точная диагностика метаболического типа гиперкальциурии позволяет существенно повысить эффективность противорецидивного лечения МКБ.
ЗАКЛЮЧЕНИЕ
Таким образом, гиперкальциурия – наиболее частое нарушение обмена веществ, выявляемое у больных МКБ. Нарушение многогранно и требует особого подхода к дифференциальной диагностике конкретного типа гиперкальциурии, от чего непосредственно зависит эффективность метафилактики МКБ. Предлагаемый алгоритм позволяет стандартизировать выявление различных типов гиперкальциурии с целью назначения больным МКБ адекватного противорецидивного лечения.
ЛИТЕРАТУРА
- Hongshi Xu, Zisman AL, Coe FL, Worcester EM. Kidney stones: an update on current pharmacological management and future directions. //Expert Opin Pharmacother. 2013. Vol. 14, N 4. P. 435-447.
- Каприн А.Д., Аполихин О.И., Сивков А.В., Москалева Н.Г., Солнцева Т.В., Комарова В.А. Анализ уронефрологической заболеваемости и смертности в Российской Федерации за 2003-2013 гг. // Экспериментальная и клиническая урология. 2015. N 2. С. 3-7.
- Romero V, Akpinar H, Assimis D. Kidney stones: A global picture of prevalence, incidence, and associated risk factors. // Rev Urol. 2010. Vol. 12, N 2-3. P. e86-e96.
- Taylor EN, Stampfer MJ, Curhan GC. Obesity, weight gain, and the risk of kidney stones. // JAMA. 2005. Vol. 293, N 4. P. 455-462.
- Giraudon A, Richard E, Gordon A, Bouty A, Dobremez E, Barat P, Blouin JM, Llanas B, Harambat J. Clinical and biochemical characterization of childhood urolithiasis. // Arch Pediatr. 2014. Vol. 21, N 12. P. 1322-1329.
- Trinchieri A. Epidemiology of urolithiasis. // Arch Ital Utol Androl. 1996. Vol. 68, N 4. P. 203-429.
- Ahmad I, Pansota MS, Tariq M, Tabassum SA. Frequency of metabolic abnormalities in urinary stones patients. // Pak J Med Sci. 2013. Vol. 29, N 6. P. 1363-1366
- Johnson CM, Wilson DM, O’Fallon WM. Renal stone epidemiology: a 25-year study in Rochester, Minnesota. // Kidney Int. 1979. Vol. 16, N 5. P. 624-631.
- Голованов С.А., Сивков А.В., Дзеранов Н.К., Яненко Э.К., Дрожжева В.В. Распространенность метаболических типов мочекаменной болезни в московском регионе: исследование II «Сравнительный анализ за период с 2005 по 2009 гг. // Экспериментальная и клиническая урология. 2011. N1. C. 34-38.
- Castiglione V, Jouret F, Bruyère O, Dubois B, Thomas A, Waltregny D, Bekaert AC, Cavalier É, Gadisseur R. Epidemiology of urolithiasis in Belgium on the basis of a morpho-constitutional classification. // Nephrol Ther. 2015. Vol. 11, N 1. P. 42-49.
- Prezioso D, Illiano E, Piccinocchi G, Cricelli C, Piccinocchi R, Saita A, Micheli C, Trinchieri A. Urolithiasis in Italy: an epidemiological study. // Arch Ital Urol Androl. 2014. Vol. 86, N 2. P. 99-102.
- Авдошин В.П., Андрюхин М.И., Исрафилов М.Н. Комплексное лечение и метафилактика уратного и смешанного уролитиаза. М., 2012. 32 с.
- Sutherland JW, Parks JH, Coe FL. Reccurence after a single renal stone in a community practice. // Miner Electrolyte Metab. 1985. Vol. 11, N 4. P. 267-269.
- Kim MJ, Mayr M.. Rezidivierende nephrolithiasis – wie weiter? // PRAXIS. 2013. Vol.102, N 19. P. 1177-1188.
- Pak CY, Sakhaee K, Moe OW, Poindexter J, Adams-Huet B, Pearle MS, Zerwekh JE, Preminger GM, Wills MR, Breslau NA, Bartter FC, Brater DC, Heller HJ, Odvina CV, Wabner CL, Fordtran JS, Oh M, Garg A, Harvey JA, Alpern RJ, Snyder WH, Peters PC. Defining hypercalciuria in nephrolitiasis. //Kidney Int. 2011. Vol. 80, N 7. P. 777-782
- Pearle MS, Lotan Y. Urinary lithiasis: etiology, epidemiology and pathogenesis. // In CampbellWalsh Urology, ninth edition [ed. Alan J. Wein]. Philadelphia, PA, 2007. Vol. 2. P. 1363-1392.
- Leslie SW, Batuman V, Fathallah-Shaykh S, Frederick J Kaskel FJ, Langman CB, Neiberger R, Pena D, Talavera F, Terris MK, Troischt TS, Windle ML. Hypercalciuria. Practice Essentials. 2006. //URL: http://emedicine.medscape.com/article/2182757-overview.
- Dasgupta D, Wee MJ, Reyes M, Li Y, Simm PJ, Sharma A, Schlingmann KP, Janner M, Biggin A, Lazier J, Gessner M. Mutations in SLC34A3/NPT2c are associated with kidney stones and nephrocalcinosis. // J Am Soc Nephrol. 2014. Vol. 25, N 10. P. 2366-2375
- Yu Y, Sanderson SR, Reyes M, Sharma A, Dunban N, Srivastava T, Juppner H, Bergwitz C. Novel NaPi-IIc mutations causing HHRH and idiopatic hypercalciuria in several unrelated families; long-term follow-up in one kindred. // Bone. 2012. Vol. 50, N 5. P. 1100-1106.
- Dinor D, Beckerman P, Ganon L, Eisenstein Z, Holtzman EJ. Loss-of-function mutation of CYP24A1, the vitamin D 24-hydroxylase gene, cause long-standing hypercalciuric nephrolithiasis and nephrocalcinosis. // J Urol. 2013. Vol. 190, N 2. P. 552-557.
- Nesterova G, Malicdan MC, Yasuda K, Sakaki T, Vildoux T, Cicone C, Horst R, Huang Y, Golas G, Introne W, Huizing M, Adams D, Boerkoel CF, Collins MT, Gahl WA. 1,25(OH)2D-24 Hydroxylase (CYP24A1) deficiency as a cause of nephrolithiasis. // Clin J Am Soc Nephrol. 2013. Vol. 8, N 4. P. 649-657.
- Kok DJ, Khan SR. Calcium oxalate nethrolithiasis, a free or fixad particle disease. // Kidney Int. 1994. Vol. 46, N 3. P. 847-854.
- Vella M, Karydi M, Coraci G, Oriti R, Melloni D. Patophysiology and clinical aspects of urinary lithiasis. // Urologia Int. 2007. Vol. 79, Suppl. 1. P. 26-31.
- Pohlman T, Hruska K.A., Menon M. Renal tubular acidosis. //J Urol. 1984. Vol. № 132, N 3. C.431-436
- Craven BL, Passman C, Assimos DG. Hypercalcemic states associated with nephrolithiasis. // Rev Urol. 2008. Vol. 10, N 3. P. 218-226.
- Лукьянчиков В.С., Королевская Л.И. Гипопаратиреоз и гипокальциемический синдром. //Клиническая медицина. 2003. N 1. С.66-70.
- Türk C, Knoll T, Petrik A, Sarica K, Skolarikos A, Straub M, Seitz C. Guidelines on Urolithiasis. // URL: http://uroweb.org/wp-content/uploads/22-Urolithiasis_LR_full.pdf
Статья опубликована в журнале"Экспериментальная и клиническая урология" №4 2015, стр.86-92










Комментарии