А.Н. Нечипоренко, Е.Ч. Михальчук, Н.А. Нечипоренко
Учреждение образования «Гродненский государственный медицинский университет», 230009, ул. Горького, 80.г. Гродно, Республика Беларусь
Пролапс тазовых органов (ПТО) в виде цистоцеле и ректоцеле относится к наиболее часто встречающимся заболеваниям у женщин средней и старшей возрастной групп. Так, у 57-78% женщин в возрасте 50 лет и старше при профилактическом осмотре обнаруживается ПТО различной степени выраженности и у 25-45% пациенток с этой патологией развиваются расстройства функции тазовых органов [1-4].
Радикальным методом лечения ПТО является хирургическое вмешательство, причем в последние годы большинство специалистов использует различные синтетические сетчатые импланты [5-8].
Использование синтетических сетчатых имплантов для коррекции ПТО связано с тем, что с одной стороны в отдаленные сроки после операций, корригировавших ПТО традиционными методами с использованием местных тканей, примерно у 35-40% оперированных женщин развивается рецидив [9]; а с другой – уточнен патогенез ПТО, в основе которого лежит несостоятельность соединительнотканных структур тазового дна (фасций и связок), которые должны обеспечивать физиологическое положение органов малого таза и их функцию [10,11].
Метод влагалищной внебрюшинной кольпопексии синтетическими имплантами при хирургическом лечении ПТ с использованием оригинальных систем, позволяющий укрепить или заместить несостоятельные связки и фасции тазового дна, патогенетически обоснован и получил высокую оценку специалистов [12-15].
Наряду с уже известными достоинствами применения оригинальных систем синтетических имплантов для хирургического лечения ПТО (частота рецидивов после операции снизилась до 8%) отмечается и ряд их недостатков. Речь идет о возможном развитии после операций специфических осложнений, связанных именно с имплантацией синтетического материала и о высокой стоимости оригинальных систем синтетических имплантов [16].
В связи с этим разработка менее затратной технологии использования синтетических имплантов в хирургии ПТО и изучение их воздействия на окружающие в месте имплантации ткани является одной из важных задач хирургии тазового дна.
Ранее проведенным изучением в эксперименте на животных ответной реакции тканей стенки влагалища и мочевого пузыря в зоне имплантации полипропиленовых сеток показано, что во всех случаях вокруг имплантированной сетки развивается асептическое воспаление и затем фибропластическая реакция [16].
Через 2 месяца после имплантации фрагмента полипропиленовой сетки эти изменения переходят в хроническое воспаление, окружающее инородное тело, с одновременным формированием богатой коллагеновыми волокнами рубцовой ткани, образующей неофасцию – трехмерную структуру вокруг и внутри сетчатого импланта [17-19]. Таким образом, в эксперименте на животных показано, что имплантация в ткани влагалища или мочевого пузыря фрагмента полипропиленовой сетки не вызывает необратимых изменений со стороны окружающих тканей и реакции отторжения не наблюдается [19].
Вместе с тем, работ, посвященных изучению влияния полипропиленовой сетки на ткани влагалища у женщин после имплантации сетчатого импланта с целью коррекции ПТО, крайне мало.
С учетом сказанного, нами была поставлена задача, применяя гистологические и гистохимические методы исследования, изучить состояние соединительной ткани передней стенки влагалища с лобково-шеечной фасцией у женщин с цистоцеле и (или) ректоцеле и состояние тканей в области инплантации синтетического сетчатого импланта через 4-6 месяцев после влагалищной внебрюшинной кольпопексии, выполненной с целью коррекции цистоцеле или ректоцеле.
МАТЕРИАЛЫ И МЕТОДЫ
Для оценки структурно-цитохимических характеристик соединительной ткани в стенках влагалища был выполнен комплекс гистологических и гистохимических методов исследования биоптатов передней и задней стенок влагалища у 31 женщины с ПТО (цистоцеле и ректоцеле III-IV ст. по классификации POP-Q). Пациентки были оперированы методом влагалищной внебрюшинной передней или задней кольпопексии синтетическими имплантами из полипропиленовой хирургической сетки ЭСФИЛ «бело-синий» (Россия), причем иссекали участок стенки влагалища в области «ведущей точки» смещения передней или задней стенки влагалища. То есть, получали материал из зоны наибольшего опущения стенки влагалища.
11 пациенток через 4-6 месяцев после хирургической коррекции ПТО были оперированы повторно ввиду развившихся осложнений и было выполнено гистологическое исследование удаленных тканей влагалища с фрагментами импланта.
После фиксации в жидкости Карнуа кусочки стенки влагалища заключали в парафин. Затем, изготовленные на микротоме Leica RM 2125 (Германия) парафиновые срезы толщиной 5 мкм после окрашивания гематоксилином и эозином, по Маллори, по Ван-Гизону и Вейгерту, использовали для гистологических исследований и получения иллюстративного материала при различных увеличениях микроскопа Axioscop 2 plus (Zeiss, Германия), цифровой видеокамеры (Leica DFC 320, Германия) и программы анализа изображения ImageWarp (Bitflow, США).
Для гистохимических исследований срезы толщиной 10 мкм окрашивали по Шабадашу – на выявление гликопротеинов и по Спайсеру – альциановым синим при рН 1,0 и 2,5 на выявление сульфои сиаломуцинов.
Средние величины количественных признаков сравнивались с помощью параметрического метода сравнения – критерия t (Стьюдента-Фишера). Качественные показатели представлялись в виде четырехпольных таблиц сопряженности. Последующая статистическая обработка проводилась с помощью непараметрического критерия соответствия хи-квадрат. Полученные данные обрабатывались с использованием пакета прикладных программ IBM SPSS Statistica, Version 10.
РЕЗУЛЬТАТЫ
При изучении гистологических препаратов стенок влагалища больных с цистоцеле и ректоцеле III-IV ст. каких-либо специфических изменений не обнаружено. Тем не менее, у этих пациенток в некоторых участках срезов биопсийного материала в стенке влагалища обнаруживались гладкие миоциты с явлениями микровакуолизации цитоплазмы (рис. 1). Плотность расположения коллагеновых волокон в стенках влагалища была неодинаковой (рис. 2). В одних местах их количество довольно высокое (насыщенно-синий цвет), а в других сниженное (светлые участки).

Рис.1. Фрагмент передней стенки влагалища при цистоцеле III ст. Отмечается микровакуолизация цитоплазмы гладких миоцитов (стрелки). Окраска по Маллори. Увел. 200
Fig. 1. A fragment of the anterior wall of the vagina with cystocele III st. Microvacuolization of the cytoplasm of smooth myocytes (arrows) is noted. Mallory stain. 200 x magnification
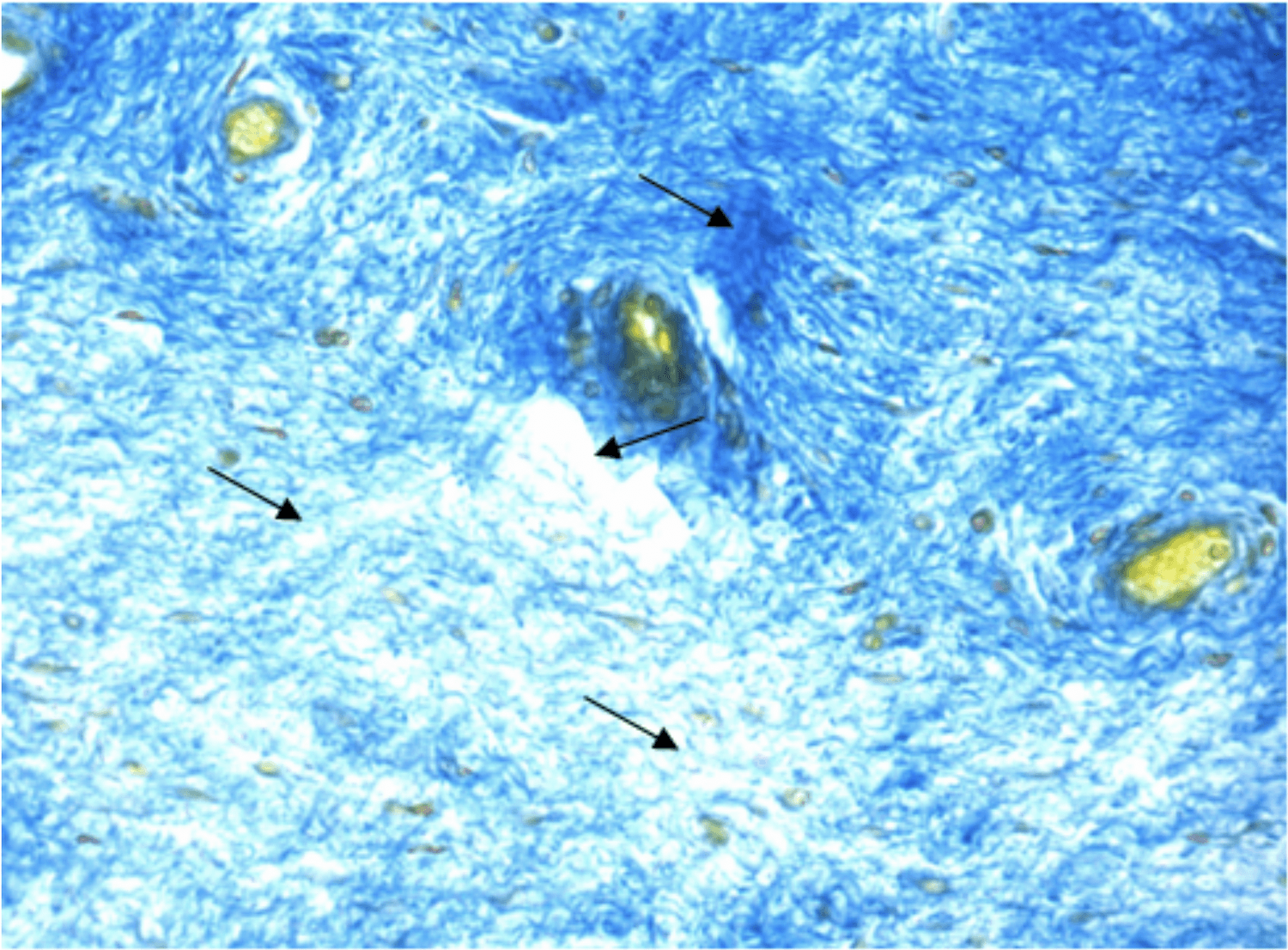
Рис. 2. Фрагмент передней стенки влагалища пациентки с цистоцеле III ст. Неодинаковая плотность коллагеновых волокон в стенке влагалища (показано стрелками). Окраска по Маллори. Увеличение 100.
Fig. 2. A fragment of the anterior wall of the vagina of the patient with cystocele III st. The uneven density of collagen fibers in the vaginal wall (shown by arrows). Mallory stain. 100 x magnification
В препаратах наблюдались участки, где пучки коллагеновых волокон подверглись разволокнению (распад коллагена на отдельные волоконца). В этих местах при окрашивании по Шабадашу наблюдаются более бледные зоны окраски основного вещества (рис. 3). Также наблюдались инфильтраты лимфоидных клеток. Сочетание разволокненных участков коллагеновых волокон и выраженной лимфоцитарной инфильтрации свидетельствует о процессах декомпенсации тканей влагалища за время прогрессирования пролапса.
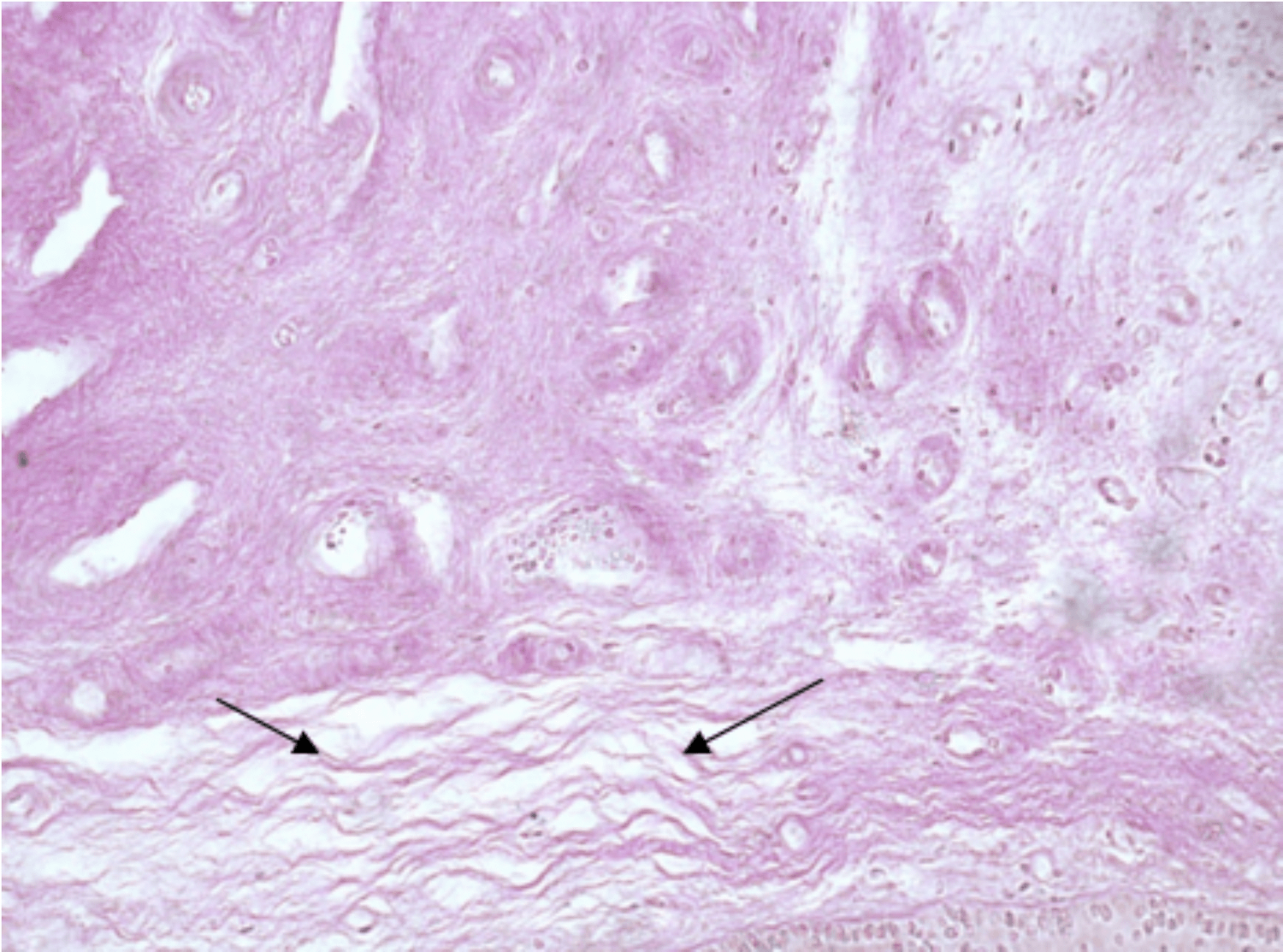
Рис. 3. Разволокнение пучка коллагеновых волокон в слизистой оболочке стенки влагалища (стрелки). Окраска по Шабадашу. Увеличение 200
Fig. 3. Depletion of a bundle of collagen fibers in the mucous membrane of the vaginal wall (arrows). Shabadash coloring. 200 х magnification
Таким образом, гистологические исследования стенок влагалища позволили подтвердить несостоятельность соединительной ткани стенок влагалища у женщин с пролапсом тазовых органов.
У 11 женщин в силу развития имплант-ассоциированных осложнений в виде смещения или сморщивания импланта через 4-6 месяцев после влагалищной внебрюшинной кольпопексии имплант или его часть удаляли.
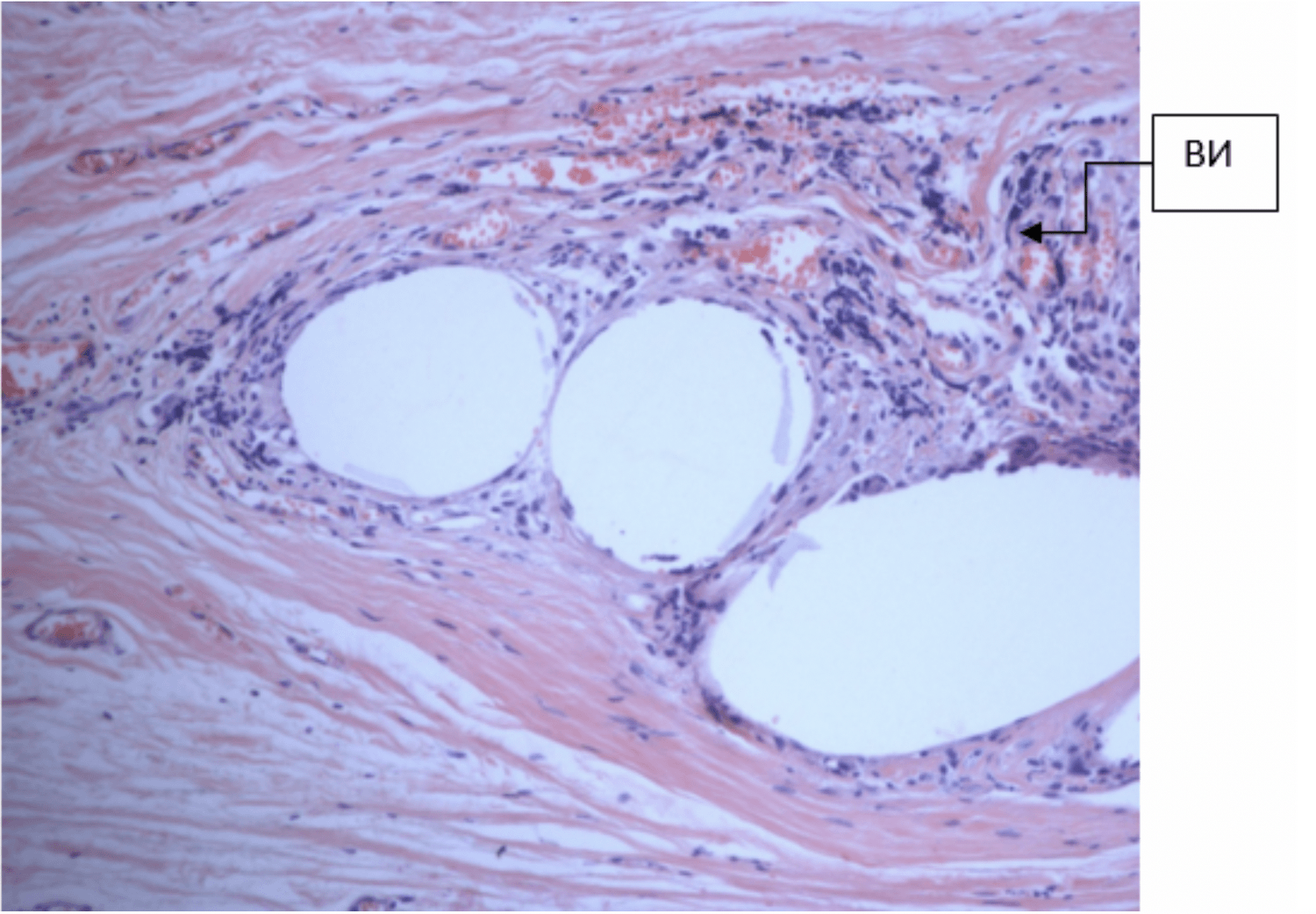
Рис. 4. Микропрепарат удаленного сетчатого импланта через 4 месяца после операции. Воспалительная инфильтрация (ВИ) вокруг волокон сетчатого импланта. Формирование коллагеновых волокон вокруг нитей импланта. Окраска гематоксилином и эозином. Увеличение 200
Fig. 4. The micropreparation of the removed mesh implant 4 months after surgery. Inflammatory infiltration (ВИ) around the fibers of the mesh implant. The formation of collagen fibers around the implant threads. Hematoxylin and eosin stain. 200 х magnification
При гистологическом исследовании фрагментов удаленных сетчатых имплантов через 4 месяца после операции, отметили развитие соединительной ткани между и вокруг волокон сетчатых имплантов и очаги воспалительной инфильтрации (рис. 4,5).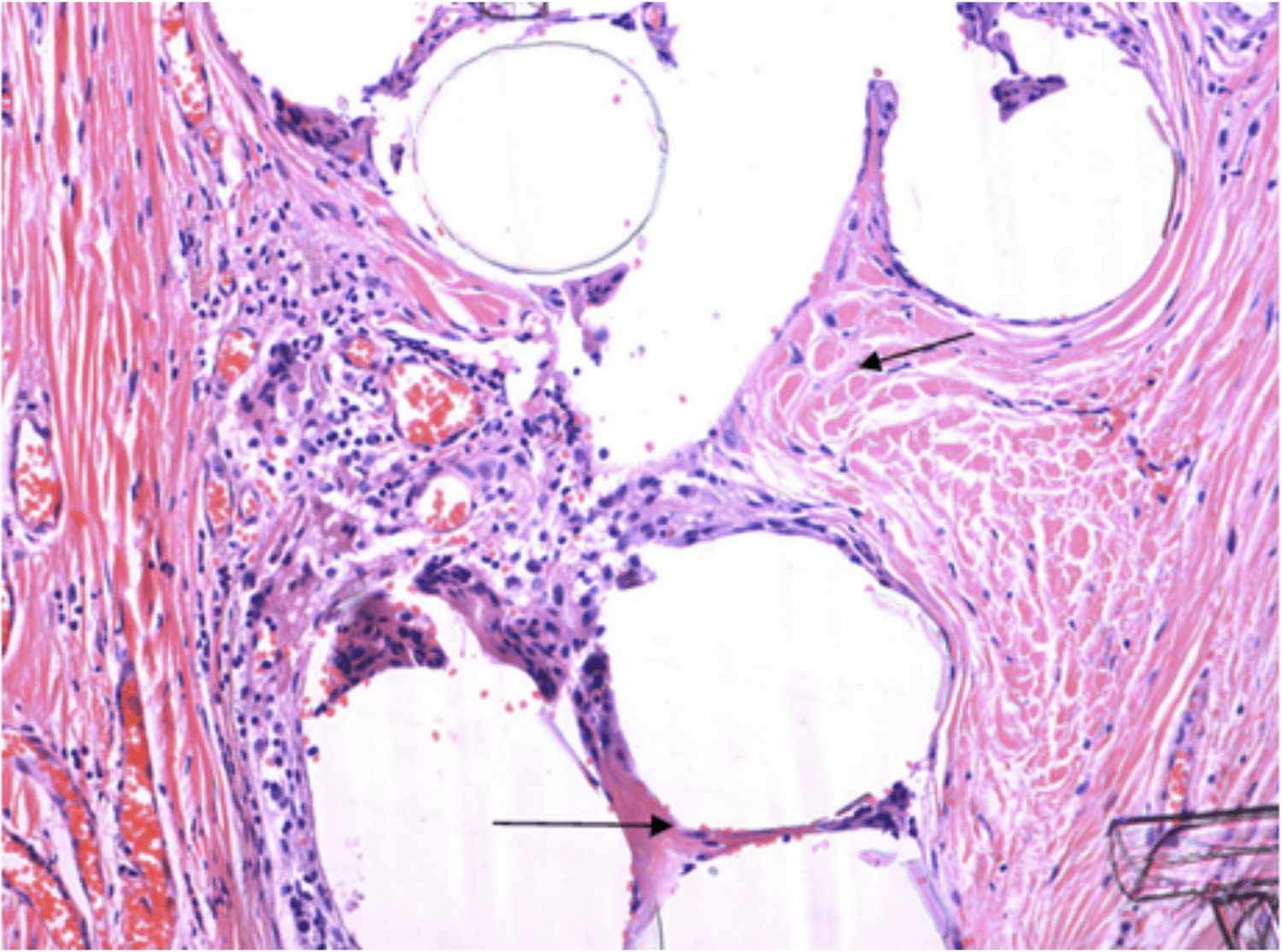
Рис. 5. Микропрепарат фрагмента удаленного сетчатого импланта. Образование соединительной ткани (стрелки) с капиллярами между волокнами синтетического импланта через 4 месяца после операции. Окраска гематоксилином и эозином. Увеличение 200
Fig. 5. Micropreparation of a fragment of a removed mesh implant. The formation of connective tissue (arrows) with capillaries between the fibers of a synthetic implant 4 months after surgery. Hematoxylin and eosin stain. 200 x magnification
На более поздних сроках после имплантации импланта (6 месяцев) количество вновь образованных коллагеновых волокон между волокнами сетчатого импланта увеличивается. Кроме того, в сформировавшейся соединительной ткани между волокнами сетчатого импланта отмечается большое количество кровеносных капилляров, заполненных эритроцитами (рис. 6, 7,8).
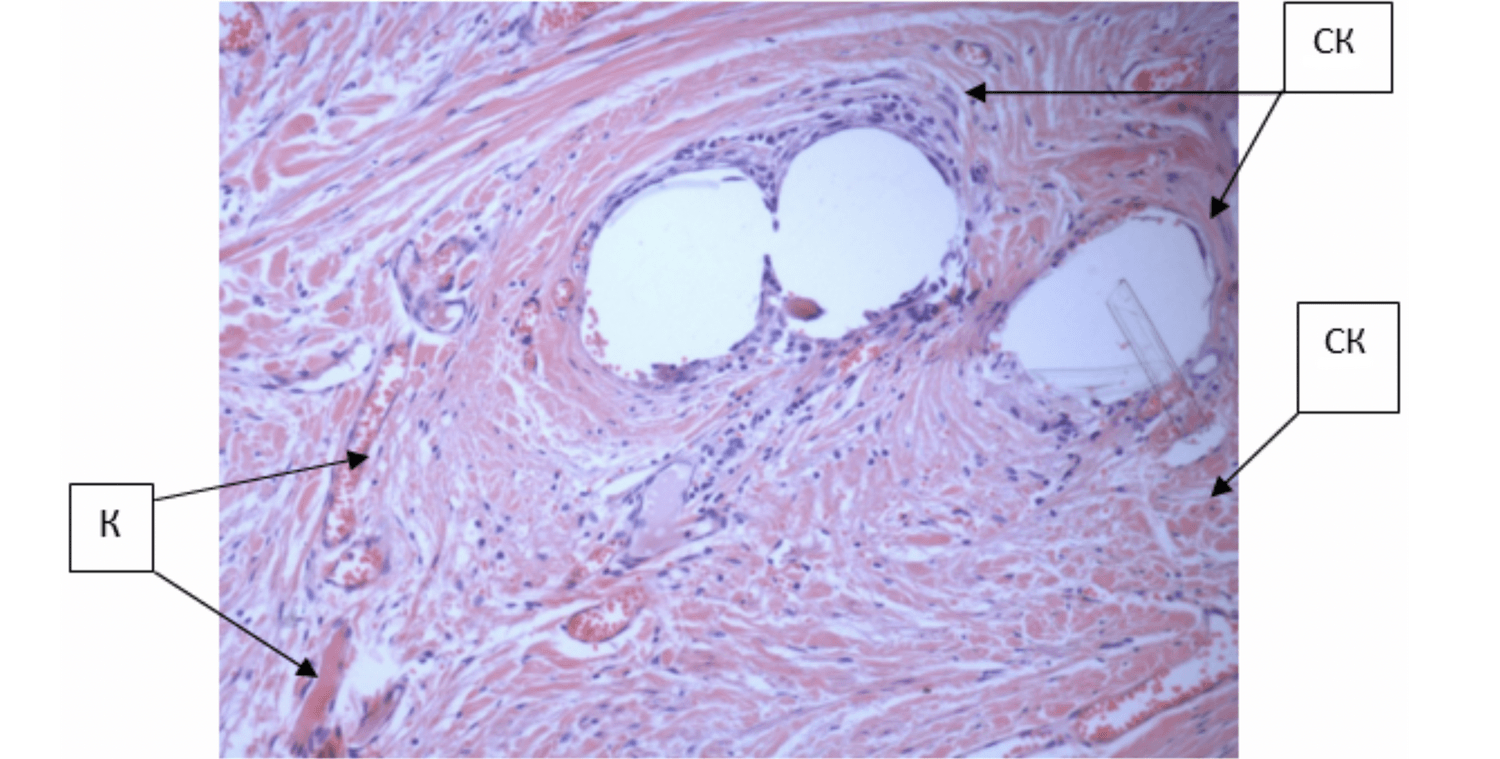
Рис. 6. Формирование общего соединительно-тканного каркаса (СК) между и вокруг волокон имплантированного сетчатого импланта. Капилляры, заполненные эритроцитами (К) (через 6 месяцев после операции). Окраска гематоксилином и эозином. Увеличение 100
Fig. 6. Formation of a common connective tissue framework (CK) between and around the fibers of the implanted mesh implant. Red blood cell-filled capillaries (K) (6 months after surgery). Hematoxylin and eosin stain. Magnification 100
Таким образом, формирование вокруг и между нитями сетчатого импланта коллагеновых волокон приводит к образованию неофасции, состоящей из полипропиленовой сетки, ячейки которой заполнены хорошо васкуляризированной зрелой соединительной тканью.
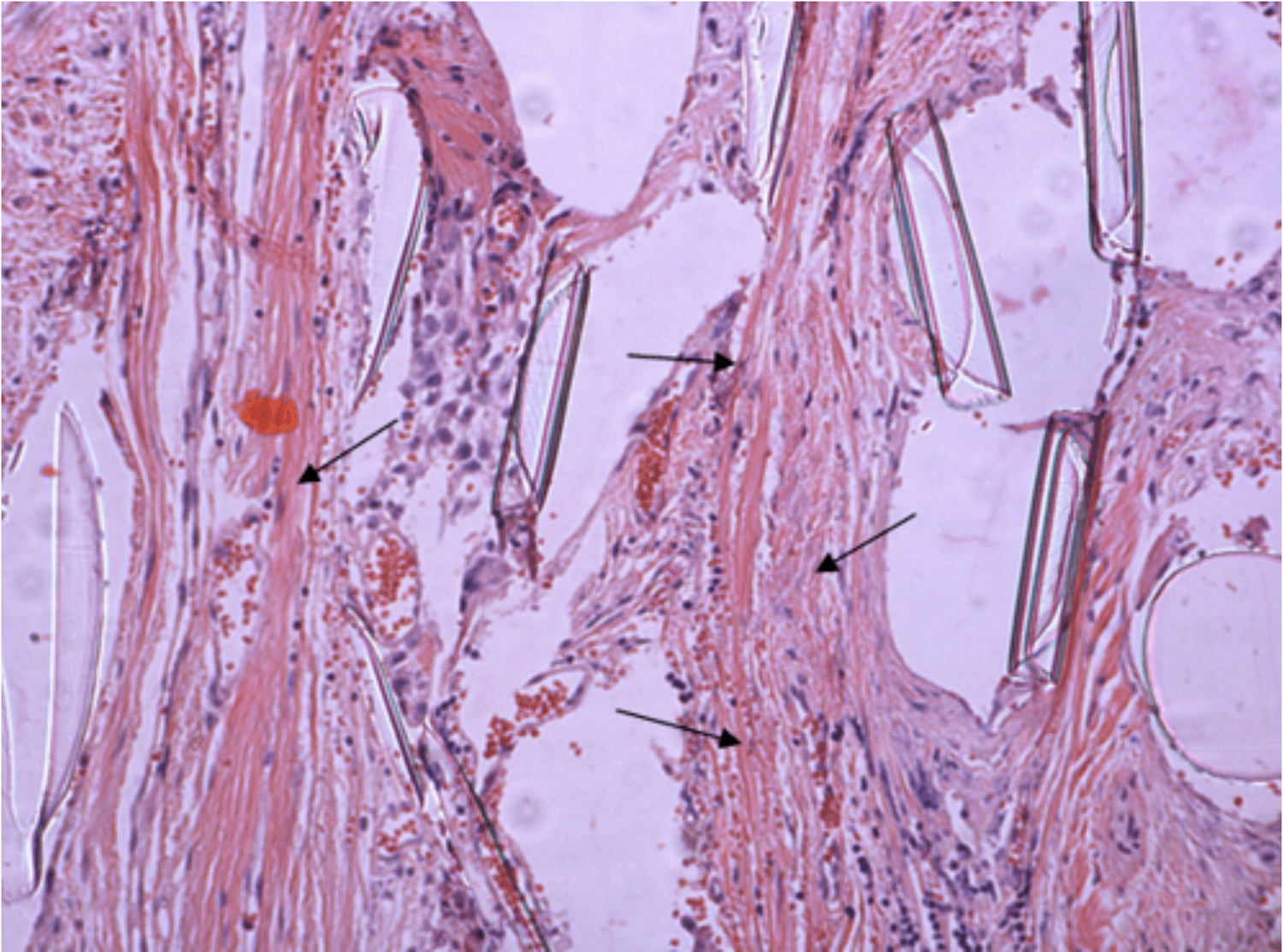
Рис. 7. Микропрепарат фрагмента удаленного сетчатого импланта. Коллагеновые волокна (стрелки) между нитями импланта через 5 месяцев после имплантации протеза в паравагинальное пространство. Окраска гематоксилином и эозином. Увеличение 400
Fig. 7. Microdrug of a fragment of a removed mesh implant. Collagen fibers (arrows) between the threads of the implant 5 months after implantation of the implant into the paravaginal space. Hematoxylin and eosin stain. 400 x magnification
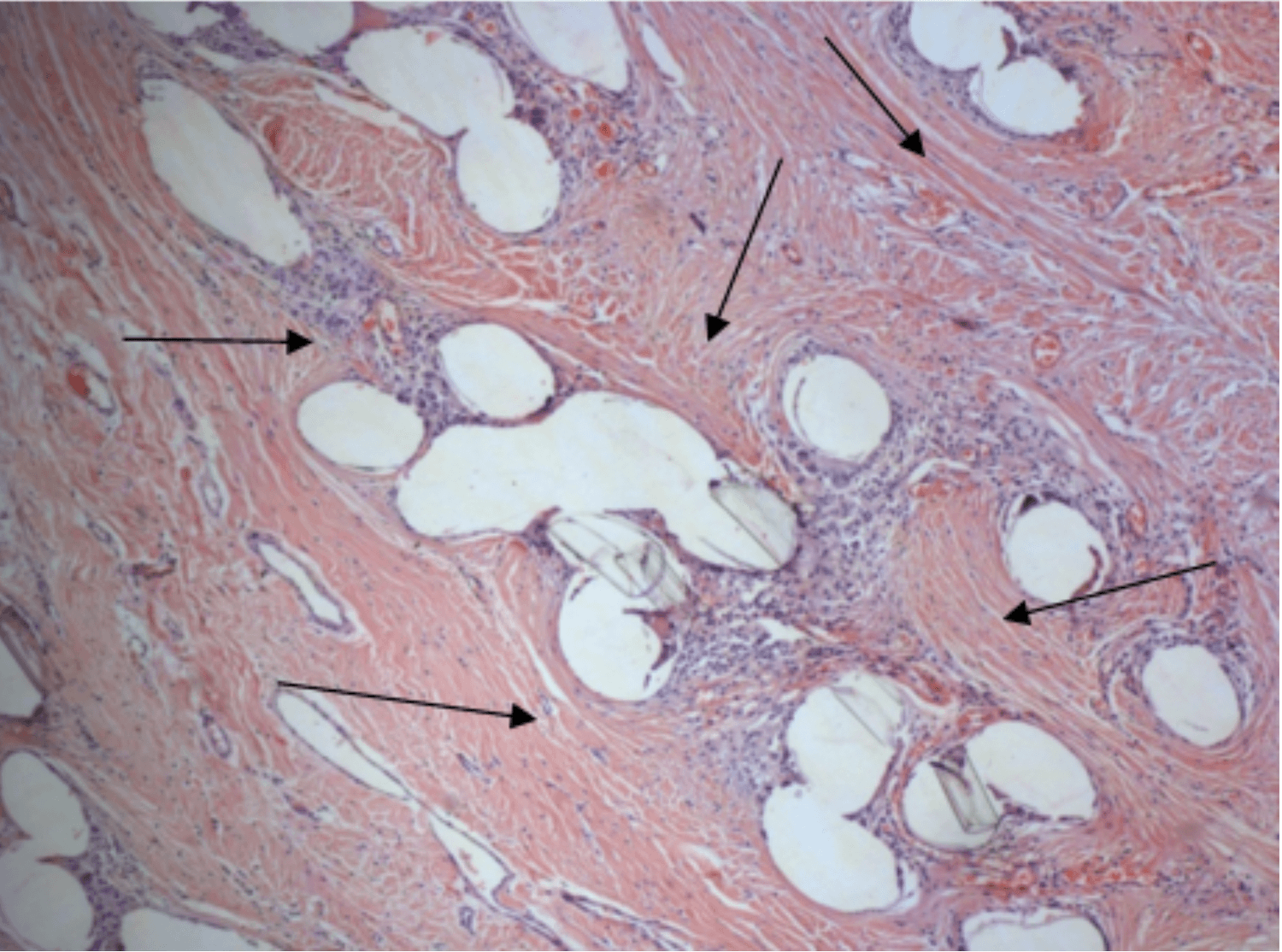
Рис. 8. Гистологический препарат фрагмента сетчатого импланта из хирургической сетки ЭСФИЛ через 6 месяцев после передней кольпопексии у пациентки с цистоцеле IV ст. Пучки вновь образованных коллагеновых волокон (показаны стрелками) заполняют пространства между нитями сетки. Окраска гематоксилином и эозином. Увеличение 40
Fig. 8. Histological preparation of a fragment of a mesh implant from the surgical mesh of ESFIL 6 months after anterior colpopexy in a patient with cystocele IV st. Bundles of newly formed collagen fibers (shown by arrows) fill the spaces between the filaments of the grid. Hematoxylin and eosin stain. Magnification x 40
ОБСУЖДЕНИЕ
Выявленные морфологические изменения в структуре коллагеновых волокон соединительной ткани стенок влагалища позволяют сделать вывод о том, что стенки влагалища у женщин с ПТО III-IV ст. подвергаются значительному механическому воздействию за счет их растяжения опускающимися органами малого таза. Это приводит к гипоксии тканей стенок влагалища, что в сочетании с механическим растяжением вызывает качественные изменения коллагена и это еще больше уменьшает биомеханическую прочность стенок влагалища, связок и фасций тазового дна. В подобном состоянии соединительной ткани стенок влагалища хирургическая коррекция ПТО с использованием местных тканей (кольпоперинеолеваторопластика) не позволяют рассчитывать на продолжительный анатомический эффект поскольку вмешательство выполняется на заведомо несостоятельных тканях. Отсюда понятна и причина частого развития рецидивов ПТО после таких операций и обоснованность использования синтетических сетчатых имплантов с целью создания тканевых структур, которые восстановят анатомическое положение органов малого таза.
Гистологические исследования удаленных фрагментов полипропиленовых сетчатых имплантов из хирургической сетки ЭСФИЛ (вариант легкий), имплантированных для коррекции ПТО, показывают, что окружающие имплант ткани реагируют развитием асептического воспаления с формированием зрелой соединительной ткани за счет активного коллагенообразования. Эти результаты согласуются с данными, приведенными в литературе [16,19]. Сетчатый имплант, находящийся в паравагинальных тканях, создает основу для формирования новой прочной неофасции. Между волокнами импланта развивается зрелая соединительная ткань с хорошей васкуляризацией. Наличие такой неофасции, состоящей из синтетической сетки и новообразованной соединительной ткани создает надежную опору для органов малого таза, что и обеспечивает их физиологическое положение.
ВЫВОДЫ
- У женщин с ПТО имеются изменения не только в структуре коллагеновых волокон, но и в химическом составе основного вещества в стенках влагалища в виде неодинакового содержания гликопротеинов, сульфомуцинов и сиаломуцинов, что может быть причиной ослабления биомеханической прочности соединительной ткани;
- Плотность расположения коллагеновых волокон в стенках влагалища при ПТО неодинаковая, в одних местах их количество высокое, в других сниженное, отмечаются очаги разволокнения коллагеновых волокон и выраженной лимфоцитарной инфильтрации, что свидетельствует о процессах декомпенсации соединительной ткани стенок влагалища за время прогрессирования пролапса;
- Имплантированный в паравагинальное пространство синтетический полипропиленовый имплант из хирургической сетки ЭСФИЛ (Россия) не вызывает в окружающих тканях необратимых изменений и не отторгается. Имплант позволяет сформироваться мощной неофасции, создающей прочную опору для органов малого таза, обеспечивающую им физиологическое положение.
ЛИТЕРАТУРА
- Лоран О.Б., Серегин А.В., Довлатов З.А. Результаты применения современных малоинвазивных технологий в лечении пролапса тазовых органов у женщин. Экспериментальная и клиническая урология 2015;1:124-130. [Loran O.B., Seregin A.V., Dovlatov Z.A. The clinical outcomes of the modern minimally invasive tech nologies in the treatment of the female pelvic organ prolaps. Eksperimentalnaya i klinicheskaya urologiya = Experimental and clinical urology 2015;2:124-130. (In Russian)].
- Ismail SI, Bain C, Hagen S. Oestrogens for treatment or prevention of pelvic organ prolapse in postmenopausal women. Cochrane Database Syst. Rev 2010. Sep 8;(9). doi: 10.1002/14651858.CD007063.pub2.
- Радзинский В.Е. Перинеология. М.: "МИА", 2006 г. 336 с. [Radzinskiy V.E. Perineologiya. M.: "MIA", 2006 g. 336 p. (In Russian)].
- Фоменко О.Ю., Шелыгин Ю.А., Попов А.А., Порядин Г.В., Титов А.Ю., Берсенева Е.А. и др. Функциональное состояние мышц тазового дна у больных с ректоцеле. Российский вестник акушерагинеколога 2017;17(3):43-48). [Fomenko O.Yu., Shelyigin Yu.A., Popov A.A., Poryadin G.V., Titov A.Yu., Berseneva E.A. et al. The functional state of the pelvic floor muscles in patients with rectocele. Rossiyskiy vestnik akushera-ginekologa = Russian Bulletin of the Obstetrician-Gynecologist 2017;17(3):43-48). (In Russian)].
- Cosson М., Caquant F, Collinet P, Rosenthal C, Clave H, Debodinance P. et al. Prolift mesh (Gynecare) for pelvic organ prolapsed surgical treatment using the TVM group technique: A retrospective study of 687 patients. International Continence Society Meeting Abstracts. Montreal 2005:121–122.
- Davila GW, Beyer R, Moore R, Del Rio S, Lukban J et al. Restoration of vaginal apical and posterior wall support with the apogee system. International Continence Society Meeting Abstracts. Montreal 2005:597 – 598.
- Moore R., Miklos J. Cystocele repair utilizing anterior wall mesh graft placed via double trans-obturator approach (Perigee system). International Continence Society Meeting Abstracts. Montreal 2005:595.
- Шкарупа Д.Д., Горгоцкий И.А., Ярова Н.П., Шкарупа Е.А.Проспективное исследование эффективности хирургической реконструкции тазового дна с применением сверхлегких сетчатых эндопротезов "Пелвикс". Экспериментальная и клиническая урология 2012;3:90-96. [Shkarupa D.D., Gorgotskiy I.A., Yarova N.P., Shkarupa E.A. Prospective evaluation of pelvic floor repair effectiveness with super-light mesh “Pelvix". Eksperimentalnaya i klinicheskaya urologiya = Experimental and clinical urology 2012;3:90-96. (In Russian)].
- Han L, Wang L, Wang Q. Association between pelvic organ prolapse and stress urinary incontinence with collagen. Exp TherMed 2014;7(5):1337–1341. doi: 10.3892/etm.2014.1563.
- Петрос П. Женское тазовое дно (Функция, дисфункция и их лечение в соответствии с интегральной теорией). МЕДпресс-информ 2017 г. 400 с. [Petros P. Female pelvic floor (Function, dysfunction and their treatment in accordance with the integral theory). MEDpress-inform 2017 g. 400 p. (In Russian)].
- Goeschen K, Petros PP. Der weibliche Beckenboden Funktionelle Anatomie, Diagnostik und Therapie nach der Integralteorie. Heidelberg: Springer Medicin Verlag 2009:278.
- Беженарь В.Ф., Айламазян Э.К., Богатырева Е.В. Эффективность применения Prolift при хирургическом лечении пролапса тазовых органов. Московский хирургический журнал 2009;8(4):5-15. [Bezhenar V.F., Aylamazyan E.K., Bogatyireva E.V. The effectiveness of the Prolift™ system in pelvic organs prolapse surgery. Moskovskiy hirurgicheskiy zhurnal = Moscow Surgical Journal 2009;8(4):5-15. (In Russian)].
- Беженарь В.Ф., Богатырева Е.В., Цыпурдеева А.А., Цуладзе Л.К., Русина Е.И., Гусева Е.С. Новые возможности хирургической коррекции тазового пролапса с использованием синтетических имплантов: пути профилактики послеоперационых осложнений. Акушерство, гинекология и репродукция 2012;6(2):6-13. [Bezhenar V.F., Bogatyireva E.V., Tsyipurdeeva A.A., Tsuladze L.K., Rusina E.I., Guseva E.S. New possibilities of surgical correction of pop with use of synthetic implants: ways of preventive postoperative complications. Akusherstvo, ginekologiya i reproduktsiya = Obstetrics, gynecology and reproduction 2012;6(2):6-13. (In Russian)].
- Солуянов М.Ю., Любарский М.С., Королева Е.Г., Ракитин Ф.А. Ошибки и осложнения хирургического лечения пролапса тазовых органов с использованием синтетических материалов. Успехи современного естествознания 2012;10:48-52. [Soluyanov M.Yu., Lyubarskiy M.S., Koroleva E.G., Rakitin F.A. Errors and surgery complications pelvic organ prolapsewith use of synthetic materials. Uspehi sovremennogo estestvoznaniya = The successes of modern natural science 2012;10:48-52. (In Russian)].
- Шкарупа Д.Д., Кубин Н.Д. Протезирующая реконструкция тазового дна влагалищным доступом: современный взгляд на проблему. Экспериментальная и клиническая урология 2015;1:88-93. [Shkarupa D.D., Kubin N.D. Prosthetic reconstruction of the pelvic floor using vaginal approach: contemporary view. Eksperimentalnaya i klinicheskaya urologiya = Experimental and clinical urology 2015;1:88-93. (In Russian)].
- Каприн А.Д., Филимонов В.Б., Васина И.В., Васин Р.В., Костин А.А. Морфологическая характеристика реакции тканей мочевого пузыря и влагалища на фиксацию к ним сетчатых полипропиленовых имплантатов в эксперименте. Экспериментальная и клиническая урология 2013;1:24-29. [Kaprin A.D., Filimonov V.B., Vasina I.V., Vasin R.V., Kostin A.A. Morphologic changes in urinary bladder and vagina tissues after polypropylene mesh implantation. Eksperimentalnaya i klinicheskaya urologiya = Experimental and clinical urology 2013;1:24-29. (In Russian)].
- Дубова Е.А., Щеголев А.И., Чекмарева И.А., Филатшна Н.В., Чижов Д.В., Егиев В.Н. Тканевая реакция на имплантацию облегченных полипропиленовых сеток. Бюллетень экспериментальной биологии и медицины 2006;12:687-69. [Dubova E.A., Schegolev A.I., Chekmareva I.A., Filatshna N.V., Chizhov D.V., Egiev V.N. Tissue response to the implantation of lightweight polypropylene nets. Byulleten eksperimentalnoy biologii i meditsinyi = Bulletin of Experimental Biology and Medicine 2006;12:687-69. (In Russian)].
- Klosterhalfen B, Klinge U, Hermanns B, Schumpelick V. Pathology of traditional surgical nets for hernia repair after long-term implantation in humans. Chirurg. 2000;71(1):43-51. doi: 10.1007/ s001040050007
- Papadimitriou J, Petros PEP. Histological studies of monofilament and multifilament polypropylene mesh implants demonstrate equivalent penetration of macrophages between fibrils. Hernia 2005;9:75-78. doi; 10.1007/s10029-004-0286-6
Статья опубликована в журнале "Экспериментальная и клиническая урология" №1 2020, стр. 130-135









Комментарии