Шкодкин С.В.1, Полищук А.В.2, Чирков С.В.3, Шушпанова К.Д.3
1ОГБУЗ «Белгородская областная клиническая больница Святителя Иоасафа»
2ОГБУЗ «Городская больница №2», г. Белгород
3Белгородский государственный национальный исследовательский университет
Полное или частичное сочетание таких симптомов как абдоминальное ожирение, инсулинорезистентность или сахарный диабет 2 типа, атерогенная дислипидемия, артериальная гипертония, нарушения системы гемостаза, эндотелиальная дисфункция и хроническое субклиническое системное воспаление описывается в литературе как метаболический синдром (МС) [1]. С каждым годом проблеме МС заслуженно уделяется все больше внимания, так как отмечается значительный рост пациентов, страдающих данным синдромом как в экономически развитых, так и в развивающихся странах [2,3]. Распространенность МС в средней возрастной группе (30-50 лет) в Европе составляет 19-29%, в США – до 39% [4,5,6]. К сожалению, эта тенденция актуальна и для России, что можно проследить в рамках проведенной программы «Целевая диспансеризация г. Москвы» [7].
Одной из причин развития МС является андрогенодефицит. Дефицит тестостерона наряду с гиподинамией и алиментарным фактором способствует прогрессированию МС. Следовательно, как показали ряд авторов, коррекция гипогонадизма оказывает положительное влияние на антропометрические и биохимические компоненты МС, а также на концентрацию маркеров воспаления [8].
Не менее сложной проблемой является так называемый синдром хронической тазовой боли (СХТБ). Согласно рекомендациям Европейской ассоциации урологов (EAU) 2015, СХТБ и простатический болевой синдром занимают 90% в структуре воспалительных заболеваний предстательной железы (ПЖ) [12]. В настоящее время СХТБ рассматривается как полиэтиологическая проблема патогенетические звенья которой до конца не ясны, что делает работу в этом направлении весьма актуальной. В своей работе мы попытались выявить взаимосвязи между наличием у пациентов МС и выраженностью таких урологических синдромов как СХТБ, симптомы нарушенного мочеиспускания (СНМ) и эректильной дисфункцией (ЭД).
Цель исследования: поиск корреляций метаболического синдрома с синдромом хронической тазовой боли, нарушением микции и эректильной дисфункцией.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование включены данные обследования 16 мужчин с МС в возрасте от 40 до 50 лет, в среднем 48,5±2,8 года, которые обратились на прием к эндокринологу по поводу избыточного веса и не имели установленного диагноза сахарного диабета. В сопоставимую по возрасту группу сравнения (48,6±2,4 года, р>0,05) вошли 13 мужчин без МС. В группах отмечены достоверные различия по таким антропометрическим показателям как вес, окружность талии и индекс массы тела, которые в основной группе составили 94,1±7,7 кг, 108,3±10,3 см и 30,6±1,3 кг/м2 и 77,9±6,4 кг, 87,8±4,8 см, и 24,4±0,5 кг/м2 в группе контроля, соответственно (р<0,05) (рис. 1).
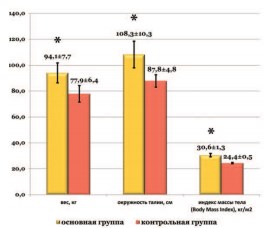
Рис.1. Данные морфометрического исследования в группах наблюдения * - имеются статистически достоверные различия (р<0,05)
Дополнительными критериями включения в исследование стали нормальный уровень простатспецифического антигена (ПСА) и отсутствие воспалительных изменений в эякуляте. Все пациенты подписали информированное согласие.
Критерии исключения: отказ пациентов от участия в исследовании, установленный диагноз «Сахарный диабет», наличие лейкоцитов в анализе мочи после массажа ПЖ, наличие патогенной микрофлоры в секрете ПЖ.
Пациентам проводилось анкетирование по опросникам AMS (Опросник симптомов старения мужчин), IPSS (Международная система суммарной оценки заболеваний ПЖ), болевая шкала LANSS (Шкала оценки невропатических симптомов и признаков), МИЭФ-5 (Международный индекс эректильной функции). Проведено объективное (физикальное) обследование: измерение массы тела, окружность талии, индекс массы тела.Лабораторная диагностика включала определение следующих показателей: тестостерон общий и свободный, глобулин связывающий половые гормоны, лютеинизирующий гормон, инсулин, глюкоза, гликозилированный гемоглобин, липидный профиль. Всем пациентам выполнена урофлоуметрия, ультразвуковое исследование (УЗИ) мочевого пузыря с определением объема остаточной мочи, трансректальное ультразвуковое исследование (ТРУЗИ) ПЖ с измерением кровотока.
Достоверность различий определяли непараметрическим критерием Манна-Уитни, статистически значимыми считали различия при вероятности больше 95% [13].
РЕЗУЛЬТАТЫ
В нашем исследовании уровень тестостерона в основной группе наблюдения составил 10,3±0,9 нмоль/л и был достоверно ниже данного показателя в контрольной группе – 16,0±1,3 нмоль/л (р<0,05, рис. 2)
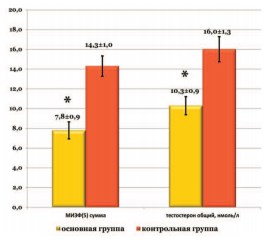
Рис.2. Индекс эректильной функции по шкале МИЭФ(5) в соотношении с уровнем общего тестостерона * - имеются статистически достоверные различия (р<0,05)
Анализ субъективной оценки выраженности ЭД в группах наблюдения на основании валидной шкалы МИЭФ-5 позволил вполне адекватно и быстро оценить степень эректильных нарушений. При этом мы получили ожидаемые результаты, согласно которым пациенты в основной группе имели достоверно более низкий суммарный балл – 7,8±0,9, по сравнению с мужчинами, не имеющими МС – 14,3±1,0 балла (р<0,05, рис. 2). Полученные результаты, указывающие на наличие гипогонадизма у пациентов основной группы наблюдения, согласуются с данными литературы, посвященными проблеме МС [11]. Это так же подтверждает гипотезу о том, что МС выступает независимым фактором гипогонадизма и ЭД [9].
При анализе анкет IPSS было выявлено, что пациенты обеих групп наблюдения имели нарушение микции. В основной группе наблюдения суммарный балл по IPSS составил 24,6±2,7 против 16,9±2,6 баллов в контрольной группе наблюдения (р0,05, рис. 3). Объем остаточной мочи у пациентов обеих групп наблюдения не превысил нормальных референтных значений и достиг в основной группе наблюдения 15,7±12,1 мл, у мужчин контрольной группы – 7,2±5,8 мл (р>0,05, рис. 3).
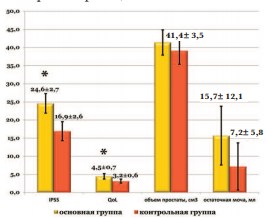
Рис.3. Корреляции между выраженностью симптомов нижних мочевых путей и данными УЗИ * - имеются статистически достоверные различия (р<0,05)
Урофлоуметрия так же не выявила признаков инфравезикальной обструкции, так при интерпретации урофлоурограмм в группах наблюдения не зарегистрировано достоверных различий по величине максимального потока мочи (р>0,05, рис. 4). Однако у пациентов с МС средняя объемная скорость мочеиспускания была ниже за счет увеличения времени мочеиспускания. Средняя объемная скорость мочеиспускания в основной группе наблюдения составила 14,8±2,7 мл/сек, тогда как в контрольной – 18,2±3,5 мл/сек (р<0,05, рис. 4). Увеличение времени мочеиспускания, выявленное в нашем исследовании у пациентов с МС, мы связываем с неоднократными повторными сокращениями детрузора, особенно в конце микции, что можно считать проявлением его гиперактивности. При этом длительность мочеиспускания в группе с МС составила 32,8±4,2 в сравнении с контрольной – 21,4±3,5 секунды (р<0,05, рис. 4).
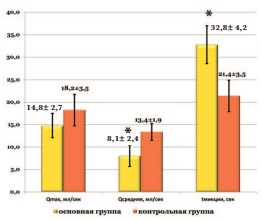
Рис.4. Показатели урофлоурограмм в группах наблюдения * - имеются статистически достоверные различия (р<0,05)
Анализ результатов анкетирования по болевой шкале LANSS показал достоверные различия в группах наблюдения, в группе с МС суммарный балл составил 17,4±0,9, в то время как в контрольной 8,2±0,4 балла (р<0,05, рис. 5). В основной группе превалировала болевая симптоматика за счет орхидалгии, простатодинии, странгурии. Детальный расспрос пациентов основной группы наблюдения установил, что хроническая боль, как проявление СХТБ, по сути выступала одним из основных факторов при обращении за медицинской помощью. В литературе имеется достаточно большое количество публикаций о зависимости СХТБ от степени развития атеросклероза и ишемии ПЖ и мочевого пузыря [10]. Для изучения этой гипотезы мы оценили кровоток в ПЖ у пациентов обеих групп наблюдения. Были получены следующие результаты: пиковая скорость кровотока Vmax в основной группе достигала 13,8±1,9мм/с, в контрольной Vmax – 14,1±1,8 мм/с (р>0,05, рис. 5). Отсутствие достоверных различий так же было продемонстрировано для индекса резистентности [Ri], который в основной группе составил 0,6±0,03, в контрольной – 0,61±0,02 (р>0,05, рис. 5). Таким образом, нами не получены корреляции между показателями магистрального кровотока в простате и наличием МС и СХТБ.
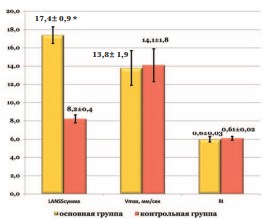
Рис.5. Выраженность синдрома хронической тазовой боли от кровотока в предстательной железе * - имеются статистически достоверные различия (р<0,05)
ОБСУЖДЕНИЕ
Анализируя данные о распространенности МС можно судить о значительном его увеличении в популяции, что расценивается как негативный фактор не только для конкретного человека, но и для социума в целом. Имеющиеся в настоящее время публикации по проведенным ранее исследованиям, посвященным МС, не позволяют получить единое мнение о его влиянии на течение многих патологических процессов. Наряду с подтверждающими результатами есть и опровергающие. Ориентируясь на собственные и литературные данные, мы считаем доказанным факт гипогонадизма и связанные с этим нарушения эрекции у пациентов с МС. Полученные нами факты о преобладании ирритативной симптоматики у пациентов с МС достаточно интересны и требует дальнейшего исследования. Это может быть следствием системной провоспалительной цитокинемии ассоциированной с МС или ишемии детрузора в связи с дефицитом оксида азота, как следствие гипогонадизма. Однако, эти гипотезы и сам факт преобладания ирритативной симптоматики требуют дальнейшего изучения. Аналогичный генез может иметь и синдром хронической тазовой боли у пациентов с МС. Причем, по нашему мнению, отсутствие корреляций простатического кровотока по УЗИ не исключает данной гипотезы, а лишь ставит под вопрос чувствительность метода, а свет на данное предположение смогли бы пролить биохимические, иммунологические и гистохимические методы исследования эякулята и биоптатов предстательной железы. В отношении синдрома хронической тазовой боли мы не исключаем эффект небольшой выборки, что может так же объяснить противоречия с результатами, полученными другими авторами.
ЗАКЛЮЧЕНИЕ
Метаболический синдром выступает независимым фактором эректильной дисфункции и гипогонадизма, что ведет к нарушениям микции и развитию СХТБ. Необходимо продолжить исследования в данном направлении, т.к. понимание деталей патогенеза данных осложнений позволит проводить адекватную патогенетическую терапию.
ЛИТЕРАТУРА
- Alberti G. Introduction to the metabolic syndrome. European Heart Journal Supplements, Volume 7, Issue suppl_D, 1 June 2005, Pages D3–D5. doi.org/10.1093/eurheartj/sui021
- Ziramet P, Shaw J, Alberti G. Preventing type 2 diabetes and the dysmetabolic syndrome in the real world: a realistic view. Diabetic medicine 2003; 20(9): 693-702. oi: 10.1046/Дж.1464-5491.2003.01052.х
- Dekker M, Girman C, Rhodes T. Metabolic Syndrome and 10-Year Cardiovascular Disease Risk in the Hoorn Study. Circulation 2005; doi.org/10.1161/CIRCULATIONAHA.104.516948;112:666-673.
- Flegal KM, Carroll MD, Ogden CL, Johnson CL. Prevalence and trends in obesity among US adults, 1999–2000. JAMA 2002;288(14):1723–7. doi:10.1001/jama.288.14.1723.
- Mancia G, Bomblelli M, Corrao G. Metabolic Syndrome in the Pressioni Arteriose Manitorate E Loro Associazioni (PAMELA) Study: Daily Life Blood Pressure, Cardiac Damage, and Prognosis. Hypertension 2007; 49;40-47; https://doi.org/10.1161/01.HYP.0000251933.22091.24 .
- Knowler WC, Barrett-Connor E, Fowler SE. Diabetes Prevention Program Research Group. Reduction in the incidence of type 2 diabetes with lifestyle intervention or metformin. N Engl J Med. 2002; 346(6):393–403. doi: 10.1056/NEJMoa012512
- Гайнулин Ш.М., Лазебник Л.Б., Дроздов В.Н. Частота повышенного индекса массы тела при проведении целевой диспансеризации по выявлению сердечно-сосудистых заболеваний у населения г.Москвы. Российский кардиологический журнал 2006(3):30-33. http://dx.doi.org/10.15829/1560-4071-2006-3-30-33
- Тишова Ю.А., Калинченко С.Ю. Роль коррекции гипогонадизма в лечении метаболического синдрома у мужчин и аспекты безопасности терапии препаратом тестостерона пролонгированного действия (результаты двойного слепого рандомизированного плацебо-контролируемого исследования). Ожирение и метаболизм. 2010.(2):36-43. doi: 10.2306-5524/1567-5688-2817.
- Stellato RK, Feldman HA, Hamdy O, Horton ES, McKinlay JB. Testosterone, sex hormonebinding globulin, and the development of type 2 diabetes in middle-aged men: prospective results from the Massachusetts male aging study. Diabetes Care. 2000; 23(4): 490–494. doi.org/10.1080/13685530008500343
- Кирпатовский В.И., Мудрая И.С., Греков Е.А., Кабанова И.В., Голованов С.А., Дрожжева В.В., Надточий О.Н. Влияние экспериментально вызванного метаболического синдрома на функциональное состояние мочевого пузыря у крыс. Экспериментальная и клиническая урология.2013(1):8-13.
- Мамедгасанов Р.М., Мехтиев Т.В. Возрастной андрогенный дефицит и эректильная дисфункция у мужчин репродуктивного возраста с сахарным диабетом 2-го типа. Проблемы эндокринологии. 2013(1):3-7. doi.org/10.14341/probl20135913-7 D. Engeler (Chair), A.P. Baranowski, J. Borovicka, A. Cottrell (Guidelines Associate), P. Dinis-Oliveira, S. Elneil, J. et al. Guidelines on Chronic Pelvic Pain. EAU 2015.Available at: http://uroweb.org/wp-content/uploads/EAU-Guidelines-Chronic-Pelvic-Pain-2015.pdf Accessed December 2017. doi: 10.1016/j.eururo.2009.08.020
- Wikipedia. Доступно по https://ru.wikipedia.org/wiki/U-критерий_Манна_—_Уитни. Ссылка активна на декабрь 2017.
Статья опубликована в журнале"Экспериментальная и клиническая урология" №4 2018, стр.78-81








Комментарии