Каприн А.Д., Филимонов В.Б., Васин Р.В., Васина И.В., Васин И.В., Костин А.А.
Проблема хирургического лечения тазового пролапса остается весьма актуальной. По данным различных авторов, от 15 до 30% женщин репродуктивного и пожилого возраста страдают данным заболеванием [1,2]. Olsen AL и соавт. обследовали 149 554 женщины в США и обнаружили, что у 11,1% существует риск подвергнуться операции по поводу тазового пролапса или недержания мочи, а у 29,2% из них уже имелся рецидив заболевания [3]. В России, по данным профилактических осмотров, у 60% женщин выявлены различные отклонения/заболевания: ректоцеле, опущение стенок влагалища и матки, недержание мочи при напряжении, деформация промежности и шейки матки, геморрой, хронические запоры, хронические трещины заднего прохода [4].
До недавнего времени хирургическое лечение пролапса гениталий выполнялось с использованием собственных тканей, что давало до 40% рецидивов [5]. Это вполне объяснимо, так как традиционные методы хирургической коррекции тазового пролапса основаны на использовании заведомо несостоятельных собственных тканей. В настоящее время разработаны различные хирургические методы лечения тазового пролапса у женщин с использованием синтетических имплантатов и тканей трансплантатов доноров [6].
Экстраперитонеальный неофасциогенез при помощи сетчатого полипропиленового имплантата является патогенетически обоснованным методом лечения опущения и выпадения внутренних половых органов и позволяет повысить эффективность хирургического лечения у пациенток с заведомо несостоятельной соединительной тканью [8].
Существенным недостатком применения стандартных наборов для лечения генитального пролапса с применением синтетических имплантатов (Prolift, Johnson&Johnson, USA и AMS Elevate, USA) является высокая стоимость, что ограничивает возможность их использования.
В этой связи изучение воздействия полипропиленового имплантата на окружающие в месте имплантации ткани является одной из важных задач тазовой хирургии. Морфологическое изучение в эксперименте на животных особенностей ответной реакции тканей в месте имплантации полипропиленовых сеток типа I позволяет дать адекватную оценку этим сеткам в зависимости от варианта их плетения, величины ячеек, структуры и физико-химических свойств.
Цель исследования: при помощи морфологических методов изучить особенности гистологической картины, в том числе реакцию системы гистиона, при использовании полипропиленовых сеток «Prolift» (Johnson&Johnson, USA) и «Гинефлекс» (Линтекс, Россия) при фиксации их к мочевому пузырю и имплантации в стенку влагалища.
МАТЕРИАЛЫ И МЕТОДЫ
Экспериментальная работа проведена на 30 кроликахсамках породы Шиншилла весом 3,5 - 4,0 кг. В табл. 1 представлена характеристика эксперимента: вид полипропиленовой сетки, место фиксации импланта и сроки выведения животных из экспериента. Условия эксперимента соответствовали международным требованиям для проведения научных исследований с участием живых организмов.
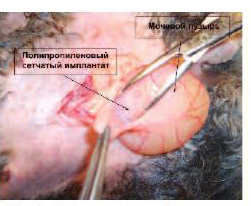
Рис 1. Полипропиленовый имплантат уложен по передней поверхности мочевого пузыря
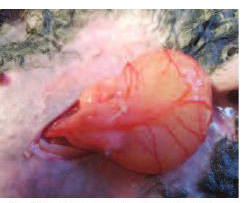
Рис 2. Перитонизация мочевого пузыря с фиксированным к нему полипропиленовым имплантатом
В работе использовались два вида полипропиленовых сеток «Prolift» (Johnson&Johnson, USA) и «Гинефлекс» (Линтекс, Россия). «Гинефлекс» (Линтекс, Россия) – облегченный, мягкий сетчатый имплантат для реконструкции тазового дна, обладающий высокой объемной пористостью (93%). Его состав: полипропиленовые и поливинилиденфторидные мононити диаметром 0,09 мм; толщина сетки 0,37мм, поверхностная плотность 40 г/м2. «Prolift» (Johnson&Johnson, USA) – сетчатый имплантат, выполненный из легковесного (42,7 гр/м2), тонкого (0,42 мм), монофиламентного, плетеного, макропористого полипропиленового материала Prolene Soth.
Таблица 1. Характеристика эксперимента
| Вид полипропиленовой сетки |
Место фиксации полипропиленового имплантата |
Количество животных и сроки выведения их из эксперимента (сутки) |
||||
| 7 | 14 | 60 | 30 | 60 | ||
| Сетка «Prolift» (Johnson&Johnson, USA) |
Передняя стенка мочевого пузыря |
3 | 3 | 3 | 3 | 3 |
| Стенка влагалища | ||||||
| Сетка «Гинефлекс» (Линтекс, Россия) |
Передняя стенка мочевого пузыря |
3 | 3 | 3 | 3 | 3 |
| Стенка влагалища | ||||||
| Итого | 30 | |||||
Все животные оперированы в асептических условиях, под наркозом (премедикация – атропин 0,5-0,6 мг/кг + димедрол 0,3-0,4 мг/кг; наркоз – Zoletil 50 фирмы Virbac 0,03 мл/кг + «Ксила» 0,05 мл/кг). Выполняли нижнюю срединную лапаротомию, обнажали переднюю поверхность мочевого пузыря. Проводили укладку полипропиленового имплантата размером1,0×1,0 см на переднюю поверхность мочевого пузыря: 15 кроликам - сетка «Prolift» (Johnson&Johnson, USA) и 15 кроликам - сетка «Гинефлекс» (Линтекс, Россия) (рис. 1). Имплантат, уложенный на переднюю стенку мочевого пузыря, укрывали висцеральной брюшиной, рану послойно ушивали (рис. 2). Тем же животным разрезали стенку влагалища, полипропиленовый имплантат размером 0,5×0,5см позициони- ровали в стенку влагалища (15 кроликам - сетка «Prolift» (Johnson& Johnson, USA) и 15 кроликам - сетка «Гинефлекс» (Линтекс, Россия), рану ушивали (рис. 3). В послеоперационном периоде в течение 7 дней проводили профилактическую антибактериальную терапию препаратом цефтриаксон (cethriaxonum) 50 мг/кг в сутки.
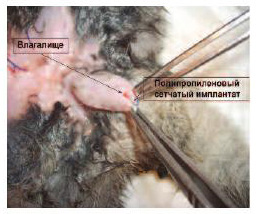
Рис 3. Полипропиленовый имплантат позиционируется в стенке влагалища
На 7, 14, 21, 30, 60 дни после оперативного вмешательства животных выводили из эксперимента с помощью внутривенного введения 15 мл воздуха или передозировки лекарственных препаратов для проведения наркоза (Zoletil, «Ксила»). Изучали макроскопические изменения, микроскопически оценивали течение воспалительного процесса и ультраструктурные особенности в зоне имплантации полипропиленовой сетки.
Переднюю брюшную стенку животных рассекали продольным срединным разрезом. После ревизии брюшной полости иссекали мочевой пузырь с фиксированным к нему полипропиленовым имплантатом и участок влагалища с имплантированной полипропиленовой сеткой. Полученный материал фиксировали в 10% растворе нейтрального формалина, промывался в проточной воде и подвергался препаровке. Затем препараты обезвоживали путем проводки через спирты возрастающей крепости и заливались в целлоидин-парафин.
После этого препараты окрашивали гематоксилином и эозином, по Шиффу и Клаусу-Гроссману на коллаген и накопление гликозоаминогликанов.
Проводили электронно-микроскопическое исследование и оценивали фазу воспаления, состояние воспалительного инфильтрата, интенсивность синтеза коллагена и межуточного вещества, формирование и состояние грануляционной и соединительной ткани, микроциркуляторное русло.
РЕЗУЛЬТАТЫ
Средняя продолжительность операций в эксперименте при фиксации полипропиленового имплантата к передней поверхности мочевого пузыря составила: 14,3±1,9 минуты («Prolift»), 14,7±1,6 минуты («Гинефлекс»); позиционирование имплантата в стенку влагалища – 10,2±2,8 минуты («Prolift»), 9,9±2,5 минуты («Гинефлекс»). Интраоперационных и послеоперационных осложнений не было.
При макроскопической оценке характера изменений в брюшной полости и в месте фиксации полипропиленовых сеток («Prolift» и «Гинефлекс») к мочевому пузырю патологических изменений не выявлено. После вскрытия полости мочевого пузыря во всех 30 случаях обнаружено, что слизистая мочевого пузыря бледно-розового цвета, блестящая, через стенку мочевого пузыря просвечивался полипропиленовый имплантат без эрозирования слизистой. Оценивая макроскопические изменения во влагалище, у всех животных, выведенных из эксперимента в указанные выше сроки, слизистая влагалища была гладкая и блестящая, через нее просвечивалась полипропиленовая сетка (рис. 4, 5).
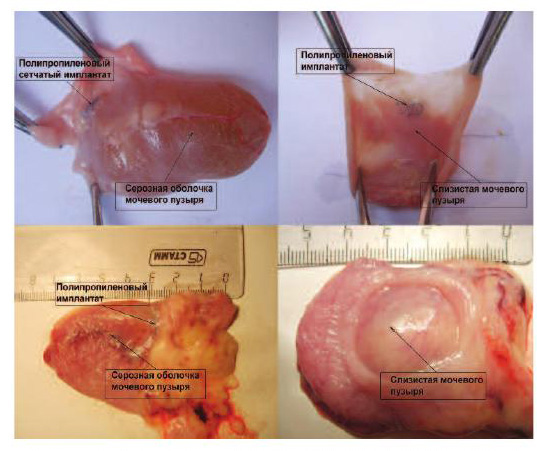
Рис. 4. Макропрепарат - мочевой пузырь (вскрытие через 1 месяц после операции): верхний ряд после имплантации сетки «Prolift», нижний ряд – «Гинефлекс»
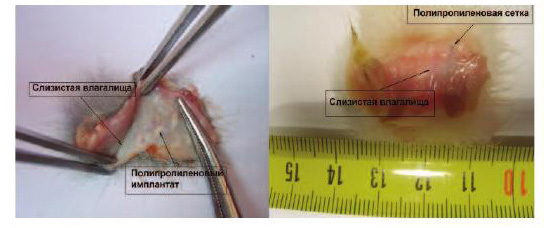
Рис. 5. Макропрепарат – слизистая влагалища в месте имплантации полипропиленовой сетки: слева - после имплантации сетки «Prolift», справа – «Гинефлекс»
При исследовании гистологического материала стенки влагалища в месте имплантации полипропиленовых сеток на 7 день после операции по периферии имплантата отмечается умеренное полнокровие сосудов, преимущественно артериального типа, умеренный отек стромы, не ярко выраженная лейкоцитарно-макрофагальная реакция (фаза асептического воспаления) (рис. 6).
При гистологическом исследовании мочевого пузыря и паравезикальной клетчатки в месте прикрепления полипропиленовых сеток через 7 суток после операции отмечается умеренноыраженная реакция сосудистого русла в виде пареза мелких артериальных сосудов и артериол; плазматическое пропитывание стенок сосудов с периваскулярной плазморрагией и отеком стромы мочевого пузыря. В строме отмечается умеренная лейкоцитарная и макрофагальная инфильтрация (рис. 7). По периферии полипропиленовых имплантатов наблюдалли умеренную дезорганизацию коллагеновых волокон и межуточного вещества.
На 14-й день после имплантации полипропиленовых сеток в стенку влагалища при микроскопическом исследовании выявили единичные фибробласты, гиперемию преимущественно в сосудах венозного типа, при этом клеточный инфильтрат состоял преимущественно из лейкоцитов, отмечены единичные эозинофилы, тучные клетки и умеренная плазмотизация отдельных лимфоцитов (рис. 8).
На 14 сутки после фиксации полипропиленовой сетки к передней стенке мочевого пузыря наблюдали уменьшение интенсивности экссудативной фазы воспалительной реакции и начало стадии пролиферации. Отмечено уменьшение отека стромы, исчезновение периваскулярных кровоизлияний. Обнаружено изменение клеточного состава в инфильтрате: практически полностью отсутствовали нейтрофильные лейкоциты, преобладали макрофаги, лимфоциты, единичные эозинофилы, отмечается скопление фибробластов (рис. 9). При окраске на коллаген фиксировались вновь образованные коллагеновые волокна и накопление гликозаминогликанов. В околопузырной клетчатке наблюдаютли умеренную пролиферацию фибробластов и участки полиморфнолеточной инфильтрации как островки формирования молодой грануляционной ткани.
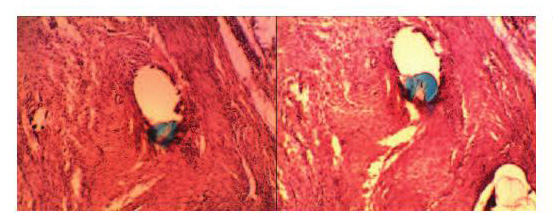
Рис. 6. Гистологические изменения в тканях влагалища кролика в месте имплантации полипропиленовой сетки на 7 сутки (в центре фотографии полипропиленовая нить синего цвета): слева - сетка «Prolift», справа – «Гинефлекс». Окраска гематоксилином и эозином. Ув. 200х
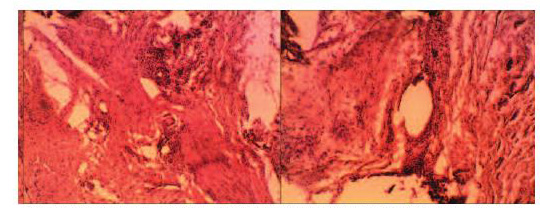
Рис. 7. Микропрепарат – реакция тканей стенки мочевого пузыря кролика вокруг полипропиленовой сетки на 7 сутки после ее имплантации (слева - сетка «Prolift», справа – «Гинефлекс»). Окраска гематоксилином и эозином. Ув. 200х
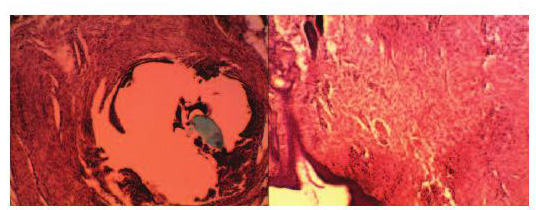
Рис. 8. Микропрепарат – реакция тканей стенки влагалища кролика на 14 сутки после имплантации полипропиленовой сетки: слева - сетка «Prolift», справа – «Гинефлекс». Окраска гематоксилином и эозином. Ув. 200х
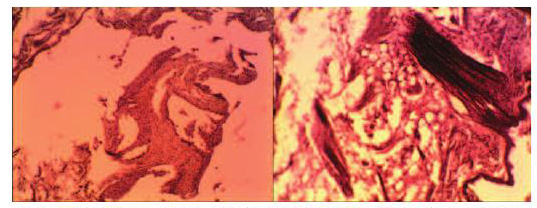
Рис. 9 . Микропрепарат – реакция тканей стенки мочевого пузыря кролика вокруг полипропиленовой сетки на 14 сутки после ее имплантации: слева - сетка «Prolift», справа – «Гинефлекс». Окраска гематоксилином и эозином. Ув. 200х
На 21й день после имплантации полипропиленовых сеток в стенку влагалища при микроскопии отмечали отсутствие венозной и артериальной гиперемии, снижение отечности стромы, клеточный инфильтрат состоял преимущественно из фибробластов, появились единичные вновь образуемые коллагеновые волокна (рис. 10).
На 21 сутки после фиксации полипропиленовых сеток к передней стенке мочевого пузыря наблюдали сформированную нежноволокнитостую соединительную ткань без признаков воспалительной реакции окружающих тканей, отмечали интенсивное накопление гликозоаминогликанов (рис. 11).
При гистологическом исследовании материала через 30 суток после фиксации полипропиленовых сеток к передней стенке мочевого пузыря и имплантации их в стенку влагалища мы не обнаружили какихлибо изменений воспалительного или склеротического характера в месте прикрепления сетки и по периферии места прикрепления. Через 60 суток после прикрепления полипропиленовых имплантатов мы наблюдали формирование тонкого слоя рубцовой соединительной ткани по периферии сетки (рис. 12, 13).
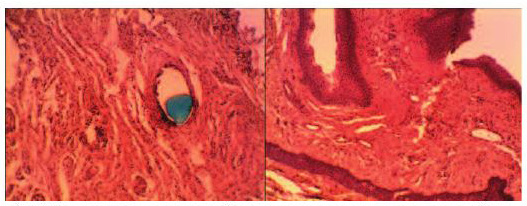
Рис. 10. Микропрепарат – реакция тканей влагалища кролика вокруг полипропиленовой сетки на 21 сутки после ее имплантации: слева - сетка «Prolift», справа – «Гинефлекс». Окраска гематоксилином и эозином. Ув. 200х
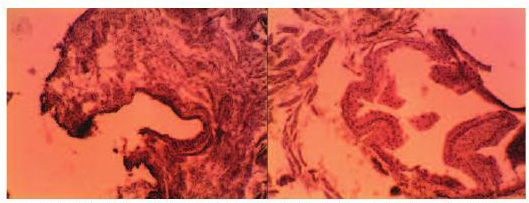
Рис. 11. Микропрепарат – реакция тканей стенки мочевого пузыря кролика на 21 сутки в зоне имплантации полипропиленовой сетки: слева - сетка «Prolift», справа – «Гинефлекс». Окраска гематоксилином и эозином. Ув. 200х
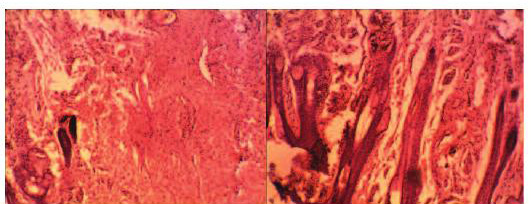
Рис. 12. Микропрепарат – реакция тканей влагалища кролика вокруг полипропиленовой сетки на 30 сутки после ее имплантации: слева - сетка «Prolift», справа – «Гинефлекс». Окраска гематоксилином и эозином. Ув. 200х
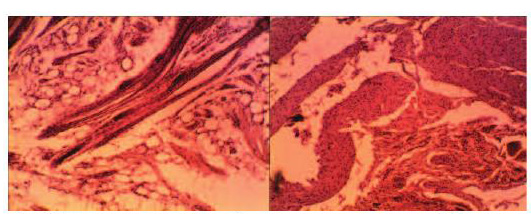
Рис. 13. Микропрепарат – реакция тканей стенки мочевого пузыря кролика на 30 сутки в зоне имплантации полипропиленовой сетки: слева - сетка «Prolift», справа – «Гинефлекс». Окраска гематоксилином и эозином. Ув. 200х
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Согласно литературным данным, существует множество экспериментальных работ по изучению особенностей тканевой реакции при имплантации различных видов полипропиленовых сеток в герниологии, но, к сожалению, мало изучено взаимодействие этих сеток при имплантации к стенке мочевого пузыря и в стенку влагалища.
Однако известно, что реакция тканей в месте имплантации сетчатого материала проходит определенные стадии. Так, имплантация большинства сетчатых материалов вызывает развитие острого или подострого воспаления с умеренным отеком и инфильтрацией полиморфноядерными лейкоцитами и макрофагами в течение 1-3 недель. Затем эти изменения переходят в хроническое воспаление, окружающее инородное тело, с одновременным формироваием богатой коллагеновыми волокнами рубцовой ткани, образующей трехмерную структуру вокруг и внутри сетчатого имплантата. При этом число фибробластов и уровень васкуляризации имеют обратную корреляционную зависимость с воспалительной реакции, тогда как выраженное острое воспаление на начальных этапах имплантации вызывает образование значительного количества фиброзной ткани [9,10].
Оценка микроскопических и ультраструктурных особенностей в зоне имплантации полипропиленовых сеток экспериментальным животным показала во всех случаях развитие преимущественно асептической воспалительной реакции (через 7 суток) и затем преимущественно фибропластической (через 14, 21, 30 и 60 суток) реакции, при этом не отмечалось какой-либо заметной воспалительной реакции или избыточного тканевого роста. Динамика морфологических изменений тканей в месте имплантации исследуемых полипропиленовых сеток типа I («Prolift» (Johnson&Johnson, USA) и «Гинефлекс» (Линтекс, Россия) к стенке мочевого пузыря и в стенку влагалища не зависела от варианта их плетения, величины ячеек, структуры и физико- химических свойств. Таким образом, воспалительнорепаративная реакция с образованием рубца сопровождала имплантацию изучаемых сеток, а реакция на имплантацию полипропиленовых сеток как в ранние сроки после начала эксперимента, так и в отдаленные, была по основным признакам сходной и сопоставимой с результатами экспериментальных исследований в герниологии. Изученные нами полипропиленовые сетки характеризуются выраженной интеграцией с окружающими тканями в зоне имплантации, что позволяет их рекомендовать для использования в клинической практике.
Вместе с тем, следует отметить, что эксперименты на животных, имеют свои особенности, и результаты их не могут быть перенесены на ситуацию с человеком. Более благоприятный эффект использования новых сеток должен быть выявлен в рандомизированном исследовании в человеческой популяции.
ВЫВОДЫ
Согласно полученным экспериментальным данным, изучаемые полипропиленовые сетки «Prolift» (Johnson&Johnson, USA) и «Гинефлекс» (Линтекс, Россия), при фиксации к мочевому пузырю и имплантации в стенку влагалища, являются биологически инертными синтетическими материалами. При сравнении гистологической картины в месте имплантации полипропиленовых сеток («Prolift» и «Гинефлекс») различий не отмечено.
В данном экспериментальном исследовании впервые дана сравнительная оценка реакции тканей мочевого пузыря и влагалища в месте имплантации сетки «Prolift» (Johnson&Johnson, USA), являвшейся эталоном в лечении тазового пролапса на момент начала данной работы, и сетки «Гинефлекс» (Линтекс, Россия). (Прим. редакции).
ЛИТЕРАТУРА
1. Кулаков В. И. Альтернативный подход к хирургической коррекции неправильных положений матки. // Акушерство и гинекология. 1995. № 6. С.36-39.
2. Wattiez A. et al. Laparoscopic operations for stress incontinence and prolapsed. // Proc. of Int. Cong. Endoscopy for diagnosis and treatment of uterine pathology. I. – Moscow, 1997.– P. 165–173.
3. Olsen A, Smith V, Bergstrom J, Colling JC, Clark AL. Epidemiology of surgically managed pelvic organ prolapse and urinary incontinence. // Obstet Gynecol. 1997. Vol. 89, N 4. P. 501-506.
4. Куликовский В.Ф., Олейник Н.В. Тазовый пролапс у женщин: руководство для врачей. М.: ГЭОТАР-Медиа, 2008. - 256 с.
5. Пушкарь Д.Ю. Диагностика и лечение сложных и комбинированных форм недержания мочи у женщин: Дис. … д-ра мед. наук. М., 1996. 258 с.
6. MiklosJR, Kohli N, Moore RD. Levator plasty release and reconstruction of rectovaginal septum using allogenic dermal graft. // lnt UrogynecolJ Pelvic Floor Dysfunct. 2002. Vol. 13. P. 446.
7. Jia X, Glazener C, Mowatt G, MacLennan G, Bain C, Fraser C, Burr J. Efficacy and safety of using mesh or graths in surgery for anterior and/or posterior vaginal wall prolapse: systematic review and meta-analysis. // BJOG. 2008. Vol. 115, N 11. P. 1350-1361.
8. Шалаев О.Н., Царьков П.В., Васильева Т.Б., Озова М.М. Экстраперитонеальный неофасцеогенез у женщин репродуктивного возраста. // Материалы международного конгресса «Дисфункция тазового дна у женщин» М. 2008. С. 69.
9. Klosterhalfen B, Klinge U, Hermanns B, Schumpelick V. Pathology of traditional surgical nets for hernia repair after long-term implantation in humans. //Chirurg. 2000. Vol. 71, N 1. P. 43-51.
10. Дубова Е.А., Щеголев А.И., Чекмарева И.А., Филаткина Н.В., Чижов Д.В., Егиев В.Н. Тканевая реакция на имплантацию облегченных полипропиленовых сеток. // Бюллетень экспериментальной биологии и медицины. 2006. № 12. С. 687-692.
Статья опубликована в журнале "Экспериментальная и клиническая урология". Номер №1/2013 стр. 24-29









Комментарии