Асратов А.Т., Качмазов А.А., Костин А.А.
Рак предстательной железы (РПЖ) относится к числу наиболее часто встречающихся злокачественных новообразований у мужчин. Так, по данным отечественных источников в РФ за последние 5 лет РПЖ вышел на шестое место среди онкологических заболеваний и тенденция к дальнейшему увеличению роста заболеваемости сохраняется [1-5]. Радикальная простатэктомия (РПЭ) является наиболее часто используемым методом лечения больных с локализованным РПЖ [2,6-9]. В последние годы все чаще используют малоинвазивные варианты операции – лапароскопическую и робот-ассистированную РПЭ [10-12]. При всех вариантах этой операции в связи с удалением предстательной железы (ПЖ) происходит пересечение нервных и сосудистых связей между шейкой мочевого пузыря и задней уретрой, что может приводить к нарушению нейрогенной регуляции мочеиспускания, ишемии дистальных отделов мочевого пузыря и, как следствие, – к развитию симптомов нижних мочевых путей и недержания мочи [13].
Недержание мочи наряду с эректильной дисфункцией является наиболее частым осложнением РПЭ, существенно ухудшающим качество жизни больных. В раннем послеоперационном периоде недержание мочи возникает практически у всех больных, но с увеличением времени, прошедшего после операции, функция удержания мочи у большинства пациентов восстанавливается. По данным Б.Я. Алексеева через 6 месяцев после РПЭ 74,6% пациентов могли удерживать мочу, через 9 месяцев – уже 92,6%, однако в 7,4% случаев недержание мочи сохранялось более года [6]. В зарубежной литературе приводятся разные сведения о частоте длительного сохранения недержания мочи (1-3 года) с колебаниями от 7% до 41,9% [14,15], в большей части публикаций эта цифра колеблется от 12 до 24% [16–19]. С внедрением лапароскопических и робот-ассистированных методов РПЭ рассчитывали на уменьшение частоты развития стойкого недержания мочи в послеоперационном периоде. Однако эти надежды не оправдались: распространенность этого осложнения осталась примерно на том же уровне [20]. Согласно данным I.H. Shao и соавт. через 1 месяц после робот-ассистированной РПЭ недержание мочи отмечено у 63,3%, и у 16% больных оно сохранилось в течение двух лет [21].
Развитие указанного осложнения значительно ухудшает качество жизни пациентов. При этом ухудшается и психологическое состояние таких больных [10,16,22] вплоть до необходимости оказания психологической поддержки ряду пациентов в связи со стойким развитием тревожности и депрессии [23-26].
Современные тенденции лечения недержания мочи, развившегося после РПЭ, включают в себя этапное лечение, начинающееся с тренировки мышц тазового дна с подключением при необходимости медикаментозной терапии, а при их неэффективности – выполнение хирургической коррекции [27,28]. Наиболее распространенными методами хирургических вмешательств у таких больных являются установка петлевых (слинговых) систем [2931] и имплантация искусственного сфинктера уретры [14,32,33]. У большинства пациентов перечисленные операции приводят к значительному улучшению состояния, однако вопрос о валидизированной оценке их влияния на улучшение качества жизни и психологического статуса этих больных освещен недостаточно.
Учитывая эти данные, целью настоящего исследования явилось изучение роли коррекции недержания мочи, развившегося после РПЭ, путем выполнения уретросуспензии с помощью петлевой системы Аргус в реабилитации этой категории больных с оценкой качества их жизни и психологического состояния.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Были проанализированы истории болезни 260 пациентов, перенесших радикальную простатэктомию по поводу рака предстательной железы в МНИОИ им. П.А. Герцена. Больных обследовали в различные сроки после операции (до и после операции – 28 пациентов, через 3 месяца – 30 пациентов, через 6 месяцев – 33 пациента, через 9 месяцев – 36 пациентов, через 1 год – 51 пациент, через 2 года – 44 пациента и через 3 года – 38 пациентов). При этом первая группа больных (до и после операции, 28 чел.) представляла собой собственный материал авторов в полном объеме, включая диагностику и хирургическое лечение. Остальные 6 групп взяли для научного изучения из базы данных МНИОИ им. П.А. Герцена и обследовали согласно нижеприведенной схеме.
Кроме указанной общей выборки из 260 больных, была сформирована группа из 31 пациента, у которых после РПЭ развилось стойкое недержание мочи, сохраняющееся через 12 и более месяцев после простатэктомии (примерно половину составляли лица с послеоперационным сроком наблюдения более двух лет, треть – более трех лет). Больным этой группы была выполнена уретросуспензия с установкой петлевой (слинговой) системы Аргус. Операции проводились в НИИ урологии и интервенционной радиологии им. Н.А. Лопаткина.
Основу обследования составило анкетирование на основе опросника KHQ (опросник состояния здоровья Кинга) и опросника Спилбергера – Ханина, характеризующего психологическое состояние пациента, оцененное по уровню ситуативной тревожности (СТ) (опасения, связанные с состоянием здоровья на момент обследования) и личностной тревожности (ЛТ), обусловленной индивидуальной реакцией пациента на состояние своего здоровья.
Анализ результатов анкетирования по KHQ проводили по модифицированной методике, предложенной А.А. Железной и соавт., согласно которой нормальное состояние здоровья соответствует 26-30 баллам, хорошее качество жизни – 31-50 баллам, удовлетворительное качество жизни – 51-70 баллам и плохое качество жизни – 71-90 баллам [34]. На основании результатов анкетирования по Спилбергеру – Ханину низкий уровень тревожности соответствует 20-30 баллам средний уровень – 31-45 баллам и высокий уровень тревожности – 46 баллам и более.
Количественные характеристики анализировали статистически с использованием методов непараметрической и вариационной статистики с помощью компьютерных программ «Excel 2007» и «Statistica 8.0». Средние значения в группах выражали в виде средней и ошибки средней (М±m). Достоверность различий между группами оценивали с использованием критерия Стьюдента – t, а выраженность корреляционных связей между отдельными показателями – при помощи коэффициента корреляции Спирмена – r. Достоверными считали различия при p<0,05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Субъективная оценка своего здоровья по опроснику KHQ пациентами в различные сроки после РПЭ показала, что сразу после операции подавляющее число больных оценивало свое состояние как плохое (71,4%), еще 25% больных считали состояние своего здоровья удовлетворительным и лишь 3,6% пациентов ощущали себя почти здоровыми (табл. 1).
Таблица 1. Динамика оценки состояния здоровья больных в разные сроки после РПЭ (согласно анкетированию по KHQ)
| Срок после операции | Нормальное | Хорошее | Удовлетворительное | Плохое |
|---|---|---|---|---|
| 10 дней после операции (n=28) | 0% | 3,6% | 25,0% | 71,4% |
| 3 мес. (n=30) | 0% | 33,3% | 50,0% | 16,7% |
| 6 мес. (n=33) | 18,2% | 60,6% | 9,1% | 12,1% |
| 9 мес. (n=36) | 11,4% | 31,4% | 48,6% | 8,6% |
| 1 год (n=51) | 19,6% | 37,3% | 35,3% | 7,8% |
| 2 года (n=44) | 6,8% | 52,3% | 25,0% | 15,9% |
| 3 года (n=38) | 13,2% | 47,4% | 34,2% | 5,3% |
Однако с увеличением времени, прошедшего после операции, ситуация постепенно менялась. Доля больных с оценкой состояния своего здоровья как плохое уже через 3 месяца после операции уменьшилась практически в 4 раза, а к 6 месяцам – более чем в 5 раз, с последующими небольшими колебаниями. При этом доля пациентов с оценкой своего здоровья как нормальное и хорошее значительно возрастала через 3 и, особенно, через 6 месяцев после операции (от 3,6% до 33,3% и 78,8%, соответственно). Через 9 месяцев процент больных, оценивающих качество своей жизни как нормальное и хорошее, снижалось до 42,8%, но в дальнейшем (через 1–3 года) несколько повышалось и оставалось стабильным, колеблясь в интервале 56,9–60,6%.
Также отмечено значительное уменьшение доли больных, оценивающих свое состояние здоровья как удовлетворительное через 6 месяцев после операции (с 50% при сроке 3 месяца до 9,1% через 6 месяцев) с последующим возрастанием доли этих больных до 25–48,6%.
Уменьшение числа больных, оценивающих состояние своего здоровья как удовлетворительное через 6 месяцев и как хорошее через 9–12 месяцев, могло быть связано как с ухудшением онкологической ситуации, так и со стойким сохранением симптомов нарушенного мочеиспускания (в том числе недержания мочи) у ряда больных. В связи с этим, мы отдельно проанализировали состояние пациентов, у которых в эти сроки сохранилось выраженное недержание мочи и которым в дальнейшем была выполнена коррекция этого состояния путем установки петлевой системы Аргус.
При сравнении субъективной оценки качества жизни по опроснику KHQ пациентов с недержанием мочи и всех пациентов через 12 месяцев после РПЭ оказалось, что все больные, у которых развилось выраженное недержание мочи, расценивали свое состояние здоровья как плохое. Средний балл в этой группе пациентов составил 79,4±1,9, колеблясь от 71 до 103. В то же время пациентов из наблюдения через 12 месяцев сумма баллов KHQ колебалась от 29 до 85. Однако лишь 7,8% пациентов расценивали состояние своего здоровья как плохое, тогда как более половины больных считали свое здоровье нормальным или хорошим, а 35,3% – удовлетворительным (табл. 2).
Таблица 2. Сравнительная характеристика состояния здоровья больных с недержанием мочи и всех больных через 1 год после РПЭ (результаты анкетирования по KHQ)
| Группы | Нормальное | Хорошее | Удовлетворительное | Плохое |
|---|---|---|---|---|
| Все больные через 12 мес. (n=51) | 19,6% | 37,3% | 35,3% | 7,8% |
| Больные с недержанием мочи (n=31) | 0%*** | 0%*** | 0%*** | 100%*** |
Примечание: *** – различия между группами достоверны при p<0,001
Средний балл субъективной оценки качества жизни в группе пациентов через 12 месяцев составил 49,1±1,6, а у больных с недержанием мочи – 79,4±1,5 (различия достоверны при (рис. 1).
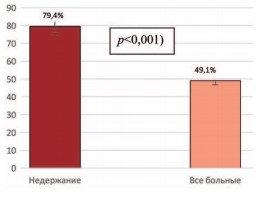
Рис. 1. Средний балл по опроснику KHQ во всей группе больных через 1 год после РПЭ и у больных с развившимся недержанием мочи (*** p<0,001)
В соответствии с плохим качеством жизни у больных с недержанием мочи значительно ухудшается их психологическое состояние. Уровень ситуативной тревожности у подавляющего числа больных с недержанием мочи был высокий и средний (29,7 и 69,7%, соответственно), а низкий уровень отмечался лишь в 5,9% случаев, тогда как у больных через 12 месяцев после РЭП преобладал низкий уровень тревожности (52,9%), а средний и высокий уровень выявлялся у 31,3 и 15,7% больных, соответственно (рис. 2А). Различия в распределении больных в группах оказались статистически достоверными при p<0,001.
Уровень личностной тревожности в обеих группах был выше, чем ситуативной. Во всей группе анализируемых больных низкий уровень тревожности был лишь у 11,7% больных, а средний и высокий – у 45,1 и 43,1%, соответственно. В то же время у больных с недержанием мочи тревожность была еще выше. Низкий уровень личностной тревожности не обнаружен ни у кого из больных, а средний и высокий – в 29,4 и 70,6%, соответственно (рис. 2Б). Различия в распределении больных по этому показателю также оказались статистически значимыми при p<0,01.
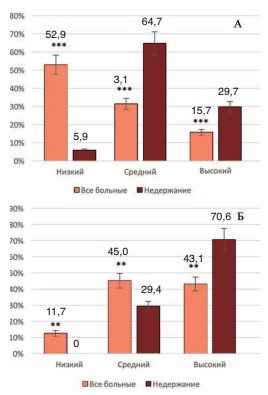
Рис. 2. Распределение больных по уровню тревожности по данным опросника Спилбергера – Ханина. А – уровень ситуативной тревожности (*** p<0,001), Б – уровень личностной тревожности (*** p<0,001)
Средние значения баллов тревожности в группе пациентов с недержанием мочи оказались достоверно выше, чем во всей группе пациентов, составив для ситуативной тревожности 50,9±1,5 и 27,1±1,5 соответственно, а для личностной тревожности – 79,5±1,3 и 42,8±1,1 (рис. 3).
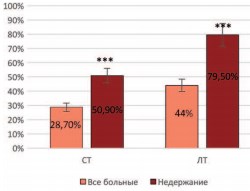
Рис. 3. Средние значения ситуативной (СТ) и личностной тревожности (ЛТ) у больных с недержанием мочи и в общей группе пациентов (согласно опроснику Спилбергера – Ханина) (р<0,001)
Корреляционный анализ взаимосвязи субъективной оценки своего здоровья по KHQ и психологического состояния по Спилбергеру – Ханину выявил достоверную положительную зависимость между этими показателями (рис. 4). У больных с высокой суммой баллов по KHQ (плохое качество жизни) отмечались более высокие баллы по Спилбергеру – Ханину (более высокий уровень тревожности). Коэффициент корреляции между этими показателями составил r=0,401 при уровне достоверности p<0,05.
Таким образом, развитие недержания мочи после РПЭ сопровождается значительным ухудшением качества жизни этих пациентов, а также ухудшением их психологического статуса с повышением уровня как ситуативной тревожности, связанной в значительной степени с опасениями сохранения этого осложнения в дальнейшем послеоперационном периоде, так и личностной тревожности, отражающей индивидуальное восприятие состояния здоровья вследствие развития недержания мочи и ухудшения общего состояния в целом.
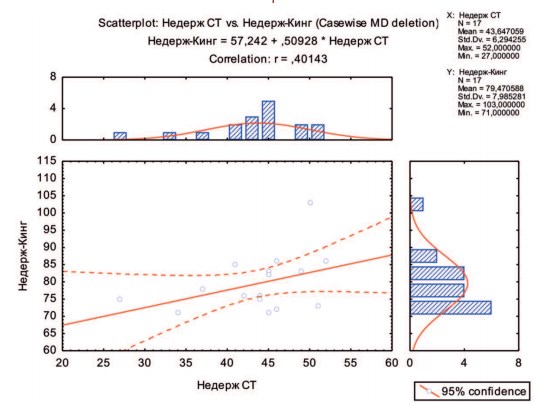
Рис. 4. Корреляционная зависимость между качеством жизни и психологическим состоянием больных с недержанием мочи, развившимся после РПЭ
В связи с этими данными возникает вопрос о возможности реабилитации этих пациентов с помощью операций, направленных на восстановление континенции, в том числе уретросуспензии с помощью петлевой системы Аргус.
Анализ качества жизни и психологического состояния рассматриваемых больных после установки слинговой системы Аргус продемонстрировал значительное улучшение как качества жизни, так и психологического состояния этих пациентов. Если до операции все больные оценивали по опроснику Кинга свое состояние как плохое (100%), то после установки системы Аргус 32,3% пациентов оценивали состояние своего здоровья как нормальное, 45,2% – как хорошее, 16,1% – как удовлетворительное и лишь 6,5% пациентов не отметили улучшения и по-прежнему оценивали состояние своего здоровья как плохое (рис. 5).
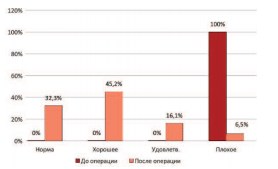
Рис. 5. Распределение больных по оценке качества жизни больными с недержанием мочи до и после установки петлевой системы Аргус
В соответствии с положительным изменением оценки состояния своего здоровья положительно менялся и психологический статус этих пациентов. Как ситуативная, так и личностная тревожность после установки системы Argus значительно уменьшались. Если до операции больных с низким уровнем тревожности почти не было (лишь у 1 больного показатель ситуативной тревожности был ниже 30 баллов), то после операции их доля составила 87,1% при резком уменьшении доли пациентов со средним и высоким уровнем тревожности (рис. 6 А, Б). Лишь у 12,9% пациентов сохранялся высокий уровень ситуативной тревожности и у 6,5% – личностной тревожности. У этих пациентов операция оказалась неэффективной или малоэффективной, что и обусловило сохранение низкого качества их жизни и психологического дискомфорта.
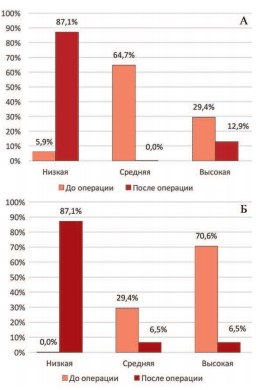
Рис.6. Распределение больных по уровню ситуативной (А) и личностной тревожности (Б) у больных с недержанием мочи, развившимся после РПЭ до и после установки петлевой системы Аргус
Таким образом, наши результаты показали, что у подавляющего числа больных коррекция недержания мочи оказала выраженный реабилитационный эффект, что свидетельствует о перспективности использования методики уретросуспензии для улучшения качества жизни пациентов с этим осложнением РПЭ.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
У всех больных, вошедших в исследование, оценивали влияние операции на показатели состояния здоровья и психоэмоционального состояния и их изменения в отдаленном послеоперационном периоде. При этом нашей целью было выявление общих тенденций в изменении состояние больных, характерных для всей популяции оперированных пациентов. Поэтому мы не ставили своей целью оценить индивидуальные изменения для каждого больного в динамике, поскольку на них могут влиять множество факторов, анализ которых не входил в задачи нашего исследования. Эти показатели были нужны для того, чтобы объективно оценить, насколько развившееся после операции недержание мочи ухудшает физическое и психологическое состояние этих пациентов в сравнении с общей популяцией больных в сопоставимом послеоперационном периоде и в какой степени коррекция этого осложнения способствует реабилитации больных.
Проведенное исследование установило, что в раннем послеоперационном периоде после РПЭ все пациенты оценивают качество своей жизни как низкое, что обусловлено травматичностью операции, длительным сохранением болевого синдрома, развитием недержания мочи. Однако со временем оценка качества жизни пациентами повышается, что в целом соответствует данным литературы [16,24]. Тем не менее, нами зарегистрировано временное ухудшение показателей KHQ через 9–12 месяцев после операции, что, по нашему мнению, вызвано с осложнениями позднего послеоперационного периода, связанными как с ухудшением онкологической ситуации, так и с неонкологическими причинами, в частности, сохранением выраженного недержания мочи и эректильной дисфункции. В настоящей работе мы не проводили анализ значимости всех этих потенциальных факторов, а остановились на одном из них – сохранении недержания мочи.
Анализ показал, что развитие этого осложнения ухудшает качество жизни и психологическое состояние пациентов, оцененное через 12 месяцев, хотя в более раннем послеоперационном периоде эти параметры были более благоприятными. При этом выявилась достоверная корреляция между оценкой больными с недержанием мочи качества жизни и их психологического состояния, определенного по уровню тревожности: у больных с более низкими показателями качества жизни отмечался более высокий уровень тревожности.
Оценке психологического статуса онкологических больных в последнее время придают большое значение [25,35]. Было найдено, что уже само установление диагноза РПЖ ведет у ряда больных к развитию депрессивного состояния, что может усугубляться в связи с необходимостью проведения оперативного лечения. Это выявляется более чем у половины обследованных больных [24,35]. Высокий уровень тревожности может сохраняться длительное время после операции и это может быть связано как с ростом уровня ПСА, так и с низким качеством жизни в связи с развитием осложнений [26].
В связи с этим мы оценили, как меняются качество жизни и психологический статус пациентов после коррекции недержания мочи с помощью установки петлевой системы Аргус. Наши данные говорят о выраженном реабилитационном эффекте такой операции. Подавляющее большинство больных (77,5%) отметило значительное улучшение качества жизни, квалифицируя ее как нормальное или хорошее, еще 16,1% – как удовлетворительное и лишь у 6,5% состояние не улучшилось. В соответствии с этим улучшалось и психологическое состояние этих пациентов с полной нормализацией в 87,1% случаев.
ЗАКЛЮЧЕНИЕ
Таким образом, проведенное нами исследование убедительно свидетельствует о целесообразности коррекции недержания мочи, развившегося у больных РПЖ после РПЭ, в частности с помощью уретросуспензии путем установки петлевых систем, что может составлять важный компонент реабилитации больных РПЖ.
ЛИТЕРАТУРА
1. Давыдов М.И., Матвеев В.Б. Статистика онкоурологических заболеваний в 2010 году. Вестник РОНЦ им. Н.Н. Блохина. 2011; 22(3(85), приложение 1):13–14.
2. Злокачественные новообразования в России в 2013 году (заболеваемость и смертность) [Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой]. М., 2015. 250 с.
3. Костин А.А., Асратов А.Т., Кульченко Н.Г., Толкачев А.О. Прогнозирование развития рака предстательной железы с помощью общих моделей дискриминантного анализа. Вестник Российского университета дружбы народов. Серия: Медицина. 2015; (3): 67–74.
4. Аполихин О.И., Сивков А.В., Катибов М.И., Рощин Д.А., Шадеркин И.А., Корякин А.В. Скрининг рака предстательной железы: оценка с позиций клинико-экономической эффективности. Экспериментальная и клиническая урология. 2015; (2): 20–24.
5. Каприн А.Д., Аполихин О.И., Сивков А.В., Солнцева Т.В., Комарова В.А. Анализ уронефрологической заболеваемости и смертности в Российской Федерации за период 2002–2014 гг. по данным официальной статистики. Экспериментальная и клиническая урология. 2016; (3): 4–13.
6. Алексеев Б.Я. Лечение локализованного и местно-распространенного рака предстательной железы: автореф. на соиск. учен. степ. д-ра мед. наук. М., 2007. 47 с.
7. Алексеев Б.Я. Рак предстательной железы. 2012 URL: www.introdes.ru.
8. Каприн А.Д., Костин А.А., Филимонов В.Б., Васин Р.В., Иванова А.Ю. Отдаленные результаты радикальной позадилонной простатэктомии. Российский медико-биологический вестник им. академика И.П. Павлова. 2015; (1): 120–129.
9. Siegel R., Ma J., Zou Z., Jemal A. Cancer Statistics, 2014. CA Cancer J Clin 2014;64(1):9– 29. doi: 10.3322/caac.21208.
10. Gershman B., Psutka S.P., McGovern F.J., Dahl D.M., Tabatabaei S., Gettman M.T., – et. al. Patient-reported functional outcomes following open, laparoscopic, and robotic assisted radical prostatectomy performed by high-volume surgeons at high-volume hospitals. Eur Urol Focus 2016; 2(2): 172–179. doi: 10.1016/j.euf.2015.06.011.
11. Ilic D, Evans SM, Allan CA, Jung JH, Murphy D, Frydenberg M. Laparoscopic and robotic-assisted versus open radical prostatectomy for the treatment of localised prostate cancer. Cochrane Database Syst Rev 2017 Sep 12; 9:CD009625. doi:10.1002/14651858.CD009625.pub2.
12. Wang M, Xie X, Wells D, Higgins C. Robotic surgical system for radical prostatectomy: A health technology assessment. Ont Health Technol. Assess Ser 2017; 17(11): 1–172.
13. Song C, Lee J, Hong JH, Choo MS, Kim CS, Ahn H. Urodynamic interpretation of changing bladder function and voiding pattern aer radical prostatectomy: a long-term follow-up. BJU Int. 2010; 106(5): 681–686. doi: 10.1111/j.1464-410X.2009.09189.x.
14. Ventimiglia E, Folkvaljon Y, Carlsson S, Bratt O, Montorsi F, Volz D, et. al. Nationwide, population based study of postradical prostatectomy urinary incontinence correction surgery. J Surg Oncol 2017 Sep 6. doi: 10.1002/jso.24816. [Epub ahead of print].
15. Mohamad Al-Ali B, Ponholzer A, Augustin H, Madersbacher S, Pummer K. e long-term effect of radical prostatectomy on erectile function, urinary continence, and lower urinary tract symptoms: A comparison to age-matched healthy controls. Biomed Res Int 2017. 2017:9615080. doi: 10.1155/2017/9615080.
16. Pompe RS, Tian Z, Preisser F, Tennstedt P, Beyer B, Michl U, et. al. Shortand longterm functional outcomes and quality of life aer radical prostatectomy: Patient-reported outcomes from a tertiary high-volume center. Eur Urol Focus 2017 Aug 28. doi:10.1016/j.euf.2017.08.001. [Epub ahead of print].
17. Tienza A, Robles JE, Hevia M, Algarra R, Diez-Caballero F, Pascual JI. Prevalence analysis of urinary incontinence aer radical prostatectomy and influential preoperative factors in a single institution. Aging Male 2017 Aug 31:1–7. doi: 10.1080/13685538.2017.1369944. [Epub ahead of print].
18. Daugherty M, Chelluri R, Bratslavsky G, Byler T. Are we underestimating the rates of incontinence aer prostate cancer treatment? Results from NHANES. Int Urol Nephrol 2017 Jul 14. doi: 10.1007/s11255-017-1660-5. [Epub ahead of print].
19. Hikita K, Honda M, Kawamoto B, Tsounapi P, Muraoka K, Sejima T, et. al. Evaluation of incontinence aer robot-assisted laparoscopic radical prostatectomy: Using the international consultation on incontinence modular questionnaire short form and noting the number of safety pads needed by japanese patients. Yonago Acta Med 2017; 60(1): 52–55.
20. Haga N, Takinami R, Tanji R, Onagi A, Matsuoka K, Koguchi T, et. al. Comprehensive approach for post-prostatectomy incontinence in the era of robot-assisted radical prostatectomy. Fukushima J Med Sci 2017; 63(2): 46–56. doi: 10.5387/fms.2017-15.
21. Shao IH, Chang YH, Hou CM, Lin ZF, Wu CT. Predictors of short-term and long-term incontinence after robot-assisted radical prostatectomy. J Int Med. Res 2017 Jan 1:300060517715396. doi: 10.1177/0300060517715396. [Epub ahead of print].
22. Lardas M, Liew M, van den Bergh RC, De Santis M, Bellmunt J, Vanden Broeck T, et. al. Quality of life outcomes after primary treatment for clinically localised prostate cancer: A systematic review. Eur. Urol. 2017 Jul 27. doi:10.1016/j.eururo.2017.06.035. [Epub ahead of print]
23. Egger SJ, Calopedos RJ, O'Connell DL, Chambers SK, Woo HH, Smith DP. Long-term psychological and quality-of-life effects of active surveillance and watchful waiting aer diagnosis of low-risk localised prostate cancer. Eur Urol 2017 Aug 26. doi:10.1016/j.eururo.2017.08.013. [Epub ahead of print].
24. Lin HY, Lai H, Chen CI, Huang CY. Depression and health-related quality of life and their association with resource fulness in survivors of prostate cancer. Arch Psychiatr Nurs 2017; 31(4): 407–413. doi: 10.1016/j.apnu.2017.04.014.
25. Bock D, Angenete E, Bjartell A, Carlsson S, Steineck G, Stranne J, et. al. Habits and self-assessed quality of life, negative intrusive thoughts and depressed mood in patients with prostate cancer: a longitudinal study. Scand J Urol 2017; 51(5): 353–359. doi: 10.1080/21681805.2017.1326523.
26. Meissner VH, Herkommer K, Marten-Mittag B, Gschwend JE, Dinkel A. Prostate cancer-related anxiety in long-term survivors after radical prostatectomy. J Cancer Surviv 2017;11(6): 800–807. doi: 10.1007/s11764-017-0619-y.
27. Capogrosso P, Sanchez-Salas R, Salonia A, Cathala N, Mombet A, Sivaraman A, et. al. Recovery of urinary continence aer radical prostatectomy. Expert Rev Anticancer ther 2016; 16(10):1039–1052. doi:10.1080/14737140.2016.1233818.
28. Kretschmer A, Hübner W, Sandhu JS, Bauer RM. Evaluation and management of postprostatectomy incontinence: A systematic review of current literature. Eur Urol Focus 2016; 2(3): 245–259. doi: 10.1016/j.euf.2016.01.002.
29. Качмазов А.А., Ромих В.В., Серебряный С.А. Регулируемая слинговая система Argus в лечении недержания мочи у мужчин. Экспериментальная и клиническая урология 2012. (1): 63–67.
30. Siracusano S, Visalli F, Favro M, Tallarigo C, Saccomanni M, Kugler A, et. al. Argus-T sling in 182 male patients: Short-term results of a multicenter study. Urology. 2017 Sep 13. doi:10.1016/j.urology.2017.07.058. [Epub ahead of print].
31. Ferro M, Bottero D, D'Elia C, Matei DV, Cioffi A, Cozzi G, et. al. Virtue male sling for post-prostatectomy stress incontinence: a prospective evaluation and mid-term outcomes. BJU Int 2017; 119(3): 482–488. doi: 10.1111/bju.13672.
32. Yafi FA, Powers MK, Zurawin J, Hellstrom WJ. Contemporary review of artificial urinary sphincters for male stress urinary incontinence. Sex Med Rev 2016; 4(2):157–166. doi: 10.1016/j.sxmr.2015.11.004.
33. Santos AC Junior, Rodrigues LO, Azevedo DC, Carvalho LM, et. al. Artificial urinary sphincter for urinary incontinence after radical prostatectomy: A historical cohort from 2004 to 2015. Int Braz J Urol 2017;43(1):150–154. doi:10.1590/S1677-5538.IBJU.2016.0244.
34. Железная А.А., Чайка К.В., Петренко Н.В. Отношение к болезни и качество жизни у пациенток с недержанием мочи. Медико-социальные проблемы семьи. 2011;16(2):70–74.
35. Dräger DL, Harke NN, Sievert KD, Protzel C, Hakenberg OW. Psychosocial stress in patients with prostate cancer: Experiences by using psychooncological screening questionnaires. Urologe A 2017; 56(11):1445–1449. doi: 10.1007/s00120-017-0458-5.
Статья опубликована в журнале "Экспериментальная и клиническая урология". Номер №4/2017 стр. 20-26









Комментарии